Aporte Al Trabajo Colaborativo
-
Upload
jholeidi-valarezo-fernandez -
Category
Documents
-
view
86 -
download
0
Transcript of Aporte Al Trabajo Colaborativo

Actividad No. 2 Reconocimiento del curso
Trabajo colaborativo
Curso Académico Química General
Grupo 201102_103
Rubén González Padilla
Codigo. 72278775
Tutora:
Stella Díaz Neira
Programa de:
Ingeniería Agroforestal
Bogotá D.C Febrero de 2012

INTRODUCCION
La ubicuidad de la química en las ciencias naturales hace que sea considerada como una de las ciencias básicas. La química es de gran importancia en muchos campos del conocimiento, como la biología, la farmacia, la medicina, entre otros.
En el presente trabajo se plasma el recorrido que se realizo por el modulo de Química general donde recordamos temas vistos en el bachillerato, se aprecian aspectos muy importantes como las unidades de concentración, los estados de la materia, las propiedades de las soluciones.
La finalidad de este trabajo es que nosotros como alumnos nos apropiemos de las temáticas del curso de química, visualicemos cada uno de los link que tiene el aula virtual con la realización de los cuadros que anexamos de esta manera se facilitara la el manejo del curso pues podemos observar que contamos con un software didáctico y varios ejemplos en el modulo.

OBJETIVOS
Más concretamente, este trabajo se centra en el conocimiento del aula virtual, tener el pleno conocimiento de cada uno de los componentes que facilitan el desarrollo de las actividades.
Establecer los conceptos fundamentales que nos permitan la comprensión de los fenómenos químicos.
Adquirir los conocimientos mínimos necesarios para que se nos facilite la comprensión de otras asignaturas relacionadas con el campo de la química.
Proyectar los conocimientos adquiridos en el curso de química general para la solución, a lo largo del ejercicio en nuestra carrera profesional, de problemas reales.
Aprender a plantear y solucionar problemas a través de una metodología sistemática y práctica.
Desarrollar en el alumno la capacidad de aprender a aprender.
Utilizar efectivamente el análisis dimensional para la solución de problemas ya sea virtual o presencial.
Utilizar los conocimientos de estequiometria para resolver problemas que involucren, densidad, masa, o moles.
Conocer las distintas reacciones químicas en solución acuosa y pueda predecir productos de reacción.
Comprender el concepto de energía y pueda realizar problemas utilizando la ley de Hess resumida.
Visualizar la estructura electrónica de los átomos y comprendamos la conexión de esta con las propiedades periódicas de los elementos.
Conocer los diferentes tipos de enlaces químicos y que pueda representar moléculas utilizando las estructuras de Lewis.

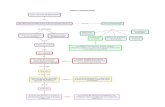
Cuadro 1.Revisión Tópicos
Tópico Nº Elementos Breve descripción de cada elemento
Tópico cero
Noticias del aula En el encontramos las novedades y anuncios del aula por parte del tutor y que no puede ser respondido por parte del estudiante.
Foro General del curso En este espacio el estudiante y tutor podrán discutir temas en general.
Agenda En esta encontramos los cronogramas de fechas y horas de apertura y cierre de las actividades.
Portafolio de grupo wiki Permite a los estudiantes y tutor trabajar juntos en el desarrollo de contenidos o temas colectivos con temas específicos.
Glosario Encontramos los significados de términos desconocidos.
Tópico uno( contenido)
Presentación del curso Misión del curso Ficha técnica Química de curso
Para que fue diseñado el modulo del curso
Protocolo del Curso Todo el contenido del curso que vamos a realizarModulo química general Guía para el desarrollo del laboratorio Contenido en Línea
Modulo y protocolo no para descargar sino para navegarlo en línea
Guía Componente Practico
Se hallan las guías de laboratorio.
Tópico dos ( fases de reconocimiento)
Actividad 1: Revisión de Presaberes
Primera tarea para empezar a conocer el curso
Actividad 2 : Reconocimiento del Curso
Foro para la realización del primer trabajo colaborativo no. 1 y ademas la presentación de cada integrante.
Act 2 : Reconocimiento del Curso - Tarea
En este espacio encontrarán la realimentación y calificación de su trabajo colaborativo. Los trabajos colaborativos se colocan en el Foro de reconocimiento, favor NO colocarlos en este espacio .
Tópico tres
Recurso de aprendizaje 1. Enlace químico
Evaluación de los conocimientos que uno posee de los temas de la unidad
Recurso de aprendizaje Unidad 1

( actividades unidades)
Actividad 3. Reconocimiento Unidad 1
Evaluación acerca de todo lo relacionado en la unidad uno
Actividad 4: Lección Evaluativa profundización Unidad 1
Act. 4: Lección Evaluativa Profundización
Actividad 5 Quiz 1 Evaluación final de la unidad uno Actividad 6: Prácticas de Laboratorio
informe de las prácticas de laboratorio 1, 2, 3
Software partículas de los átomos y iones
Ayuda didáctica para realizar ejercicios con los átomos
Software configuración electrónica
Ayuda didáctica para realizar una configuración electrónica
Tópico cuatro Mini curso SolucionesRecurso de aprendizaje
UNIDAD 2Ayuda virtual del contenido de unidad dos
Actividad 7: Reconocimiento Unidad 2
Evaluación de los conocimientos que uno posee de los temas de la unidad
Actividad. 8: Lección evaluativa Profundización Unidad 2
Evaluación acerca de todo lo relacionado en la unidad dos
Actividad 9: Quiz 2 Evaluación final de la unidad dos Actividad 10: Práctica de Laboratorio
informe de las prácticas de laboratorio 4,5,6
Tópico cinco Recurso de aprendizaje Unidad 3
Ayuda presentación en power point del contenido de unidad tres
Actividad. 11 Reconocimiento unidad 3
Evaluación de los conocimientos que uno posee de los temas de la unidad tres
Actividad 12: Lección Evaluativa Profundización Unidad 3
Evaluación acerca de todo lo relacionado en la unidad tres
Actividad 13: Quiz 3 Evaluación final de la unidad tres Actividad 14: Práctica de laboratorio
informe de las prácticas de laboratorio 7,8,9
Tópico seis Actividad. 15. 201102 - Examen Nacional
Evaluación Final del curso Química General

Cuadro 2.Revisióndel módulo
UNIDAD CAPITULO LECCIONNo. Nombre No. Nombre No. nombre
UNO ESTRUCTURA DE LA MATERIA
1 ELEMENTOS Y COMPUESTOS QUIMICOS
1 Estructura de los Átomos2 Configuración Electrónica3 Tabla Periódica4 Propiedades periódicas de los elementos5 Compuestos Químicos. Estructura6 Enlaces Químicos.
2
ESTADOS DE LA MATERIA
7 Teoría Cinético Molecular8 Estado Sólido9 Estado Liquido10 Estado Gaseoso11 Gases ideales12 Cambios de estado
3CANTIDAD DE SUSTANCIA
13 Masa atómica y masa molecular14 Mol y Número de Avogadro15 Masa Molar
AUTOEVALUACION UNIDAD UNO
DOSMEZCLAS
4 SOLUCIONES VERDADERAS
16 Componentes de una solución17 Clasificación de las Soluciones18 Unidades de Concentración. Unidades Físicas19 Unidades de Concentración. Unidades Químicas
20 Propiedades Coligativas de las Soluciones
5 SUSPENCIONES Y COLOIDES
21 Suspensiones.22 Coloides

23 Comparación de las propiedades de las soluciones, coloides ySuspensiones.
6 EQUILIBRIO QUIMICO
24 Generalidades del Equilibrio Químico25 Constante de Equilibrio26 Principio de L´Chatelier27 Equilibrio Iónico28 Porcentaje de disociación29 Producto iónico del agua30 Potencial de Hidrógeno (pH)
AUTOEVALUACION UNIDAD DOS
TRES CAMBIOS QUIMICOS 7
__
8
REACCIONES QUÌMICAS
__________________
OXIDACIÓN-REDUCCIÓN
31 Ecuación química32 Clasificación de las reacciones33 Leyes Ponderales34 Balanceo de ecuaciones35 Reacciones de oxidación reducción36 Número de oxidación37 Oxidación y reducción38 Balanceo redox por método del cambio del No. de oxidación39 Balanceo redox por método del ion electrón
9 ESTEQUIOMÉTRIA 40 Relación estequiométrica molar REM41 Reactivo Límite42 Pureza de los reactivos43 Rendimiento de una reacción44 Cálculos de Estequiometria que involucran gases
y soluciones

Cuadro 3.Revisión del módulo (continuación)
Unidad Capítulo Conceptosclaves(identifique 10) por cadaCapítulo
Leyes yprincipiosidentifique una por cada capítulo)
Númerode Ejerciciosresueltos
NúmeroAuto Evaluaciones
Para qué me sirve
Uno
1
Átomos, Estructuras de Lewis de Pauli
Principio de Exclusión
45 4
Para comprender la estructura del átomo, sus partes y distribución de electrones.
A demás de cómo se forman las moléculas, entendiendo la teoría de enlace. Diferencie los elementos de los de los compuestos y las propiedades.
protones, electrones, Neutronessubatómicas, Configuración Electrónica,Tabla Periódica, Tamaño atómico, Afinidad electrónicaEnlaces Químicos
2
Volumen Ley de Charles
Ley de Avogadro 18 2
Las bases sobre los diferentes estados de la materia y el estudio de los más representativos, para que conceptualice y Comprenda el por qué de sus diferencias.
PresiónEvaporaciónPresión de vapor Temperatura de FusiónCohesiónadhesión temperatura de ebulliciónDifusiónAcción capilar
3 Molécula Mediciones exactas. 5 1 La temperatura, Entender la diferencia entre masa atómica, masa molecular y masa molar.
mol Masa

Realizar Inter -conversiones masa, número de moles y cantidad de partículas en una mol (número de Avogadro).
cantidad de sustanciaMoléculasIsótoposunidades estructuralesMolesMolar
Dos
4
Soluto,
Propiedades Coligativas 19 1
Soluciones y las formas de expresar y calcular la concentración de las soluciones
solvente, solubilidad, solución,concentración soluciónporcentaje de soluciónConcentración molarMolaridad concentración normalModalidad
5
Dispersiones groseras Reconocer los coloides, diferencias de las soluciones verdaderas y de las suspensiones
Dispersiones finasSuspensionesDispersarteSoluciones ColoidesEmulsiónDispersa
6
micela Efecto Tyndall
No hay ejemplos Liófilo
PHÁcidosBasesDisociación

constante de disociaciónacido fuerte y débil
base conjugadaCatalizador
Tres
7
Ecuación Química Principio de Ley Chatelier
Ley de las proporciones múltiples
Ley de los pesos equivalentes.
Ley de la conservación de la masa
7 2 Para entender el equilibrio químico de las reacciones reversibles, relacionarlo con el equilibrio iónico de las reacciones de ionización de ácidos y bases para realizar cálculos de pH de estos últimos
ReacciónEndotérmicaReacciónExotérmicaCombustiones dematerialesorgánicosfórmula molecular
Método del ensayo y errorBalanceo de EcuacionesCon transferenciade electrones(Oxido-reducción
8
Reacción química, Ley de la conservación
Reglas para asignar un número de oxidación
Conceptualizar, cómo se representa una reacción química (Ecuación química), recordar los conceptos de oxidante y reductor, conceptualizará el concepto de número, de oxidación y el ajuste de reacciones, redox por el método de cambio en el método del ión– Electrón.
Ecuación químicaformula molecularÁcidosBasesSalesMétodo de oxido-reducciónLeyes Pondérales SíntesisExotérmicasRelación Estequiométrica Molar
Ley de la conservación
7 3 Interpretar y aplicar la ley de la, conservación de la masa en la, realización de cálculos Cálculos

9
Estequiométricos estequiometricos.. Reactivo límite o limitanteCondiciones experimentalesecuación químicaRendimiento real Rendimiento porcentualRendimiento teórico

CONCLUSION
Se realizo un vistazo a las unidades y capitulo del modulo general de química y al mismo tiempo darnos cuenta de la importancia de la química en muchos aspectos de la vida y lo relevante que es la preparación de cualquier producto.
Se nos presentan buenas ayudas para sacar adelante nuestro aprendizaje al Contar con suficiente material didáctico (recursos) que nos aumentan la comprensión del curso de química general.
Tenemos que observar cada uno de los link que encontramos en el aula virtual pues en ellos tenemos herramientas de trabajo y ejercicios para poner en práctica los conocimientos adquirido a medida que se van dando las lecciones.

BIBLIOGRAFIA
Modulo Química General
CIBERGRAFIA
http://campus03.unadvirtual.org/moodle/mod/forum/post.php. En este modulo se encuentran los contenidos del programa de quimica (consulta febrero de 2012) páginas 5-202