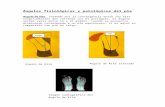
Hallazgos clínico patológicos en dos casos de psitácidos ...
ASPECTOS PATOLÓGICOS DE LA REPARACIÓN
-
Upload
marisol-lugo -
Category
Documents
-
view
625 -
download
7
Transcript of ASPECTOS PATOLÓGICOS DE LA REPARACIÓN

ASPECTOS PATOLÓGICOS DE LA REPARACIÓN
Las complicaciones durante la cicatrización de las heridas se pueden relacionar con alteraciones en cualquiera de los elementos básicos del proceso reparativo. Estas alteraciones se pueden agrupar en tres categorías generales:
1) formación deficiente de la cicatriz:
La formación inadecuada de tejido de granulación o del ensamblaje de la cicatriz puede causar dos tipos de complicaciones: dehiscencia de la herida y ulceración. La dehiscencia o rotura de una herida es más frecuente tras la cirugía abdominal y se debe al aumento de la presión abdominal. Los vómitos, la tos o el íleo pueden generar estrés mecánico sobre una herida abdominal. Las heridas se pueden ulcerar porque tienen una vascularización inadecuada durante la cicatrización. Por ejemplo, las heridas de las extremidades inferiores en pacientes con enfermedad vascular periférica aterosclerótica se ulceran de forma típica. Las heridas que no se curan aparecen también en zonas insensibles. Estas úlceras neuropáticas se describen en ocasiones en enfermos con neuropatía periférica diabética.
2) formación excesiva de componentes de la reparación:
Una formación excesiva de los componentes del proceso de reparación puede dar lugar a cicatrices hipertróficas o queloides. La acumulación de una excesiva cantidad de colágeno puede generar una cicatriz elevada, que se llama cicatriz hipertrófica; si el tejido cicatricial se extiende más allá de los márgenes de la herida original y no regresa, se denomina queloide. La formación de queloides parece depender de una predisposición individual y por motivos desconocidos esta alteración es algo más frecuente en los afroamericanos. Las cicatrices hipertróficas se suelen observar tras lesiones térmicas o traumáticas que afectan a las capas profundas de la dermis. Se produce colágeno por los miofibroblastos, que persisten en la lesión gracias a la producción autocrina de TGF - y el establecimiento de adherencias focales. La granulación exuberante es otro tipo de alteración de la cicatrización que consiste en la formación de una cantidad excesiva de tejido de granulación, que protruye por encima del nivel de la piel circundante y bloquea el proceso de reepitelización (este proceso se ha llamado, con gran fervor literario, la carne orgullosa). El tejido de granulación excesivo se debe extirpar con el bisturí eléctrico o mediante resección quirúrgica para permitir la recuperación de la continuidad del epitelio. Por último (y por suerte, con escasa frecuencia), las cicatrices incisionales o las lesiones traumáticas pueden seguirse de la proliferación exuberante de fibroblastos y otros elementos del tejido conjuntivo que pueden, de hecho, recidivar tras la resección. Este tipo de lesiones se llaman desmoides o fibromatosis agresivas, y se consideran lesiones intermedias entre las proliferaciones tumorales benignas y malignas (aunque de bajo grado). La frontera entre las hiperplasias benignas propias de la reparación y las neoplasias es muy poco nítida.

3) formación de contracturas:
La contracción del tamaño de la herida es una parte importante del proceso de cicatrización normal. Una exageración de este proceso da lugar a la contractura y provoca deformidades en las heridas y los tejidos circundantes. Las contracturas se desarrollan con especial frecuencia en las palmas, plantas y la superficie anterior del tórax. Las contracturas se suelen observar tras quemaduras graves y pueden limitar el movimiento de las articulaciones.
Fibrosis
El depósito de colágeno forma parte de la cicatrización normal de las heridas. Sin embargo, el término fibrosis se aplica de forma más amplia para aludir al depósito excesivo de colágeno y otros componentes de la MEC en un tejido. Como se ha comentado antes, los términos cicatriz y fibrosis se usan como sinónimos, pero fibrosis suele aludir al depósito de colágeno en las enfermedades crónicas. Los mecanismos básicos asociados al desarrollo de fibrosis en las enfermedades inflamatorias crónicas se parecen, en general, a los mecanismos de cicatrización de las heridas cutáneas. Sin embargo, a diferencia de los estímulos de corta duración que activan la secuencia ordenada de pasos implicados en la cicatrización de las heridas cutáneas, los estímulos lesivos ocasionados por infecciones, reacciones auto inmunitarias, traumatismos y otros tipos de daños tisulares persisten en las enfermedades crónicas, provocando disfunción y, con frecuencia, insuficiencia orgánica. La persistencia de una lesión se asocia a inflamación crónica, que se caracteriza por la proliferación y activación de linfocitos y macrófagos, y la producción de abundantes factores de crecimiento inflamatorios y fibrogénicos y citosinas. La respuesta del huésped frente a los estímulos lesivos se organiza para tratar de eliminarlos y luego reparar el daño. La onda inicial de respuesta del huésped frente a los invasores externos y el daño tisular genera macrófagos activados por la vía clásica», que consiguen ingerir y destruir los microbios y tejidos muertos de una forma eficaz. A continuación, se acumulan los «macrófagos activados por vía alternativa», que suprimen las actividades microbicidas e intervienen en la remodelación tisular, al tiempo que inducen la angiogenia y la formación de cicatrices. Las citosinas que inducen la activación de los macrófagos por la vía clásica las producen los linfocitos T H 1 y corresponden sobre todo a IFN - y TNF, mientras que la activación por vía alternativa de los macrófagos se suele inducir por IL-4 e IL-13, citosinas elaboradas en los linfocitos T H 2 y otras células como los mastocitos y eosinófilos. Los macrófagos activados por la vía alternativa producen TGF - y otros factores de crecimiento implicados en los procesos de reparación. TGF- casi siempre participa como un importante agente fibrogénico en estas enfermedades, independientemente de la causa original. Se produce por la mayor parte de las células del tejido de granulación e induce la emigración y proliferación de los fibroblastos, aumenta la síntesis de colágeno y fibronectina y reduce la degradación de la MEC, porque inhibe las metaloproteinasas. Las concentraciones de TGF - en los tejidos no se regulan principalmente por la transcripción del gen, sino que dependen de la activación tras la transcripción del TGF - latente, la velocidad de secreción de la molécula activa y factores de la MEC que fomentan o reducen la actividad de TGF - .

Los mecanismos responsables de la activación del TGF - en la fibrosis no se conocen de forma exacta, pero la muerte celular mediante apoptosis o necrosis y la producción de especies reactivas del oxígeno parecen importantes activadores, independientemente del tejido. Del mismo modo, las células que producen el colágeno tras ser estimuladas por TGF - varían según el tejido. En la mayor parte de los casos, como la fibrosis pulmonar o renal, los miofibroblastos son la principal fuente del colágeno, mientras que en la cirrosis hepática las principales productoras de colágeno son las células estrelladas.
Estudios recientes han aportado pruebas del importante papel de la osteopontina (OPN) en la cicatrización de las heridas y la fibrosis. La OPN se expresa mucho en la fibrosis a nivel cardíaco, pulmonar, hepático, renal y en algunos tejidos más. En experimentos animales, el bloqueo de la expresión de OPN durante la cicatrización de las heridas reduce la formación de tejido de granulación y cicatrices. Aunque los mecanismos mediante los cuales la OPN estimula la fibrosis no se comprenden bien, los datos recientes demuestran que OPN es un mediador de la diferenciación de los miofibroblastos inducidos por TGF - .A diferencia de las heridas en adultos, las heridas de la piel fetal se curan sin cicatriz. Se han planteado varios factores para estimular esta curación sin cicatrices, como la secreción de formas no fibrogénicas de TGF - , carencia de osteopontina o la ausencia de una respuesta T H 2, pero no se han obtenido resultados concretos.
Dada la grave disfunción orgánica secundaria a la fibrosis, se están realizando intensos esfuerzos por desarrollar agentes antifibróticos útiles. Dentro de los agentes que se están estudiando, cabe citar los inhibidores de la unión o transmisión de señales por TGF - , los inhibidores de la angiogenia, los antagonistas de los receptores de tipo señuelo y el receptor de degeneración IL-13Ra2, que bloquea la IL-13.
Los trastornos fibróticos incluyen múltiples cuadros, como la cirrosis hepática, la esclerosis sistémica, las enfermedades fibrosantes pulmonares (fibrosis pulmonar idiopática, neumoconiosis y fibrosis pulmonar secundaria a radiación o fármacos), pancreatitis crónica, glomerulonefritis y pericarditis constrictiva. Estos procesos se comentan en los capítulos correspondientes de esta obra.