Disoluciones I. ¿Qué es una sustancia pura? Las sustancias puras están formadas por partículas...
-
Upload
custodia-che -
Category
Documents
-
view
26 -
download
0
Transcript of Disoluciones I. ¿Qué es una sustancia pura? Las sustancias puras están formadas por partículas...

Disoluciones IDisoluciones I

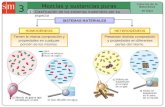
¿Qué es una sustancia pura? Las sustancias puras están formadas por partículas (átomos o moléculas) iguales, tienen una composición fija, no pueden separase por medios físicos. Tienen propiedades específicas: densidad, la temperatura permanece constante en los cambios de estado temperatura de ebullición y fusión), solubilidad, conductividad térmica y eléctrica y numerosas propiedades más. Por ejemplo el alcohol etílico (componente de las bebidas alcohólicas) tiene, entre otras, las siguientes propiedades específicas: - densidad 0,79 g/ml - punto de fusión –114ºC - punto de ebullición 78,5ºC Además, es incoloro, de olor característico y totalmente miscible con el agua. Otro ejemplo: Cuando calentamos y evaporamos agua pura no queda ningún residuo y el líquido obtenido al condensar el vapor agua sigue siendo agua pura.
Para distinguir una sustancia pura de otra nos basamos en sus propiedades.


Las sustancias puras a su vez se clasifican en sustancias simples y sustancias compuestas. En las sustancias simples encontramos a los elementos químicos, y en las sustancias compuestas encontramos a los compuestos químicos.


¿Qué es una mezcla? Las mezclas son una asociación física de dos o más sustancias puras sin que exista reacción química entre ellas, tienen una composición variable, pueden separarse por medios físicos, poseen temperaturas variables durante el cambio de estado.

Mezclas comunes
Composición
Granito Cuarzo, feldespato, y micaPetróleo Metano, etano, propanoOrina Urea, aguaAlcohol medicinal Alcohol y aguaLejía Agua, hipoclorito de sodioSangre Agua, hemoglobina, glucosaCoca Cola Agua, CO2, cafeína
Vinagre Agua, ácido acéticoGasolina Hetpano, octano


Las mezclas homogéneas se caracterizan porque sus componentes no pueden distinguirse, sólo se observa una sola fase. Por ejemplo, si mezclamos agua (fase líquida) con sal (fase sólida) y agitamos bien la mezcla, la sal se disuelve en la fase líquida. ¿Puedo distinguir donde está la sal y el agua? No.Un caso especial de mezclas homogéneas sólidas son las aleaciones, que son mezclas de metales fundidos, por ejemplo el bronce y el acero. Las mezclas homogéneas líquidas se llaman disoluciones químicas, y en ellas es donde ocurren las reacciones químicas de la naturaleza.


Las heterogéneas se caracteriza porque se pueden distinguir a simple vista sus componentes, o con ayuda de un microscopio. Los componentes pueden separarse por medio de filtración, tamizado, centrifugación, decantación, etc.



DEFINICIONES. FORMAS DE EXPRESARDEFINICIONES. FORMAS DE EXPRESARLA CONCENTRACIÓN.LA CONCENTRACIÓN.11
Disolución: mezcla homogénea de dos o más sustancias.
Clasificación de las disoluciones
• Dependiendo de la naturaleza de la fase:
Sólida Líquida Gaseosa

Clasificación de las disoluciones líquidas
• Dependiendo del estado del soluto:
Soluto sólido Soluto líquido Soluto gaseoso
• Dependiendo del disolvente: AcuosasNo acuosas
• Dependiendo de la naturaleza del soluto:
Electrolíticas: soluto se disocia en iones (ej. sal)(conducen la corriente eléctrica)
No electrolíticas: soluto no se disocia en iones (ej. azúcar)(no conducen la corriente eléctrica)

La descripción de una disolución implica conocer suscomponentes y sus cantidades relativas concentración.
Formas de expresar la concentración
• Fracción molar (x)
Tot
ii n
nx
1xi
i
• Representa el tanto por uno en moles de i• Adimensional• 0 xi
• Molalidad (m)
disolvente kg
nm i
i • Unidades: molkg-1 (molal,m)• Ventaja: No varía con T

• Molaridad (M)• Unidades: molL-1 (molar,M)• Desventaja: Varía con T• Ventaja: Facilidad para medir V
disolución L
nM i
i
• Normalidad (N)• Unidades: equivL-1 (normal,N)• Desventaja: depende de la reacción• Uso no recomendado
disolución L
(i) esequivalentNi
equivalentes (i) = ni valencia Protones transferidos en rcc. ácido-baseElectrones transferidos en rcc. redox
• Porcentaje en peso (% p/p)
100disolución masa
soluto masapeso% 610
disolución masa
soluto masappm
Partes por millón (ppm)

a) Calcule la molaridad de una solución que contiene 0.0345 mol de NH4Cl en 400 mL de solución
b) ¿cuántos moles de HNO3 hay en 35.0 mL de una solución 2.20 M de ácido nítrico?
c) ¿cuántos mililitros de una solución 1.50 M de KOH se necesitan para suministrar 0.125 mol de KOH?.

Un vinagre tiene 6.02% m/m de ácido acético CH3CO2H. ¿Cuántos gramos de ácido acético hay en una botella de vinagre de 355 ml?. Suponga una densidad de 1.01 g/ml

El ácido sulfúrico H2SO4(ac) 6.0 M tiene una densidad de 1.338 g/mL. ¿Cuál es el %m/m, la fracción molar, la molalidad del ácido en esta disolución?

Una disolución al 30% m/m de HNO3 (masa molar 63 g/mol) en agua tiene una densidad de 1.18 g/mL. ¿Cuál es la molaridad, la fracción molar y la molalidad del HNO3 en esta disolución?

Un volumen de 10 ml de KNO3 2.55 M, se diluye hasta 150 ml: Determine la concentración (en gr/l) de la disolución diluida. ¿Cuál es la molaridad, la fracción molar y la molalidad de la nueva disolución?

Calcular la molaridad de una disolución que contiene 30.3 g de (NH4)Cr2O7 en 250 ml de agua. ¿Cuál es la fracción molar y la molalidad de la disolución?