Ejercicios de Ecuacion de Clayperon
-
Upload
stebhan-sanchez -
Category
Documents
-
view
34 -
download
2
description
Transcript of Ejercicios de Ecuacion de Clayperon
Determinar el nmero de componentes de los ejercicios del 1 al 6:
F= Grados de libertad.
C= Componentes.
P= Fases.
1) H2(g) + N2(g)
C= 2
2) NH2
C=1
3) Una solucin de Ca (NO3) en agua.
C= 2
4) Una solucin acuosa de NaCl + Na2SO4
C= 2
5) Una solucin acuosa de KCl + Na2SO4
C=3
6) C12H22O11(S) + una solucin acuosa de C12H22O11
C=2
Actividad No. 6: Determinar el nmero de fases de los sistemas del 1 al 6, correspondientes a la actividad No. 5:
F= Grados de libertad.
C= Componentes.
P= Fases.
1) H2(g) + N2(g)
P= gas
2) NH2
P= gas (1)
3) Una solucin de Ca (NO3) en agua.
P= liquida (1)
4) Una solucin acuosa de NaCl + Na2SO4
P= liquida (1)
5) Una solucin acuosa de KCl + Na2SO4
P= liquida (1)
6) C12H22O11(S) + una solucin acuosa de C12H22O11
P= solida y liquida (2)
Actividad No. 11: Determinar los grados de libertad de los sistemas del ejercicio No. 6:
F= Grados de libertad.
C= Componentes.
P= Fases.
1) H2(g) + N2(g)
C= 2
P= gas (1)
F= 2 1 + 2
F=3
2) NH2
C=1
P= gas (1)
F= 1 1 + 2
F=2
3) Una solucin de Ca (NO3) en agua.
C= 2
P= liquida (1)
F= 2 1 + 2
F=3
4) Una solucin acuosa de NaCl + Na2SO4
C= 2
P= liquida (1)
F= 3 1 + 2
F=4
5) Una solucin acuosa de KCl + Na2SO4
C=3
P= liquida (1)
F= 3 1 + 2
F=4
6) C12H22O11(S) + una solucin acuosa de C12H22O11
C=2
P= solida y liquida (2)
F= 2 2 + 2
F=2
ACTIVIDAD # 12 RESOLVER PROBLEMAS.
Calcule los grados de libertad al punto triple del agua.
Formula:
F= C P + 2
Siendo C, los componentes y P las fases.
1. Agua (Solido)
2. Agua (Liquida)
3. Agua (Gaseosa)
Entonces:
F= 1 3 + 2
F= - 2 + 2
F= 0
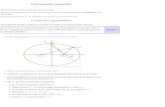
ACTIVIDAD # 13 REALIZAR UNA GRAFICA DE PUNTOS CON LOS DATOS REALIZADOS.
T c
Actividad 14.-Resolver problemas.
Obtener mediante la ecuacin de Antoine la presin de vapor de los siguientes sustancias en Kpa , Pa , Atm, mmHg.
ECUACION DE ANTOINE
NOMBRE
TEMPERATURA
A
B
C
PROPILENO
26C+273 K= 299K
13.8782
1875.25
-22.9101
TOLUENO
28C+273 K=301 K
14.2515
3242.38
-47.1806
OXIDO DE ETILENO
29C+273 K=302K
14.5116
2478.12
-33.1582
ACETILENO
24C+273K=297K
14.8321
1836.66
-8.4521
Formula
1.- PROPILENO A 26C
= 1195.15Kpa
1195.15Kpa= 1195151.602 Pa.
1195.15Kpa
2.- TOLUENO A 28C
Pa
3.- OXIDO DE ETILENO A 29C
4.- ACETILENO A 24C
Act. 15 Del ejercicio de prctica No 3 resolver tomando en cuenta P2 = 1.5 atm y P2=2.5 atm Grafica T2 ebullicin Vs presin y escribir conclusin
Vapor H2O Gas ideal
Hm = 2239.4
a) p1= 1 atm p2= 1.5 atm T1= 373.15 k
T2 = = 385.20 K
B) P1 = 1 atm
P2 = 2.5 atm
T1= 373.15
T2 = = 401.60 K
P1 = 1 atm
P2 = 1.5 atm
T1= 373.15
T2 = 385.20K
P1 = 1 atm
P2 = 2 atm
T1= 373.15
T2 = 395.25K
P1 = 1 atm
P2 = 2.5 atm
T1= 373.15
T2 = 401.60K
atm
Temperatura K
Conclusin: se puede observar que la temperatura va con respecto a la presin si se est aumentando la temperatura tambin aumentara su esta disminuye la temperatura disminuir:
Practica 2 ejercicios.Determinacin de la capacidad calorfica
Cpa M2 (T2 - T3) = C + Cpa M1 (T3 - T1)
m=masa (g)
T= Temperatura (C)
C= Capacidad calorfica del calormetro
Cpa H2O =
1) Determinando la masa
m1 = V1=
m2 = V2=
H2O =
m1 =
m2 =
2) Determinar la capacidad calorifica del calorimetro=
m1 =150g T3=27C
m2 = 25g
T1=24 C
T2=50C
De la formula (1), despejamos C=
c= -
c==
Sustituyendo valores:
c= -
c= -
Ejercicio 1 De la practica 3
Determine la relacin de cambio de presin de equilibrio con la temperatura, para un cambio de fase de agua solida a liquida a 273.15 K, en atm.K-1 dado que fusH= 6.01 KJ.mol-1. VL=0.0180 L.mol-1 y Vs = 0.0196 L.mol -1.
DATOS:
Solido Liquido
T= 273.15 K
fusH= 6.01 KJ.mol-1
L= 0.0180 L.mol-1
S = 0.0196 L.mol-1
= 18 g.mol-1
Para cambio de fase (Fusin)
m= Vm (S) Vm (S)
Empleando frmulas:
FusH= 0.61 = 6010
6010 -3L.atm]= 59.318
FusVm= (0.0180 L.mol-1) (0.0196 L.mol-1)
m = -1.6 x 10 -3
Sustituyendo valores.
Ejercicio 2
2. Bajo la presin de una atmosfera, el sodio funde a 97.8 C. observndose un aumento del volumen especifico de 0.0279 ml (g) -1. Calclese la temperatura de fusin del sodio a 100 atm.
PM= (H2O) ; 18
fusH =630
P= 1 atm = 1,013x
Ejercicio 3
calcular la temperatura a la que hervir el agua sometida a una presin de 2 atm, sabiendo que la temperatura de ebullicin normal es de 100c a nivel del mar. el calor de vaporizacin del agua se supone constante e igual a 2239.4 y R= 8.3144 NOTA: considere el vapor de agua como gas ideal.
Te=?
P2= 2 atm
T1=100 c + 273=373 k
P1= 1 atm
H=2239 J/g
R=8.31 J/mol.k
Fluido Agua
Vapor H2O Gas ideal
Pvb=RT
sustituyendo V en 1
=
Conversiones:
sustituyendo
Ejercicio 4
4.- Utilice los datos de la tabla 7.1 para estimar el punto de ebullicn del Argn 1.5 atm. Reporte sus resultados en K.
Elemento
Tpn
(K)
fusHm
(KJ/mol)
fusSm
(J/molK)
Tpen
(K)
vapHm
(KJ/mol)
vapSm
(J/molK)
Argn
83.8
1.21
14.4
87.3
6.53
74.8
Observemos los datos que tenemos y el Argn es un gas ideal por tanto utlizaremos los siguientes datos y formula de Clapeyron.
Datos a utilizar:
P1= 1atm
P2= 1.5 atm
T1= Tpn= 87.3K
vapHm= 6.53KJ/mol
T2= ?
vapHm= 6.53KJ/mol = 6530 J/mol
Utilizando la formula de Clapeyron para gases ideales, y despejando T2, tenemos que: T2=
Sustituyendo los datos en la ecuacion:
T2= =
P vapor (Kpa)1020304050607080901001.2282.33799999999999874.2427.37512.3319.92000000000000231.1647.33999999999999670.099999999999994101.32499999999999P vapor (Kpa)037037538038539040040511.522.5