Enlace covalente
Transcript of Enlace covalente

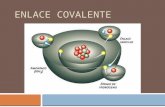
ENLACE COVALENTE

Se da entre elementos no metálicos.
Comparten e- con mayor ó menor intensidad, tendiendo a estabilizarse, es decir, a alcanzar el octeto y adquirir así la configuración electrónica del gas noble más cercano.
Forman moléculas

Representación
• Estructura de Lewis o Fórmula electrónica: se representan con puntos o curces los e- del nivel más externo (e- de valencia) de todos los átomos que la conforman, incluidos los compartidos y los no compartidos.

• Fórmula desarrollada: representa mediante un guión los pares de e- que participan de la unión y con puntos los e- no compartidos.
• Fórmula semidesarrollada: solo representa mediante un guión los pares de e- que participan de la unión covalente.

Según la cantidad de pares de electrones que compartan entre los dos átomos
Los enlaces covalentes comunes pueden ser de tres clases:
• Simple: comparten 1 solo par de e-
• Doble: comparten 2 pares de e-
• Triple : comparten 3 pares de e-

Las uniones covalentes también pueden ser:
Coordinada o dativa: • Es la unión covalente en la cual el par de e- compartido
es aportado por un solo átomo.
• El enlace coordinado, se simboliza en la formula semidesarrollada con una flecha que parte desde el átomo que aporta el par electrónico a la unión.

Ejemplos
Fórmula Molecular
Fórmula Electrónica
Fórmula Desarrollada
Fórmula Semidesarrollada
Cl2O
CO2
Cl2O5