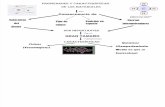
Enlaces quimicos
-
Upload
alma-lorena-arvizu -
Category
Engineering
-
view
143 -
download
0
Transcript of Enlaces quimicos

Alumna: Alma Lorena Arvizu RamirezFacilitador: Jesús Torres Grageda.
Materia: Propiedad de los materiales.
Ing. Industrial en Productividad y Calidad.

• Un enlace atómico es un enlace químico. El enlace químico es el proceso físico responsable de las interacciones entre átomos y moléculas.

• Este enlace se produce cuando átomos de elementos metálicos (especialmente los situados más a la izquierda en la tabla periódica -períodos 1, 2 y 3) se encuentran con átomos no metálicos (los elementos situados a la derecha en la tabla periódica -especialmente los períodos 16 y 17).

Los enlaces covalentes son las fuerzas que mantienen
unidos entre sí los átomos no metálicos (los elementos
situados a la derecha en la tabla periódica -C, O, F, Cl, ...).
Estos átomos tienen muchos electrones en su nivel más
externo (electrones de valencia) y tienen tendencia a ganar
electrones más que a cederlos, para adquirir la estabilidad
de la estructura electrónica de gas noble. Por tanto, los
átomos no metálicos no pueden cederse electrones entre sí
para formar iones de signo opuesto.

• es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y loselectrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí.
• Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas.

• Las fuerzas de Van der Waals o interacciones de Van der Waals, son las fuerzas atractivas o repulsivas entre moléculas (o entre partes de una misma molécula) distintas a aquellas debidas a un enlace intramolecular (Enlace iónico, Enlace metálico y enlace covalente de tipo reticular) o a la interacción electrostática de iones con otros o con moléculas neutras. El término incluye:
• Fuerza entre dos dipolos permanentes (interacción dipolo-dipolo o fuerzas de Keesom).
• Fuerza entre un dipolo permanente y un dipolo inducido (fuerzas de Debye).
• Fuerza entre dos dipolos inducidos instantáneamente (fuerzas de dispersión de London).

• La fuerza por puente de hidrógeno o enlace de hidrógeno es la fuerza atractiva entre un átomo electronegativo y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo. Resulta de la formación de una fuerza dipolo-dipolo con un átomo de hidrógeno unido a un átomo de nitrógeno,oxígeno o flúor (de ahí el nombre de "enlace de hidrógeno", que no debe confundirse con un enlace covalente a átomos de hidrógeno.