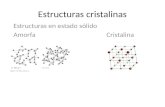
ESTRUCTURAS-CRISTALINAS
-
Upload
samandamachado -
Category
Documents
-
view
8 -
download
0
description
Transcript of ESTRUCTURAS-CRISTALINAS
18
DEDICATORIA
El presente trabajo lo dedicamos primeramente a nuestros padres quien nos da la fortaleza para poder vencer los obstculos y barreras de todos los das, a nuestro docente que se sacrifican da a da por darnos lo mejor de ellos para as poder alcanzar nuestras nuestro objetivo y meta a Dios y tambin alas personas hicieron posible este trabajo de investigacin.
INTRODUCCINLa mayora de los slidos tienen estructura cristalina. Esto quiere decir, que poseen una ordenacin peridica de sus tomos o iones a lo largo de las tres direcciones del espacio. Sin embargo, algunos slidos no presentan dicha ordenacin peridica, son los denominados slidos amorfos. Las estructuras cristalinas pueden ser fcilmente descritas mediante la llamada celdilla unidad, que es la menor unidad que, por repeticin indefinida en las tres direcciones del espacio, genera el cristal. Si conocemos la disposicin exacta de los tomos dentro de una celdilla unidad, conoceremos la disposicin en todo el cristal. La celdilla unidad es siempre un paraleleppedo pudiendo ser especificado su tamao y forma a partir de las longitudes, a, b y c de las tres aristas independientes y los tres ngulos , y entre estas aristas, de tal forma que los valores tanto de las aristas como de los ngulos (parmetros de celdilla) son caractersticos de cada uno de los sistemas cristalinos, que se muestran de forma resumida en la Tabla I. Cualquier slido cristalino puede ser adscrito a uno de los siete sistemas de ejes cristalogrficos o sistemas cristalinos.Los slidos son incomprensibles debido a sus partculas, slo poseen movimiento vibratorio en un espacio muy reducido, se cristalizan adoptando formas geomtricas definidas que son caractersticas de cada sustancia qumica.
La Historia De Los Cristales Daniel Swarovski
Esta marca de lujo de productos fabricados con cristal se ha convertido en una de las firmas ms caras y con mayor reconocimiento mundial. Paradjicamente ha sabido sacarle a las crisis el mejor partido y han sido en estos periodos cuando ha registrado un mayor crecimiento. Su origen est en una mquina casi perfecta para cortar cristal inventada por Daniel Swarovski de cuya diversificacin supo hacer un imperio.La historia de Swarovski es una historia de innovacin, creatividad y conocimiento social. Su fundador, Daniel Swarovski, como no poda ser de otra manera, naci en Bohemia en 1862. Esta parte del Imperio Austrohngaro era uno de los centros industriales ms importantes para el vidrio y el cristal. En la pequea fbrica de su padre se cortaba cristal y fue ah donde naci su vocacin. De joven, Daniel mir siempre el trabajo de su padre. Despus l complet su aprendizaje con su padre, as como con otros cortadores de cristal, hasta que lleg el punto de inflexin en su carrera con la Primera Exhibicin Elctrica en Viena. All le surgi la idea de utilizar las nuevas tcnicas de Siemens y Edison para crear una mquina para el corte de cristal. Nueve aos despus, l estaba listo para registrar una patente: una mquina que cortaba el cristal a la perfeccin de una manera ms rpida y precisa que el trabajo manual. Fue una nueva era para el mundo del cristal. Junto con su familia se muda de Bohemia al Tyrol. Los Alpes proporcionan el factor firme para fundar la compaa all: con bastante agua y energa en forma de agua para impulsar sus mquinas, Daniel Swarovski encontr aqu una situacin ideal para su empresa. De hecho, con sus tres hijos, Wilhelm, Friedrich y Alfred, constituye una planta para la produccin de cristal y proporcional material crudo de calidad superior.En 1913 empez a producir su propio cristal. ste era un hito importante en la historia de la compaa que tomaba un nuevo rumbo. Pronto, estos cristales cortados con formas de joyas causaron gran excitacin y se codiciaron por todas partes.Durante la Primera Guerra Mundial, la escasez de mquinas cortantes y materiales fue la oportunidad para que Swarovski desarrollara sus propias herramientas. De este modo, en 1919 se registr bajo la marca de fbrica Tyrolit.Por otro lado, en los aos veinte, los vestidos de baile se comenzaron a bordar con perlas y cristales. As se embelleci el arte fino del bordado de cristal gracias, sobre todo a otro invento de Swarovski: una cinta de cristal que poda aplicarse directamente a los tejidos, zapatos y todos los accesorios imaginables.Pero su diversificacin fue ms all, esta vez de la mano de su hijo mayo Wilhelm, que produjo el primer prototipo de un par de prismticos en 1935. Estos prismticos abrieron las puertas a la industria de la ptica y se convirtieron en el artculo salvador de la compaa durante la guerra. Hoy Swarovski Optik es el lder de los instrumentos de precisin pticos. Mientras, sus experimentos con vidrios reflectantes de la lnea Swareflex se han vuelto imprescindibles en medios de transporte como trenes y barcos.Durante la dcada de los 50, Swarovski hizo adelantos importantes en el desarrollo de la produccin de la piedra de cristal, las piedras se cubrieron con partculas de metal delgadas para aumentar su brillo. En colaboracin con Christian Dior, Manfred Swarovski, el nieto fundador de la compaa, estos experimentos dieron lugar a Aurora Borealis, cristales que brillaban con los colores del arco iris. Esta novedad se volvi un xito mundial y dio lugar a una nueva tendencia de moda: piedras cubiertas en una variedad de colores con brillos iriscentes.A estos inventos les sucedieron otros como su tecnologa Hot-Fix, que hizo posible agregar brillo a cualquier artculo de ropa o a la aplicacin Strass en los candelabros que se pueden ver en la Opera Metropolitana de Nueva York o en el Castillo de Versalles.Un ratn que da lugar a una nueva pocaCon un ratn de cristal empieza una nueva era para Swarovski: la venta de productos de cristal terminados. Esta creacin, de 1976, adems de ser un objeto representativo de los Juegos Olmpicos de Invierno, fue el primer objeto de cristal color plata de una lnea que ahora incorpora ms de 120 artculos de regalo, que consiguieron convertir a los clientes en coleccionistas, hasta el punto de crear lo que hoy se denomina Sociedad Swarovski a la que pertenecen 400.000 integrantes de 35 pases.Despus lanza su primera lnea de joyera: anillos, pendientes, pulseras o collares. De todas sus creaciones e innovaciones, la ms importante de la firma es, sin duda, el haber convertido al cristal en joyas de gran valor. Pero sus invenciones no se quedaron aqu; jarrones, cuencos, relojes, accesorios de moda, carteras o una malla de cristal que es usada habitualmente por diseadores como Dolce & Gabana, Chanel y Louis Vuitton. La compaa ha llevado a cabo durante estos aos una importante imagen de marca que la ha posicionado como una de las firmas de lujo ms consolidadas, para ello ha colaborado en la realizacin de varias obras de arte contemporneas y ha querido extender sus redes a todos los hbitos sociales desde la decoracin a la moda. De este modo, la ensea ha conseguido poner en marcha una red de ms de 500 tiendas en 120 pases, que se unen a todo un mercado paralelo de objetos.Pero esta carrera consolidada no les ha dejado ajenos a la crisis. Los descensos del consumo provocados por la crisis ha tenido como consecuencia una fuerte disminucin de pedidos que obligar a adaptar la produccin y reducir la mano de obra durante este ao 2009. Esta compaa lleg a facturar el ao pasado ms de 2.520 millones de euros
LaEstructura cristalinaes la formaslidade cmo se ordenan y empaquetan lostomos,molculas, oiones. Estos son empaquetados de manera ordenada y con patrones de repeticin que se extienden en las tres dimensiones del espacio. La cristalografaes el estudio cientfico de los cristales y su formacin.El estado cristalino de lamateriaes el de mayor orden, es decir, donde las correlaciones internas son mayores. Esto se refleja en sus propiedades antrpicas y discontinuas. Suelen aparecer como entidades puras,homogneasy con formas geomtricas definidas (hbito) cuando estn bien formados. No obstante, su morfologa externa no es suficiente para evaluar la denominadacristalinidadde un material
Tipos De Cristales:
CRISTALES SOLIDOS:Aparte del vidrio y las sustancias amorfas, cuya estructura no aparece ordenada sino corrida, toda la materia slida se encuentra en estado cristalino. En general, se presenta en forma de agregado de pequeos cristales (o poli cristalinos) como en el hielo, las rocas muy duras, los ladrillos, el hormign, los plsticos, los metales muy proporcionales, los huesos, etc., o mal cristalizados como las fibras de madera corridas.Tambin pueden constituir cristales nicos de dimensiones minsculas como el azcar o la sal, las piedras preciosas y la mayora de losminerales, de los cuales algunos se utilizan en tecnologa moderna por sus sofisticadas aplicaciones, como elcuarzode lososciladoreso lossemiconductoresde los dispositivos electrnicos.
CRISTALES LUMINOSOS:Algunos lquidos anistropos, denominados a veces "cristales lquidos", han de considerarse en realidad comocuerpos mesomorfos, es decir, estados de la materia intermedios entre el estadoamorfoy el estado cristalino.Los cristales lquidos se usan en pantallas (displays) de aparatos electrnicos. Su diseo ms corriente consta de dos lminas de vidrio metalizado que emparedan una fina pelcula de sustancia mesomorfa. La aplicacin de una tensin elctrica a la pelcula provoca una intensa turbulencia que comporta una difusin local de la luz, con la cual la zona cargada se vuelveopaca. Al desaparecer la excitacin, el cristal lquido recupera sutransparencia.Las propiedades de los cristales, como su punto de fusin, densidad y dureza estn determinadas por el tipo de fuerzas que mantienen unidas a las partculas. Se clasifican en: inico, covalente, molecular o metlico.
CRISTALES INICOS:Los cristales inicos tienen dos caractersticas importantes: estn formados de enlaces cargados y los aniones y cationes suelen ser de distinto tamao. Son duros y a la vez quebradizos. La fuerza que los mantiene unidos es electrosttica. Ejemplos: KCl, CsCl, ZnS y CF2. La mayora de los cristales inicos tienen puntos de fusin altos, lo cual refleja la gran fuerza de cohesin que mantiene juntos a los iones. Su estabilidad depende en parte de su energa reticular; cuanto mayor sea esta energa, ms estable ser el compuesto.
CRISTALES COVALENTES:Los tomos de los cristales covalentes se mantienen unidos en una red tridimensional nicamente por enlaces covalentes. El grafito y el diamante, altropos del carbono, son buenos ejemplos. Debido a sus enlaces covalentes fuertes en tres dimensiones, el diamante presenta una dureza particular y un elevado punto de fusin. El cuarzo es otro ejemplo de cristal covalente. La distribucin de los tomos de silicio en el cuarzo es semejante a la del carbono en el diamante, pero en el cuarzo hay un tomo de oxgeno entre cada par de tomos de silicio.
CRISTALES MOLECULARES:En un cristal molecular, los puntos reticulares estn ocupados por molculas que se mantienen unidas porfuerzas de van der Waalsy/o de enlaces de hidrgeno. El dixido de azufre (SO2) slido es un ejemplo de un cristal molecular al igual que los cristales de I2, P4y S8. Con excepcin del hielo, los cristales moleculares suelen empaquetarse tan juntos como su forma y tamao lo permitan. Debido a que las fuerzas de van der Waals y los enlaces de hidrgeno son ms dbiles que los enlaces inicos o covalentes, los cristales moleculares suelen ser quebradizos y la mayora funden a temperaturas menores de 100C.
CRISTALES METALICOS:La estructura de los cristales metlicos es ms simple porque cada punto reticular del cristal est ocupado por un tomo del mismo metal. Los cristales metlicos por lo regular tienen una estructura cbica centrada en el cuerpo o en las caras; tambin pueden ser hexagonales de empaquetamiento compacto, por lo que suelen ser muy densos. Sus propiedades varan de acuerdo a la especie y van desde blandos a duros y de puntos de fusin bajos a altos, pero todos en general son buenos conductores de calor y electricidad.
Simetra De Los Cristales:La clasificacin principal de los cristales se efecta con arreglo a susimetra. Un objeto tiene simetra si puede efectuarse con l alguna operacin tal que lo deje idntico a s mismo.Solamente algunos elementos de simetra se presentan en los cristales. Estos elementos son: centro de simetra, ejes secundarios, ejes ternarios, ejes cuaternarios, ejes senarios, ejes de inversin cuaternarios, ejes de inversin senarios y plano de simetra. Un cristal es invariante con relacin a un eje de ordenQ, si el conjunto de las propiedades del cristal son las mismas a lo largo de dos direcciones, que se deducen una de otra por una rotacin de unngulo2N/Qradianes en torno a ese eje. Por lo que, como consecuencia de su triple periodicidad, se demuestra que el medio cristalino slo puede poseer ejes de orden 2, 3,4 6; los ejes de simetra quinarios no se encuentran en los cristales, porque el ngulo del
pentgono, 108, no es divisor de 360.
Sistemas Cristalinos:Si se tienen en cuenta los elementos de simetra, se pueden distinguirsiete sistemas cristalinos, que toman el nombre de una figura geomtrica elemental. Como son:1. Cbico (cubo)2. Tetragonal (prismarecto cuadrangular)3. Ortorrmbico (prisma recto de basermbica)4. Monoclnico (prisma oblicuo de base rmbica)5. Triclnico (paraleleppedocualquiera)6. Rombodrico (paraleleppedo cuyas caras son rombos)7. Hexagonal (prisma recto de base hexagonal)Las diversas formas de un mismo cristal pueden proceder dedislocaciones, por los vrtices o por las aristas, de la forma tpica. Estas modificaciones se pueden interpretar a partir del conocimiento de la estructura reticular de un cristal.El conjunto de caras externas que limita un cristal constituye una forma cristalina. Estas caras se deducen unas de otras por accin de las operaciones de simetra del cristal.
CUARZO INCOLORO
Estructura de un cristal decloruro de sodio , un tpico ejemplo de un compuesto inico.las esferas prpuras son cationes desodio y las esferas verdes sananiones de cloruro.
Estructura de diamante.
ESTRUCTURA Si nos fijamos con detenimiento, en estos grficos existe siempre una fraccin de los mismos que se repite. Asimismo, loscristales,tomos, ionesomolculasse empaquetan y dan lugar a motivos que se repiten del orden de 1Angstrom= 10-8cm; a esta repetitividad, entres dimensiones, la denominamosred cristalina El conjunto que se repite, portranslacin ordenada, genera toda la red (todo el cristal) y la denominamos unidad elemental ocelda unida.
DIFERENCIA ENTRE VIDRIOS Y CRISTALES : En ocasiones la repetitividad se rompe o no es exacta, y esto diferencia losvidriosy loscristales, los vidrios generalmente se denominan materiales amorfos (desordenados o poco ordenados).No obstante, lamateriano es totalmente ordenada o desordenada (cristalinaono cristalina) y nos encontramos una graduacin continua del orden en que est organizada esta materia (grados de cristalinidad), en donde los extremos seran materiales con estructura atmica perfectamente ordenada (cristalinos) y completamente desordenada (amorfos).
ESTRUCTURA CRISTALINA ORDENADA:
En la estructura cristalina (ordenada) de loscompuestos inorgnicos, los elementos que se repiten sontomosoionesenlazados entre s, de manera que generalmente no se distinguen unidades aisladas; estos enlaces proporcionan la estabilidad y dureza del material. En loscompuestos orgnicosse distinguen claramente unidades moleculares aisladas, caracterizadas por uniones atmicas muy dbiles, dentro delcristal. Son materiales ms blandos e inestables que los inorgnicos.
ESTRUCTURAS CRISTALINAS DE LOS SOLIDOSREDES CRISTALINASLa red cristalina est formada por iones de signo opuesto, de manera que cada uno crea a su alrededor un campo elctrico que posibilita que estn rodeados de iones contrarios. Los slidos cristalinos mantienen sus iones prcticamente en contacto mutuo, lo que explica que sean prcticamente incompresibles. Adems, estos iones no pueden moverse libremente, sino que se hallan dispuestos en posiciones fijas distribuidas desordenadamente en el espacio formando retculos cristalinos o redes espaciales. Los cristalgrafos clasifican los retculos cristalinos en siete tipos de poliedros llama sistemas cristalogrficos. En cada uno de ellos los iones pueden ocupar los vrtices, los centros de las caras o el centro del cuerpo de dichos poliedros. El ms sencillo de stos recibe el nombre de celdilla unidad. Uno de los parmetros bsicos de todo cristal es el llamado ndice de coordinacin que podemos definir como el nmero de iones de un signo que rodean a un ion de signo opuesto. Podrn existir, segn los casos, ndices diferentes para el catin y para el anin. El ndice de coordinacin, as como el tipo de estructura geomtrica en que cristalice un compuesto inico dependen de dos factores: Tamao de los iones. El valor del radio de los iones marcar las distancias de equilibrio a que stos se situarn entre s por simple cuestin de cabida en el espacio de la red. Carga de los iones. Se agruparn los iones en la red de forma que se mantenga la electro neutralidad del cristal.El nmero de iones existentes en la red cristalina es indefinido, de manera que la frmula con que caracterizamos una sustancia inica slo indica la cantidad relativa (proporcin) de iones de uno u otro signo que deben existir en el cristal para mantener la neutralidad elctrica.1Podemos agrupar la mayor parte de los compuestos inicos en una serie de estructuras:
Redndice de coordinacinCompuesto
Cbica centrada en el cuerpo8CsCl, CsBr, Csl
Cbica centrada en las caras6NaCl, NaBr, Nal, MgO, CaO
Tetradrica4ZnS, BeO, BeS
Tipo fluoritaCatin = 8Anin = 4CaF2, SrF2, BaCl2
Tipo rutiloCatin = 6Anin = 3TiO2, SnO2, PbO2
La mayor parte de los slidos de la naturaleza son cristalinos lo que significa que los tomos, molculas o iones que los forman se disponen ordenados geomtricamente en el espacio. Esta estructura ordenada no se aprecia en muchos casos a simple vista porque estn formados por un conjunto de microcristales orientados de diferentes maneras formando una estructura policristalina, aparentemente amorfa.Este "orden" se opone al desorden que se manifiesta en los gases o lquidos. Cuando un mineral no presenta estructura cristalina se denomina amorfo.La cristalografa es la ciencia que estudia las formas y propiedades fisicoqumicas de la materia en estado cristalino.Las redes cristalinas se caracterizan fundamentalmente por un orden o periodicidad. La estructura interna de los cristales viene representada por la llamada celdilla unidad que se repite una y otra vez en las tres direcciones del espacio. El tamao de esta celdilla viene determinado por la longitud de sus tres aristas (a, b, c), y la forma por el valor de los ngulos entre dichas aristas (,,).El conjunto de elementos de simetra de un objeto que pasan por un punto, definen la simetra total del objeto (grupo puntual de simetra). Hay muchos grupos puntuales, pero en los cristales stos han de ser compatibles con la periodicidad (repetitividad por traslacin) por lo que hay slo 32 posibles grupos puntuales que se denominan clases cristalinas.Combinando las dos traslaciones y el ngulo que forman entre s, slo hay cinco posibles formaciones de redes planas: paralelogramo, rectngulo, cuadrado, hexgono y rombo.Si formamos una red espacial apilando estas redes planas, slo existen catorce posibles formaciones que representan las formas ms sencillas en que puede descomponerse la materia cristalina sin que por ello pierdan sus propiedades originales, son las llamadas redes de Bravais.Los cristales presentan formas ms o menos regulares con definicin de aristas, caras y vrtices. Internamente, estn constituidos por partculas que guardan entre s relaciones y distancias fijas; estos parmetros internos se estudian mediante rayos X, mientras que los externos se realizan midiendo los ngulos que forman sus caras.2
Sistemas cristalinosSe establece la clasificacin de los sistemas cristalinos de acuerdo con las celdas unitarias. La magnitud y la forma de la celda unitaria se determinan por las longitudes de las 3 aristas (a, b, c) y por los ngulos (, , ) que se forman entre stos ejes. 7
Los cristales que se encuentran en la naturaleza pueden agruparse en 7 sistemas diferentes. A su vez, en algunos sistemas es posible deducir otras formas de distribucn de tomos, molculas o iones; en total se deducen 14 redes de bravais.Siete sistemas cristalinos:SISTEMASCelda unitariaEJEMPLOS
LONGITUDESNGULOS
Cbico
Tetragonal
Ortorrmbico
Monoclnico
Rombodrico
Hexagonal
Triclnico
Catorce redes de Bravais1. Sistema cbico
2. 3. Sistema tetragonal
4. Sistema monoclnico
5. 6. Sistema ortorrmbico
7. 8. Sistema rombodrico
9. Sistema hexagonal
10. 11. Sistema triclnico
Utilidades:Cada cristal acta como pila energtica, desprendiendo determinadas influencias. He elegido algunas piedras que tienen caractersticas propias y pueden utilizarse en las situaciones en que se sienta la necesidad de ser apoyado.No deben llevarse como simples amuletos sino que se debe de tratar de entrar en contacto con la vibracin emitida por ellas, que as activada servir para contrarrestar la vibracin negativa por los problemas que estamos tratando de resolver, en caso de que no haya autnticos problemas en nuestra vida sino simplemente un deseo de logro, se deber provocar igualmente el mecanismo de contacto con la vibracin emitida por la piedra.
Veamos a continuacin las piedras y su significado: Cuarzo verde: salud Cuarzo rosado: amor, estimula la creatividad Cuarzo gris: mejora la salud emocional, eleva la autoestima. Cuarzo nevado: refuerza el sistema inmunolgico. Cuarzo cristal: claridad mental, iluminacin, fuerza, proteccin. Jade: dinero y trabajo. gata: protege contra accidentes, suerte en los negocios. Ojo de tigre: buena suerte, atrae el dinero, potencia el tercer ojo. Hematites: protege contra las malas influencias. Amatista: paz, equilibrio, transmutadora de las energas negativas. Jaspe rojo: energa, vitalidad, suerte, pudor, y sexo. Obsidiano: contra la envidia, aleja pensamientos negativos. Aguamarina: equilibrio, piedra de la juventud, esperanza y buena salud. Lapiz Lazuli: salud y armona en el hogar. palo: eleva al ser a los mas altos valores espirituales Onix negro: proteccin total. Turquesa: posee poderes curativos, sinnimo de buena fortuna. Malaquita: poder y fuerza. Aventurina: para disipar situaciones negativas, estabiliza sistema nervioso. Berilio: refuerza la vida espiritual y la esperanza. Calcedonia: protege en los viajes, alejando las desgracias y las enfermedades. Carbunclo: da decisin, energa, confianza en uno mismo, y bienestar fsico. Coral: protege de las enfermedades, propicia el afecto y la entrega. Corindn: aumenta la firmeza espiritual. Cornalina: favorece las amistades y el coraje. Crisolito: da sabidura y prudencia. Diamante: propicia para la fidelidad, la sinceridad, los afectos y la cordialidad. Esmeralda: ayuda a revelar el futuro, da constancia en el amor y fidelidad. Granate: energa, entrega, simpata.
Paneles fotovoltaicos:Un panel fotovoltaico constade un cristal de slice que, al ser estimulado por un fotn,es capaz de desprender electrones(efecto fotoelctrico)que son recogidos por un material conductor.La fabricacin de paneles fotovoltaicos tiene la necesidadde obtencin de cristales planos, a un bajo coste.Actividad 11b
(Contiene pelcula Flash)
Cristales lquidos:Los cristales lquidos constan de un fluido compuesto por molculas alargadas que tienen la propiedad de ordenarse como un cristal ante la polarizacin elctrica del medio. Al ordenarse cambian sus propiedades pticas (color, opacidad, etc). Se han utilizado intensamente en las pantallas de pequeos aparatos electrnicos (calculadoras, relojes) y actualmente se estn introduciendo en el mercado de los monitores (pantalla plana).
Cristales artificiales.La necesidad de cristales abrasivos en la industria y el alto coste de los naturales (por ejemplo, los diamantes industriales) ha posibilitado la aparicin de artificiales. Estos cristales no alcanzan los resultados delos naturales, pero su menor coste rentabiliza su obtencin y uso.
Estas tcnicas tambin se han adentrado en el mundo dela joyera, obtenindose gran variedad de piedras preciosas artificiales con colores escasos en las naturales.
Informtica:Un chip consta de distintas capas de materiales crecidos durante el proceso de fabricacin:metal, xido y semiconductor cristalino (slice) que, alrecibir un impulso elctrico, puede transmitirlo o no aun material conductor. Las tcnicas de cristalizacinhan permitido reducirlos a tamaos tan insospechadosque la limitacin consiste en conseguir reducir al mismo tamao sus conexiones.
Universidad Nacional Jos Faustino Snchez Carrin