Gas Perfecto
-
Upload
denisronald -
Category
Documents
-
view
278 -
download
1
description
Transcript of Gas Perfecto
Comportamiento
de un fluido
líquido y un gas
T1 T2
T1>>T2
Comente e
identifique que
tipo de fluidos es
cada uno
• ¿A qué se denomina un gas perfecto?
• ¿Qué propiedades y características tiene un gas perfecto?
• ¿Cuáles son las leyes de un gas ideal?
• ¿Cómo se comporta un gas a condiciones normales
LOGRO DE APRENDIZAJE
• Al término de la sesión, el estudiante resuelve
ejercicios, relacionado con el comportamiento de gases
ideales como fluidos, teniendo en cuenta sus leyes y
comportamiento a efectos de su temperatura y presión;
con orden, fundamento teórico, claridad y precisión.
GAS PERFECTO
• Las relaciones termodinámicas y los flujos de fluidos compresibles se
limitan al los gases prefectos (o ideales), los cuales satisfacen la siguiente
ley:
TRvp s
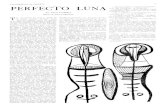
• En el proceso de condensación mostrado en la figura, el gas está a una temperatura
menor a la temperatura critica (está en forma de vapor). Si se aplica presión (se
disminuye el volumen) paulatinamente, el vapor pasa al estado liquido (se
condensa). Esto es el resultado de la cercanía de las moléculas y la manifestación
de las fuerzas de cohesión para formar una nueva fase (líquida).
(a) (b) (c) (d)
• fluido ideal: carece de fricción y es incompresible
• gas perfecto: tiene viscosidad (desarrolla esfuerzos de corte) y es
compresible
• La ecuación se puede escribir:
• y R tiene unidades de
RTp
KKg
Nm
KKg
m
m
NR
º
1:
3
2
• Ley de CHARLES: p = cte, V del gas depende solo de T
• Ley de BOYLE: T = cte, V del gas depende solo de p
• haciendo el análisis a nivel molecular e introduciendo la ley de
AVOGADRO (volúmenes iguales de gases a la misma T y p absolutas
tienen el mismo número de moléculas, por lo tanto, sus masas son
proporcionales a los pesos moleculares) resulta el producto MR llamado
cte. universal de los gases.
• M: peso molecular
KmolKg
NmMR 8312
KKg
Nm
MR
8312
• Calor específico cv: es el número de unidades de calor agregadas por
unidad de masa para aumentar la temperatura 1 grado cuando V es cte.
• Calor específico cp: es el número de unidades de calor agregadas por
unidad de masa para aumentar la temperatura 1 grado cuando p es cte.
• k es la relación de calores específicos
• R se relaciona con cv y cp mediante la forma
v
p
c
ck
Rcc vp
LEYES DE LOS GASES
• Ley de Boyle-Mariotte (a “T” constante).
p · V = constante; p1 · V1 = p2 · V2
• Ley de Charles Gay-Lussac (a “p” constante).
• V V1 V2
— = constante ; —— = ——
T T1 T2
ECUACIÓN GENERAL DE LOS GASES IDEALES.
• Igualmente puede demostrarse que a V constante:
P— = constante ; T
• Con lo que uniendo las tres fórmulas queda:
• P · V——— = constante ;
T
12
ECUACIÓN GENERAL DE LOS GASES IDEALES.
• La constante depende de la cantidad de gas.
Para 1 mol Para “n” moles
• P · V P · V——— = R ; ——— = n · R
T T
• que suele escribirse de la siguiente forma:
p ·V = n ·R ·T
• R = 0’082 atm·l/mol·K = 8’31 J/mol·K
CONDICIONES NORMALES
• Se denominan condiciones normales (C.N.) a las siguientes
condiciones de presión y temperatura:
• P = 1 atmósfera
• T = 0 ºC = 273 K
Ejemplo: A la presión de 3 atm y 20 ºc, una cierta masa gaseosa
ocupa un volumen de 30 litros. Calcula el volumen que ocuparía
en condiciones normales.
Ejercicio: calcula la masa molecular de un gas, sabiendo que
32,7 g del mismo ocupan a 50ºc y 3040 mm de hg de presión un
volumen de 6765 ml
17
TEORÍA CINÉTICA DE LOS GASES (POSTULADOS).
• Los gases están formados por partículas separadas enormemente en
comparación a su tamaño. El volumen de las partículas del gas es
despreciable frente al volumen del recipiente.
• Las partículas están en movimiento continuo y desordenado chocando
entre sí y con las paredes del recipiente, lo cual produce la presión.
• Los choques son perfectamente elásticos, es decir, en ellos no se pierde
energía (cinética).
• La energía cinética media es directamente proporcional a la temperatura.
¿Qué aprendimos en la clase de
hoy?
¿Para que servirá lo aprendido en la
carrera de Ingeniería de Minas?