GESTION DE LABORATORIO -...
Transcript of GESTION DE LABORATORIO -...

GESTION DE
LABORATORIO
Bioqca. Samantha Cardozo
Especialista en Docencia Universitaria
Especialista en Ingeniería en Calidad

TEMA 4.
DOCUMENTACION DEL
SISTEMA DE CALIDAD.
MANUAL DE CALIDAD
MANUAL DE PROCEDIMIENTOS
INSTRUCCIONES OPERATIVAS
REGISTROS E INFORMES

- Conocer la estructura de la documentación de un Sistema de Gestión de
Calidad (SGC)
-Suministrar herramientas para la confección de documentos del SGC.
-Identificar los puntos mínimos que deben constar en un Manual de
Calidad
- Reflexionar sobre la importancia de la documentación y su utilidad.
OBJETIVOS

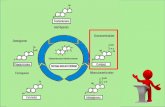
ETAPAS DE LA IMPLEMENTACIÓN DE UN
SGC.
Revisión y Control de los
procesos y documentos.
Acciones correctivas
Nombrar un Responsable
de Calidad. Formar un
equipo interno
Identificación del proyecto. Evaluar
documentación disponible
Compromiso de la dirección
Implementar
Capacitar al personal. Redactar Documentos
Identificar procesos.
Redactar el MC. Redactar la Política de
la Calidad. Definir objetivos
Revisión por la Dirección.
Definición de nuevos objetivos
MEJORA
CONTINUA

Si se documenta, debe hacerse.
Si se hace, debe documentarse.
Lo que no está documentado,
jamás se ha hecho.

Un documento es una información materializada en diferentes
tipos de medios impresos o electrónicos, donde se describe, se
prueba, se establece o se hace constar algo.
En un laboratorio, existen documentos procedentes de:
•Fuentes externas
•Fuentes internas

Qué debe
hacerse
Cómo sucede
Cómo debe hacerse
Cómo se hizo
NIVELES DE DOCUMENTACIÓN DEL SISTEMA DE CALIDAD
Procesos generales
Formularios y registros

• Cumplir con las especificaciones de un producto o servicio. La
documentación prueba que las cosas se hicieron de la forma estipulada.
• Asegurar la reproducibilidad de los resultados.
• Facilitar el entrenamiento.
• Cumplir con los requisitos legales exigidos por la autoridad sanitaria y
con las normas vigentes.
• Rastrear o reconstruir el proceso.
• Asegurar la “trazabilidad” de los procesos y productos a través de los
registros históricos.
En caso de presentarse un problema, la documentación permite
rehacer el proceso, identificar dónde ocurrió el error y corregirlo.
RAZONES PRINCIPALES PARA DOCUMENTAR

ETAPAS DE PREPARACIÓN DE UN
DOCUMENTO.
OBTENCION DE LA INFORMACION PRIMARIA
REDACCIÓN
REVISIÓN
APROBACIÓN
EDICIÓN
EMISIÓN
DIVULGACIÓN
ENTRENAMIENTO
APLICACIÓN
EVALUACIÓN

“Es el documento donde se presenta: • La estructura organizativa del laboratorio, • sus principales objetivos respecto al gerenciamiento de la calidad y • las responsabilidades más importantes de cada uno de los niveles de la organización” MA2 - FBA
MANUAL DE
CALIDAD
“El documento que especifica el sistema de gestión de la calidad de una organización”. ISO 9001:2008 apartado 3.7.4
Nivel 1

MANUAL DE
CALIDAD
Tamaño y complejidad
Formato
Utilidad
Responsable
Comunicar y presentar. Describir e implementar un sistema de la calidad eficaz. Controlar y facilitar las actividades de aseguramiento.
Suministrar las bases documentales para las auditorias. Formar al personal en los requisitos del SGC.
Demostrar que el sistema de la calidad cumple con los requisitos de la calidad exigidos en situaciones contractuales.

ESTRUCTURA DEL MANUAL DE
CALIDAD. Puntos mínimos.
MANUAL DE
CALIDAD
CARATULA
Misión - Visión
Introducción
Alcance
Norma de referencia
Lista de distribución
Control
de cambios
Índice
POLÍTICA Y
OBJETIVOS
Compromiso
de la Dirección

ESTRUCTURA MANUAL DE
CALIDAD
Carátula
Encabezado de página
HOSPITAL….
Servicio de Laboratorio MANUAL DE CALIDAD
Código del documento: SL.MC
N° de Versión: 0 Página 2
de 35 Fecha: 25 /06 /11
Página 2 de 35
Apellido y Nombre FIRMA FECHA
ELABORADO POR
REVISADO POR
APROBADO POR
Pie de página

ESTRUCTURA MANUAL DE
CALIDAD 1. LISTA DE DISTRIBUCIÓN
COPIA RESPONSABLE SECCIÓN FECHA FIRMA
1. CONTROL DE CAMBIOS
N° de Versión MODIFICACIÓN FECHA DE APROBACIÓN
FECHA DE IMPLEMENTACIÓN
FIRMA DEL RESPONSABLE DE CALIDAD
0 Primer ejemplar 30/09/10 4/10/10
(Se modifica de tal pág a tal pág)

POLÍTICA DE CALIDAD
• Documento que expresa la orientación y propósitos
generales del organismo concernientes a la calidad,
expresados formalmente por el más alto nivel de dirección.
• Misión del laboratorio: ¿Qué somos? ¿Qué hacemos?
Visión: ¿Qué proyección tenemos?
• La política debe contemplar los siguientes aspectos:
– Que servicio brinda el laboratorio
– Cuál es el propósito del sistema
– Compromiso de defenderla, comunicarla e implementarla
– Compromisos con las buenas prácticas de laboratorio
– Compromiso de la dirección de cumplir con la norma

El Laboratorio Biomédico Dr. Rapela en la búsqueda de la satisfacción a los clientes y la
excelencia de los servicios que presta, asume como objetivo desarrollar en todos los
niveles de su Organización, un Sistema de Gestión que se mantenga a lo largo del tiempo,
promoviendo una mejora continua, bajo el lema
"ser hoy mejores que ayer y mañana mejores que hoy" .
Para cumplimentar la Política de Calidad la Dirección del Laboratorio Biomédico Dr.
RAPELA a establecido los siguientes objetivos :
Cliente
Considerar a nuestros Clientes como lo mas importante, orientando los esfuerzos para
que reciba el mejor servicio, dando siempre algo mas de lo esperado.
Calidad
Establecer y mantener un Sistema de Gestión de Calidad que cumpla con los
requerimiento de las Normas ISO 9001, ISO 17025 e ISO 15189.
Servicio
Como resultado final de nuestros esfuerzos, poner a disposición de nuestros Clientes los
servicios de Análisis Clínicos, Toxicológicos, Bromatológicos, de Medicamentos,
Veterinarios y de Medio Ambiente realizados con la más alta calidad y que a través de una
comunicación fluida sea percibido como de excelencia.
EJ.: LABORATORIO BIOMÉDICO DR. RAPELA
ISO 9001:2008
ALAC – Asociación de Laboratorios de Alta Complejidad
Fundación Bioquímica Argentina
Acreditado por el OAA Norma NM-ISO 15189: 2008. (El alcance
de la acreditacion está descripto en el F01-(DC-LM-01).

Liderazgo
Alcanzar una posición de liderazgo en el mercado del
Servicio Analítico Integral.
Equipamiento
Contar con equipamiento de ultima generación, con una actualización permanente de las
herramientas técnicas e informática.
Personal
Establecer las pautas que permitan al personal la capacitación permanente, motivando la
actitud positiva, el rendimiento y la participación para asumir nuevos emprendimientos,
además de la optimización de los presentes, manteniendo en todos sus actos:
La Honestidad y sinceridad en los resultados.
El Método y el Espíritu de observación en las distintas operaciones.
El Compromiso de familiarizarse con la documentación del sistema.
La Obligación de implementar las políticas y los procedimientos en su trabajo
Para todo ello la Dirección del Laboratorio Biomédico Dr. RAPELA se compromete a
desarrollar y mantener un Sistema de Gestión, cumpliendo y haciendo cumplir las
buenas prácticas profesionales y los procedimientos que permitan alcanzar la efectiva
implementación del mismo.
Dr. Juan Carlos Rapela
DIRECCION
Fecha de Vigencia: 30 de Julio de 2007
Fuente: http://www.rapela.com.ar/politica-de-calidad/

MANUAL DE
CALIDAD
DESCRIPCIÓN
DEL LABORATORIO
DERIVACIÓN
DE MUESTRAS
EQUIPOS
ESTRUCTURA ORGANIZATIVA
Y ADMINISTRATIVA
DESCRIPCIÓN
DE FUNCIONES
Documentación
IDENTIFICACIÓN DE SIGNATARIOS
REFERENCIA A PROCEDIMIENTOS
CAMPOS Y
ACTIVIDADES
ESTRUCTURA DEL MANUAL DE
CALIDAD

ORGANIGRAMA
Director Técnico
Medio
Interno
Química
Clínica
Bacteriología
y Micología
Hematología
y
Hemostasia
Orinas
y
Fecales
Inmunología Mantenim. Administrac. Limpieza
Responsable
de Calidad
Urgencias
1 B 1 B 5 B
1 T
2 B
1 T 1 B 1 B 1 T 3 A 2 M
4 B
3 T
(Rotativo)
B: Bioqca/o
T: Tca/o
A: Administrativa/o
JH: Jefa de Hogar

MANUAL DE
CALIDAD
ESTRUCTURA DEL MANUAL DE
CALIDAD
Gestión de servicios,
instrumentos,
reactivos y fungibles
Validación de
resultados
(analítica y
fisiopatológica)
Servicio al cliente
Gestión de reclamos
Aseguramiento
de la calidad
Capacitación
del personal
Bioseguridad

G) Capacitación del personal
En un sistema de calidad se debe asegurar
que los procesos y procedimientos
serán ejecutados de una manera
normalizada y predecible.
Transforma las buenas intenciones del personal en
buenos resultados.
Capacitación continua: Mayor competencia de los
empleados, mejores prácticas, disminución en
las variaciones de los procesos, mayor calidad
de los productos y servicios.
Beneficios
Las inversiones en capacitación y promoción del personal deben formar parte de las decisiones estratégicas de la dirección.

MANUAL DE
CALIDAD
ESTRUCTURA DEL MANUAL DE
CALIDAD
Acciones correctivas
Auditorías
internas
Anexos
Acciones
preventivas
Referencia
Revisión de
la Dirección
Control del trabajo
de ensayo
y/o calibración
no conforme

Exactitud y
adecuación
Proceso de aprobación,
emisión y control
del MC
Distribución
del MC
PROCESO DE
ELABORACIÓN
DEL MC
Incorporación
de cambios
Uso de referencias
Designar
Responsable
Revisión y
aprobación final
Control de emisión
Y de los cambios
Copias
no controldas

Los procesos se describen como una secuencia de equipos, personal y
procedimientos desarrollados en un medio ambiente adecuado y que permiten
transformar muestras (entrada) en un resultado final o una información (salida),
creando un valor agregado para el usuario.
Nivel 2: LOS PROCESOS

PROCESOS ESTRATÉGICOS
* GESTIÓN DE
RECLAMOS
* CONTRATOS Y
CONVENIOS
* REVISIÓN POR LA
DIRECCIÓN
* PLANIFICACIÓN DEL
SISTEMA DE CALIDAD
* AUDITORIAS
INTERNAS
* CONTROL DE
DOCUMENTOS

PROCESOS OPERATIVOS
* ELABORACIÓN DEL INFORME
* CONSERVACIÓN Y
TRANSPORTE DE
MUESTRAS
* OBTENCIÓN DE MUESTRAS
* PROCESOS
ANALÍTICOS
* VALIDACIÓN DE LOS
MÉTODOS

PROCESOS DE APOYO
* SISTEMA DE
INFORMACIÓN * LIMPIEZA Y
ACONDICIONAMIENTO DEL
MATERIAL
* GESTIÓN Y
MANTENIMIENTO
DE EQUIPOS
* COMPRAS Y EVALUACIÓN
DE PROVEEDORES
* GESTIÓN DE
PERSONAL

(Disponible en http://www.interlab.com.ec)


Los procedimientos son documentos que proporcionan las
instrucciones necesarias para la correcta ejecución de las actividades
administrativas o técnicas. En general se puede decir que un
procedimiento establece cómo debe hacerse en el sentido amplio:
Nivel 3: PROCEDIMIENTOS
OPERATIVOS ESTÁNDAR (POE)
¿Qué se debe hacer?
¿Cuándo?
¿Cómo y dónde se hará?
¿Quién debe hacerlo?

Las Normas ISO 9000 definen un procedimiento como
“Forma especificada para llevar a cabo una actividad o
un proceso". En otras palabras…
es la descripción precisa, concisa y clara del material,
equipo, condiciones, actividades y requerimientos para
obtener un producto o un servicio de una calidad
definida.
Nivel 3: PROCEDIMIENTOS
OPERATIVOS ESTÁNDAR (POE)

MODELO DE UN POE

NIVEL 4: FORMULARIOS Y REGISTROS
Los formularios y registros son documentos creados para tener una evidencia de
las actividades efectuadas, de sus controles y de sus resultados.
Los FORMULARIOS son documentos con espacios en blanco, que una vez
llenados se transforman en registros.
Deben ser completados en el mismo momento en que se realiza la actividad,
anotando en ellos, clara y sistemáticamente toda la información pertinente.
Aunque es común que estos datos se archiven en papel, cada vez más se están
utilizando archivos electrónicos de computadora.
Es muy importante recalcar que en un sistema de calidad,
lo que no ha sido registrado, no se ha hecho, no existe.
Gran parte del trabajo de las auditorias internas y externas consiste
precisamente en comprobar el funcionamiento del sistema de registro.

Formularios
Su función es permitir el registro de las actividades y sus resultados al
ejecutar un proceso o un POE, por lo tanto deben incluir espacios en
blanco (campos) para registrar la información obtenida.
Por su parte, los procesos y POEs tienen que hacer referencia al – y
adjuntar el – formulario pertinente, el cual debe contener los siguientes
campos:
Identificación (organización, numeración, paginado y fecha);
Título;
Autoría,
Aprobación y actualizaciones con sus respectivas fechas;
Identificación de cambios,
Localización.
NIVEL 4: FORMULARIOS Y REGISTROS

NIVEL 4: FORMULARIOS Y REGISTROS Los REGISTROS son documentos que proporcionan evidencias objetivas de
actividades realizadas o resultados obtenidos.
Se caracterizan porque:
a) son consecuencia inmediata de ejecutar un procedimiento y documentar sus
resultados;
b) proporcionan la evidencia necesaria para establecer si la actividad o la tarea se
adecuó al procedimiento correspondiente;
c) no están sujetos a actualización porque no deben ser modificados (salvo en
casos
especiales y dejando constancia de todas las circunstancias del cambio, siguiendo
los procedimientos al respecto).
Los registros pueden realizarse en medios impresos o electrónicos, y estar en
formato analógico o digital.
El laboratorio debe garantizar que los registros no puedan ser modificados o que,
si lo son, quede constancia de ello y de quién y cuándo lo hizo, especialmente
cuando sean más susceptibles a la modificación, como en el caso de los
guardados en formato digital.

NIVEL 4: FORMULARIOS Y REGISTROS
Un registro apropiado debe ser:
• Veraz (describe lo que efectivamente sucedió).
• Exacto (lleva doble verificación).
• Permanente (no usa lápiz ni tinta lavable).
• Oportuno (se realiza en tiempo real).
• Claro (entendible para todos).
• Coherente (en lo que hace a fechas, temperaturas, pesos,
tiempos, etc.).
• Legible.
• No alterable (no usar corrector ni borrador).
• Completo (no deja espacios en blanco, cruzar con una
raya lo que no se llena).




CAMBIOS A LOS DOCUMENTOS
Los documentos sólo deben modificarse mediante un proceso determinado,
tanto para redactar los nuevos documentos y revisar los existentes, como para
actualizar el índice maestro y distribuir –y archivar– los documentos controlados.
Este proceso a su vez requiere de un POE DE CONTROL DE CAMBIOS que
defina los tipos de cambios, las responsabilidades y capacitación de personal
necesarios, y garantice que los usuarios sólo tengan acceso a versiones
vigentes de los documentos.
Por todo ello, se justifica la utilización de un FORMULARIO DE CONTROL DE
CAMBIOS que permita registrar:
• ¿Cuál es el cambio propuesto?
• ¿Por qué es necesario?
• ¿Quién lo solicitó?
• ¿Quién lo aprobó?
• ¿A quién y qué afecta? (POEs, personal, equipos, etc.).
• Si es de rutina o emergencia.
• La fecha de su entrada en vigencia.

Escribir lo que se
hace
Hacer lo que está
escrito
Poder demostrarlo
La documentación
Debe responder a la realidad de la
organización....
Debe proveer la información adecuada...
Debe proporcionar evidencias objetivas....
Debe ser entendida y aplicada por todos...

-“Curso de Gestión de Calidad y Buenas Prácticas de Laboratorio”. II
Edición. OPS, 2009. Módulo 3: Documentación del sistema de calidad
- “Curso de Gestión de Calidad para Servicios de Sangre”. Módulo 3:
Documentación del sistema de calidad. OPS.
- “Guía para un Manual de Sistemas de Calidad en un Laboratorio de
Prueba”. Organización Mundial de la Salud, Ginebra, 1998.
-“Curso de Gestión de Calidad para Laboratorios” Módulo 8: Gestión de No
Conformidades. OPS, 2005.
-Fernández Espina, C. y Mazziotta, D. (2005): “GESTION DE CALIDAD EN
EL LABORATORIO CLÍNICO”. COLABIOCLI. Editorial Médica
Panamericana. 1°edición. Buenos Aires. Argentina.
BIBLIOGRAFÍA