Las buenas prácticas en Inmunohematología Lo que no...
Transcript of Las buenas prácticas en Inmunohematología Lo que no...

Dra. Virginia Callao Molina
Las buenas prácticas en Inmunohematología
Lo que no debemos olvidar


Las buenas prácticas en Inmunohematología
Lo que no debemos olvidar

BUENAS PRÁCTICAS
Hacer bien la cosas
Trabajar con seguridad
Aplicar conceptos de calidad
Ser eficientes
Ser competentes

QUE SON LAS DIRECTRICES DE BUENAS PRACTICAS
O NORMAS DE CORRECTA FABRICACIÓN (GMPs)??
ASEGURAR QUE TODOS LOS PRODUCTOS SE FABRIQUEN DE FORMA UNIFORME Y CONTROLADA

Historia del las Buenas prácticas de manufactura
Históricamente las BPM surgen como una respuesta o reacción ante hechos graves (algunas veces fatales), relacionados con la falta de inocuidad, pureza y eficacia de alimentos y/o medicamentos. Los primeros antecedentes de las BPM datan de 1906 en USA y se relacionan con la aparición del libro"La Jungla" de Upton Sinclair. RELATA LAS CONDICIONES INSALUBRES DE LA INDUSTRIA CÁRNICA EN CHICAGO

GOOD MANUFACTURING PRACTICE


MARCO LEGAL / GUÍAS:
- Directiva 2005/62/CE de la C. Europea (directrices de buenas practicas)
- Consejo de Europa: Directiva 2016.1214.UE
- Real Decreto 2088/2005 y RD 905/2018
- WHO guidelines on GMP for blood establishments
- Guía consejo de Europa


In 2016 the European directive, (EU) 2016/1214 was published directing blood banks to Good Practices Guidelines (GPG). These guidelines, which are based on updated scientific and technical expertise, reinforced the importance of full traceability of blood products. Following this directive, all blood establishments, should implement these practices in their quality system. This European directive was included in the Spanish legislation in July 2018 (Royal Decree 905/2018, of July 20).
Consejo de Europa. Directiva 2016.1214.UE
TRAZABILIDAD !!!!

Good Manufacturing Practice Council of Europe
APLICAR GMPs A TODO EL PROCESO

Las buenas prácticas en Inmunohematología
Lo que no debemos olvidar

HEMATIES
Inmunohematología
Estudia los procesos inmunes que tienen lugar en el
organismo en relación con los elementos sanguíneos.

Aglutinación
Inmunohematología
Se fundamenta en reproducir “in vitro” las reacciones antígeno-
anticuerpo que se pueden producir “in vivo” .

Inmunohematología
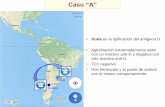
Uno de los aspectos más importantes es el estudio
de los grupos sanguíneos eritrocitarios,
fundamentales en diferentes escenarios

Seguridad receptor: evitar reacciones transfusionales
Seguridad feto y RN: evitar EHFRN Seguridad paciente: evitar rechazo
Estudio de los grupos sanguíneos
TRASPLANTE GESTACIÓN
DONACIÓN TRANSFUSIÓN

La Inmunohematología nos sirve para dar seguridad a los pacientes
Sirve para salvar vidas

SISTEMA DE GESTIÓN DE
CALIDAD
PERSONAS
PROCEDIMIENTOS
Y TÉCNICAS DE TRABAJO
PETICIONES Y
MUESTRAS
COMPONENTES
SANGUÍNEOS
SISTEMA
INFORMÁTICO
REQUISITOS PARA TRABAJAR BIEN EN INMUNOHEMATOLOGÍA
EQUIPOS Y REACTIVOS

SISTEMA DE GESTIÓN DE
CALIDAD
PERSONAS
PROCEDIMIENTOS
Y TÉCNICAS DE TRABAJO
PETICIONES Y
MUESTRAS
COMPONENTES
SANGUÍNEOS
SISTEMA
INFORMÁTICO
REQUISITOS PARA TRABAJAR BIEN EN INMUNOHEMATOLOGÍA
EQUIPOS Y REACTIVOS

NORMATIVA

GUÍAS Y ESTÁNDARES



PERSONAS

PERSONAS

Personal suficiente Cualificación Perfil de puesto de trabajo
Formación y evaluación inicial
Formación continuada
Formación en calidad y buenas prácticas
Evaluación periódica de la capacitación
PERSONAS

PROCEDIMIENTOS Y TÉCNICAS DE TRABAJO
Detallados
Comprensibles
Actualizados
Al alcance del personal

EQUIPOS

EQUIPOS
MANUAL DE EQUIPAMIENTO
FICHAS DE EQUIPOS

EQUIPOS
Equipos críticos: - Mantenimiento preventivo - Mantenimiento correctivo
Calibración periódica Instrucciones de uso
Equipos defectuosos
Proveedores autorizados

EQUIPOS

REACTIVOS

REACTIVOS
Registros de reactivos
Proveedores autorizados
Marcado CE
Certificado de conformidad
Almacenamiento y condiciones de uso
Validez: inspección visual
y caducidad

REACTIVOS
Controles diarios (anexo 2)
Control de calidad externo
Controles del fabricante correctos
Análisis de incidencias
Laboratorios de referencia

REACTIVOS

SISTEMAS DE INFORMACIÓN
Validación
Documento de seguridad
Gestión de contraseñas y
copias de seguridad
Gestión de datos de carácter personal
Trazabilidad
Formación

La transfusión

La transfusión no está exenta de riesgos
Serious Hazards of Transfusión. Annual SHOT report-2018.

Serious Hazards of Transfusión. Annual SHOT report-2018.
SEGUIR LOS PROCEDIMIENTOS!!!!
SEGUIR NORMAS GMP !!!!
ERRORES DE LABORATORIO

1.882.152 CS transfundidos en 2017
4.201 notificaciones
22,3 por 10.000 CS
INFORME ESPAÑOL DE HV


Serious Hazards of Transfusión. Annual SHOT report-2018.

La transfusión

PETICIONES DE TRANSFUSIÓN
DOCUMENTAR LA DECISIÓN DE TRANSFUSIÓN
PETICIÓN BIEN CUMPLIMENTADA

MUESTRAS PRETRANSFUSIONALES
Procedimientos
Formación del personal
Identificación activa del receptor
Identificación en la cabecera
Persona responsable

Muestra correctamente extraída e identificada
-Identificar siempre en cabecera del paciente
-Nunca en el control de enfermería
-Nunca manejar muestras sin identificar
Una muestra mal identificada puede suponer una transfusión incorrecta
VALIDEZ: 72 HORAS

Pruebas pretransfusionales
OBJETIVO: ASEGURAR LA COMPATIBILIDAD
ENTRE DONANTE Y RECEPTOR

Técnicas serológicas básicas
Técnica de tubo
Técnica de microcolumna (tarjeta)

Técnica de tubo
Manipulación del tubo:
Movimiento lento y homogéneo para despegar el botón.
RECOMENDACIONES

Técnica de tubo
Interpretación 4 +
3+
2+
1+
neg

Técnica de microcolumna
Las tarjetas son la base
de la técnica, por tanto
es imprescindible cuidar
su manipulación y
conservación

Conservación: Evitar fuentes de calor Temperatura: indicaciones de laboratorio comercial ( 4ºC – 22ºC)
Almacenamiento: Posición vertical.
Evitar contaminaciones.
Destapar pocillo a pocillo.
Consejos prácticos:
Intentar depositar en la copa lo que vamos a dispensar.
Ajustar la punta a la pipeta
Manipulación: Observar si el gel está en buen estado.
Desechar pocillos deshidratados.
Líquido en copa: Centrifugar. Rotular la tarjeta de forma vertical sin volcarla

Tarjetas: interpretación
Grados de reacción

PRUEBAS PRETRANSFUSIONALES (I)

PRUEBAS DE PRETRANSFUSIONALES (II)

Pruebas pretransfusionales
1. Pruebas en la unidad de hematíes
1. Debe confirmarse el grupo ABO de todos los
hematíes disponibles para transfusión.
2. El tipaje Rh (D) debe confirmarse, como mínimo,
en los hematíes etiquetados como Rh (D) negativo.

Rh (D): Se debe determinar utilizando anticuerpos monoclonales anti-D potentes de tipo
IgM que aglutinan directamente a los hematíes (que no reaccionen con la variante DVI )
1. En caso de resultados dudosos debe considerarse al paciente como Rh (D) negativo
2. Pruebas en el receptor (1)
Pruebas pretransfusionales
.
Grupo ABO: Los hematíes deben enfrentarse a anti-A y anti-B, y el plasma a hematíes A1 y B
1. Deben resolverse las posibles discrepancias.
2. Si la transfusión es necesaria antes de resolver la discrepancia, utilizar sólo hematíes O

Escrutinio de anticuerpos irregulares eritrocitarios:
2. Pruebas en el receptor (2)
Pruebas pretransfusionales
.
El método utilizado debe garantizar la detección de anticuerpos clínicamente significativos:
- Utilizar la prueba indirecta de la antiglobulina .
- Garantizar que las células empleadas en el escrutinio presentan los antígenos correspondientes
a la mayoría de anticuerpos clínicamente significativos, preferiblemente en forma homocigota.

Identificación de anticuerpos irregulares eritrocitarios:
2. Pruebas en el receptor (3)
Pruebas pretransfusionales
.
-Si el escrutinio es positivo se debe complementar el estudio con técnicas que
permitan la identificación de anticuerpos clínicamente significativos.

Fenotipo eritrocitario
- Siempre que tenga anticuerpos irregulares, para ayudar en la identificación.
- Cuando queramos disponer de esta información en pacientes determinados
- Evitar aloinmunización (mujeres en edad fértil, etc..).
- Facilitar la identificación mas adelante, post-transfusión.
2. Pruebas en el receptor (4)
Pruebas pretransfusionales
.

3. Pruebas de compatibilidad
Pruebas pretransfusionales
1. Si no hay presencia actual ni antecedentes de anticuerpos irregulares,
para asegurar la compatibilidad ABO se debe realizar:
• Una prueba cruzada inmediata (salina) o
• Prueba cruzada electrónica.
La compatibilidad ABO entre los c. sanguíneos que contengan hematíes y el
plasma/suero del receptor debe estar asegurada antes de la transfusión.
2. En caso de presencia de anticuerpos
irregulares en la muestra actual o en registros
históricos, debe realizarse una prueba cruzada
basada en la prueba indirecta de la antiglobulina
(prueba cruzada completa ) utilizando hematíes
carentes del antígeno diana.

SISTEMA DE GESTIÓN DE LA CALIDAD
OBJETIVOS
GESTIÓN POR PROCESOS
GESTIÓN DE LOS RIESGOS
CONTROL DOCUMENTAL
MEDICIÓN, ANÁLISIS Y MEJORA CONTÍNUA
EVALUACIÓN DE INDICADORES

No hay que olvidar……..

Debemos trabajar con un sistema de gestión de la calidad
No hay que olvidar……..
Las muestras proceden de pacientes
Las muestras deben estar bien identificadas
Las técnicas de trabajo deben estar validadas
Los reactivos y equipos deben estar validados y controlados
Se deben seguir las instrucciones del fabricante
El personal debe estar capacitado y formado
Deben existir procedimientos de trabajo y registros
Debe asegurarse la trazabilidad de los resultados
Debe existir un sistema informático validado

TRABAJA BIEN !!!
SALVA VIDAS !!!

gracias PUNTA DEL ESTE. 2016