Nomenclatura Química Inorgánica
description
Transcript of Nomenclatura Química Inorgánica

CLAVES PARA NOMBRAR Y FORMULAR
SIN EQUIVOCARSE
Nomenclatura Química Inorgánica

¿En qué orden se colocan los elementos?
Primero se escribe el símbolo del elemento menos electronegativo, que es el que se ubica más a la izquierda en la tabla , si están en el mismo grupo, es el que está más abajo.
La posición del hidrógeno varía según el elemento con el cual se combine, a la izquierda con no metales, a la derecha con metales.

¿En qué orden se colocan los elementos?
El oxígeno siempre va a la derecha, excepto con el flúor porque es mas electronegativo que el oxígeno
Si se combinan dos no metales se debe respetar el siguiente orden de electronegatividad:
B, Si, C, Sb, As, P, N, H, Te, Se, S, At, I, Br, Cl, O, F

¿Cómo se colocan los subíndices?
En los compuestos binarios (no metal o metal con oxígeno o hidrógeno) se intercambian las valencias.
El subíndice 1 no se escribeSi todos los subíndice son múltiplos se simplifican ,
excepto en los peróxidosLa suma de la multiplicación de los subíndices por
el número de oxidación en un compuesto siempre debe ser cero (excepto en los iones)

¿Qué indican los sufijos y prefijos?
Los prefijos y sufijos se utilizan con el siguiente criterio:
Dos valencias : oso (menor) ico (mayor) Tres valencias: hipo ….oso (menor), oso ico (mayor) Cuatro valencias: hipo…oso (menor), oso, ico per…..ico (mayor)
Si tiene una sola valencia se nombra como ….. de…...

¿Qué indican los sufijos y los prefijos?
En la nomenclatura sistemática pueden usarse prefijos:
mono (1), di (2) , tri (3) , tetra (4) penta (5) , hexa (6), hepta (7)
En la nomenclatura de Stock se coloca un número romano entre paréntesis, cuando el elemento tiene mas de una valencia.

Nombres particulares…
Algunos compuestos se nombran utilizando la raíz latina:
Azufre : sulfurCobre : cuprEstaño: estannHierro: ferManganeso: manganNitrogeno: nitrPlata: argentPlomo: plumb

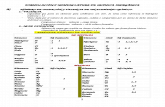
Números de Oxidación: Elementos Representativos
Grupo Número de Oxidación Excepciones
Grupo I (1): Li, Na, K, Rb, Cs, Fr
+1 Hidrógeno +1 (no metal)-1 (metal)
Grupo II (2): Be, Mg, Ca, Sr, Ba, Ra
+2
Grupo 3 (13): Al, B +1, +3 Boro +3Aluminio +3
Grupo 4 (14): C, Si +2, +4, -4 -4 combinan con hidrógeno
Grupo 5 (15): N, P, As, Sb +1, +3. +5-3
Nitrógeno +1, +2, +3, +4, +5 -3 combinan con H
Grupo 6 (16): S, Se, Te, O +2, +4, +6-2
Oxígeno -2 siempre-2 combinan con H
Grupo 7 (17): Br, Cl, F, I +1, +3, +5, +7-1
Fluor -1 siempre-1 combinan con H

Números de Oxidación: Elementos de Transición
Valencias Elementos
+1 y +2 Cu, Hg
+1 y +3 Au
+2 y +3 Fe, Co, Ni,
+1 Ag
+2 Zn, Cd
+2 y +4 Pt, Ge, S, Pb
+2, +3, y +6 (compuestos ternarios)
Cr
+2, +3, +4, +6 y +7 (4,6 y 7 en compuestos
ternarios)
Mn

Óxidos
Formula General : X2On
n es la valencia del elemento X
Óxidos Ácidos : No metal – Oxígeno
Óxidos Básicos: Metal – Oxígeno
Se nombran como Óxido de……. O con la terminación oso -ico

Hidruros
Formula General : MeHn - HnNoMe
n es la valencia del elemento X o Y
No Me Hidruros de no metal: No metal – Hidrógeno (+1)
Hidrácidos: F, Cl, Br, I, S, Se, TeHidruros volátiles: N, P, As, Sb, C, Si , B
Me Hidruros Básicos: Metal – Hidrógeno (-1)
Se nombran como Hidruros de…….

Sales Binarias
Formula General : MeaNmb
a es la valencia del No metal b es la valencia del Metal
Si el metal tiene una sola valencia:…….uro de metal
Si el metal tiene dos valencias:…..uro ……..oso……uro………ico

Hidróxidos
Formula General : Me(OH)n
n es la valencia del metal
Si el metal tiene una sola valencia:Hidróxido de metal
Si el metal tiene dos valencias:Hidróxido ……..osoHidróxido ………ico

Oxácidos
Formula General : HaNoMebOc
Acido hipo ……osoAcido …….oso
Acido….icoAcido per……ico

Sales de Oxácidos
Formula General : Mea(NoMebOc)n
n es la valencia del metal
hipo ……oso hipo…..ito…….oso ….ito
….ico atoper……ico per….ato