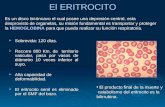
Prac ósmosis en el eritrocito
-
Upload
biofisica2011 -
Category
Documents
-
view
1.029 -
download
4
Transcript of Prac ósmosis en el eritrocito

Laboratorio de Biofísica Práctica “Ósmosis en el eritrocito”
OBJETIVOS
1. Conocer el procedimiento para la preparación de soluciones isoosmolares, hipoosmolares e hiperosmolares.
2. Calcular la presión osmótica de las soluciones. 3. Comprobar la correcta preparación de las soluciones, mediante la
observación al microscopio de la imagen normal de los eritrocitos en suspensión isotónica y los cambios producidos al ponerlos en contacto con soluciones hipo o hipertónicas de cloruro de sodio.
4. Calcular la concentración en mmol/l para iones y carbohidratos (sólo glucosa) de diferentes bebidas comerciales.
PROCEDIMIENTO
PREPARACIÓN DE LAS SOLUCIONES
Preparar 100 ml de las soluciones de cloruro de sodio siguientes:
1- Agua destilada 2- SS 25 mOsm/l 3- SS 50 mOsm/l 4- SS 75 mOsm/l 5- SS 100 mOsm/l 6- SS 125 mOsm/l 7- SS 150 mOsm/l 8- SS 175 mOsm/l 9- SS 200 mOsm/l 10- SS 300 mOsm/l ó 0.9% 11- SS 600 mOsm/l 12- SS 1200 mOsm/l
OBSERVACIÓN DE LOS CAMBIOS MORFOLÓGICOS DE LOS ERITROCITOS
1. Homogenice suavemente, haciendo ochos en la mesa, la suspensión de eritrocitos y con una pipeta Pasteur coloque una gota en un portaobjetos limpio, cúbrala con el cubreobjetos y con cuidado póngala en la platina del microscopio.
2. Encienda la luz del microscopio, ajuste la distancia interpupilar de los oculares (si es binocular) y la posición del diafragma (cerrado), recuerde que la profundidad del campo y la resolución mejoran con el diafragma cerrado.
3. Cerciórese que la platina del microscopio esté alejada de los objetivos, ponga en el revólver el objetivo de más bajo poder (lupa), y con el enfoque macrométrico acerque lentamente la preparación al objetivo. Observe el

aspecto general del campo a bajo poder, cerca de un borde y seleccione una parte en la que se encuentren las células dispersas pero abundantes.
4. Enfoque con el poder siguiente; como el microscopio está en buenas condiciones, la lente es isofocal con la anterior por lo que sólo se requiere un ligero ajuste con el enfoque micrométrico. Observe el aspecto de las células presentes.
5. Lleve ahora la preparación al alto poder (40x) (OJO NO ES INMERSION - NO ES EL DE 100 X) fíjese que el objetivo entre en posición sin tocar la lámina , sin llenarse de líquido. Para esto puede ver por el lado del microscopio a la preparación y al objetivo. Observe la morfología general. Dibuje un eritrocito. Compare las dimensiones del eritrocito con el diámetro del campo.
6. Desplace lentamente la preparación hacia uno de los bordes del cubreobjetos. Coloque una gota de solución hipertónica de NaCl en el borde del cubreobjetos. Espere a que cese el flujo hidráulico. Observe la apariencia de los eritrocitos ahora en el medio hipertónico. (Dibuje).
7. Realice una preparación para observar la morfología de los eritrocitos con las soluciones de cloruro de sodio de 600, 300, 100 y 0 mOsm/l, realizando esquemas y anotaciones en su libreta.
DETERMINACION DE LA CURVA DE FRAGILIDAD OSMÓTICA
Los eritrocitos constituyen una población heterogénea, debido a sus variaciones en tamaño, (micro, normo y macrocitos), forma (esferocitos, bicóncavos, en diana), edad, etc. Esto determina que no todos presenten la misma resistencia a los cambios en la presión osmótica del medio que los rodea. Como no nos interesa la dinámica de la hemólisis, sino un punto final, la medición se hace luego de transcurrido un lapso de tiempo que nos asegure que se ha alcanzado el punto final.
Utilizaremos una serie de tubos con concentraciones crecientes de solución salina, desde el agua destilada, osmolaridad = 0, hasta salina al 0,9%, osmolaridad = 300mOsm, o isotónica con el plasma, y observaremos la hemólisis que se produce una vez alcanzado el punto de equilibrio. Como la hemoglobina se encuentra dentro de los eritrocitos, mediremos la hemoglobina disuelta como una medida del grado en que se han hemolizado los eritrocitos. Para evitar la interferencia de las células, las separaremos por centrifugación a mediana velocidad, y mediremos la concentración de hemoglobina en el líquido sobrenadante.
1. Numere una serie de tubos y agregue en cada uno 4,6 ml de las concentraciones de solución salina 1 a la 10 (desde agua destilada hasta SS 300 mOsm).

2. Agregue a cada uno de los tubos 0,4ml de la suspensión de eritrocitos al 4%. Cada vez que tome eritrocitos debe asegurarse de homogeneizar la mezcla.
Cubra la boca del tubo con una película de parafina (parafilm) y agite el tubo suavemente por inversión, para homogeneizar los componentes de la mezcla.
3. Deje reposar 10 min a temperatura ambiente, para que los eritrocitos reaccionen con la solución.
4. Equilibre los tubos en parejas. Centrifúguelos a velocidad intermedia durante cuatro minutos. Los tubos número 1 y 2 no hay necesidad de centrifugarlos.
5. Saque los tubos con cuidado y extraiga el sobrenadante con pipeta Pasteur, TENGA MUCHO CUIDADO DE NO TOCAR EL BOTON DE ERITROCITOS QUE SE FORMO EN EL FONDO DEL TUBO. Ponga el sobrenadante en otro tubo bien identificado.
6. Lleve los tubos al fotómetro y léalos a 540nm de longitud de onda, pídale al asistente que calibre el aparato para que lea directamente concentración, con el contenido del tubo del agua destilada al 0% y eritrocitos al 4% en agua destilada, como el 100% de hemólisis. Anote los valores obtenidos en cada tubo.
Referencias Pacheco, L. F. 2007. “Osmosis y permeabilidad del eritrocito”. Departamento de Fisiología, Escuela de Medicina, Universidad de Costa Rica