GUIA Y PROTOCOLO DE ACTUACION INSPECTIVA ACTOS ANTISINDICALES
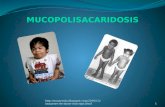
Protocolo de actuacion en las mucopolisacaridosis
-
Upload
andres-dante-podesta -
Category
Documents
-
view
1.863 -
download
5
Transcript of Protocolo de actuacion en las mucopolisacaridosis

PROTOCOLO DE ACTUACIÓN EN LAS MUCOPOLISACARIDOSIS
A González-Meneses López, A Barcia Ramírez, JL Díaz Rodríguez
González-Meneses López A, Barcia Ramírez A, Díaz Rodríguez JL. Protocolo de actuación en las mucopolisacaridosis.
Protoc diagn ter pediatr. 2010;1:24-36.
INTRODUCCIÓN
Las mucopolisacaridosis (MPS) son errores in-natos del metabolismo secundarios a defec-tos enzimáticos que producen un acúmulo li-sosomal de diversos tipos de glucosamino-glucanos (GAG) provocando consecuente-mente síntomas progresivos en todos los ór-ganos y sistemas. Son por tanto enfermeda-des multisistémicas que requieren un enfo-que multidisciplinar para su tratamiento ymanejo adecuado. En los últimos años se hanproducido avances muy importantes en eltratamiento de estas enfermedades con laaparición de tratamientos enzimáticos susti-tutivos, inhibidores de sustrato y mejoras enla supervivencia de los trasplantes de médulaósea. Además, en el horizonte cercano se es-tán perfeccionando estos mismos tratamien-tos ayudados con detecciones muy precocesen la prueba del talón, diagnósticos genéti-cos preimplantatorios, fármacos capaces desaltarse los codones de parada prematura, yotros que impiden que una enzima defectuo-sa, pero aún con capacidad residual de actua-ción se degrade (fármacos chaperones). To-das estas novedades suponen una gran espe-ranza para los afectados por estas enferme-dades y sus familias y un reto para los profe-sionales encargados del diagnóstico, trata-miento y seguimiento de los mismos.
El objetivo de este protocolo de actuación esayudar al diagnóstico, tratamiento y segui-miento adecuado de estas enfermedades apo-yándonos en las nuevas herramientas tera-péuticas, pero dentro de un enfoque multidis-ciplinar y multisistémico de las mismas, yaque, de otro modo, no se puede dar una res-puesta integral a una enfermedad global.
CLASIFICACIÓN
Las MPS podemos clasificarlas según la enzi-ma alterada y, dentro de cada tipo, en diversasmanifestaciones clínicas. En la siguiente tablapodemos ver la clasificación de estas enferme-dades.
CLÍNICA
Mucopolisacaridosis tipo I (OMIN 252800)La MPS I es la mucopolisacaridosis causadapor el déficit de la enzima a-1-iduronidasa, loque provoca un acúmulo heparán y dermatánsulfato.
Es una enfermedad autonómica recesiva, y elgen responsable está localizado en el locus4p16.3. Las mutaciones más frecuentementeencontradas en estos pacientes son W402X y
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
24

Q70X, que provocan un déficit total de activi-dad enzimática. La prevalencia varía según lasdistintas áreas geográficas, de 1:111000 a1:84000 nacidos vivos.
Es una enfermedad progresiva y potencial-mente mortal. Muestra un espectro muy di-verso de síntomas que afectan a numerososórganos y aparatos.
Dependiendo del grado de déficit de actividadenzimática, podemos encontrar distintas ma-nifestaciones clínicas, clasificándose según sugravedad en:
a) Síndrome de Hurler: forma más grave dela enfermedad, de progresión rápida.Diagnóstico antes de los 2 años de edady una esperanza de vida menor a 20 añossin tratamiento.
b) Síndrome de Scheie: forma más atenuadade la enfermedad, de progresión más lenta.Diagnóstico a partir de los 10 años de edadcon una esperanza de vida de 35 a 40 años.
c) Síndrome Hurler-Scheie: formas interme-dias de la enfermedad. Diagnóstico entre
los 3 y 8 años. Esperanza de vida de entre 20y 30 años.
En la MPS I las manifestaciones de la enferme-dad son multisistémicas, progresivas y hetero-géneas, con distintos órganos involucradoscon diferente nivel de gravedad.
• Aspecto general:
– Rasgos faciales toscos: nariz aplastada,labios engrosados, macroglosia, altera-ción en la forma de los dientes, orejasde implantación baja, con lóbulos pro-minentes.
– Macrocefalia con frente prominente.
– Hipertricosis de la cara y del cuerpo.Pelo estropajoso.
– Engrosamiento de la piel.
– Cuello corto.
• Manifestaciones del sistema nervioso cen-tral (SNC) y sistema nervioso periférico(SNP):
TIPOIH
MPS I ISIH/S
MPS IIAB
MPS III CD
MPS IV A
BMPS VI
MPS VII
MPS IX
ENZYMA DEFICIENTE
a-1-iduronidasa
Iduronato sulfataseHeparan N-sulfatasa-N-Acetila-glucosaminidasaa-glucosaminida acetiltransferasaN-Acetilglucosamina 6-sulfatasaGalactosa 6-sulfatasaa-GalactosidasaArylsulfatasa B
a-Glucuronidasa
a-Hialuronidasa
GAG AFECTADO
Dermatán y heparán sulfato
Dermatán y heparán sulfato
Heparan sulfato
Keratan sulfato, condroitin 6-sulfatoKeratan sulfatoDermatan sulfatoDermatan y heparan sulfato,condroitin 4 y 6 sulfatoÁc. Hialurónico
LOCUS CROMOSÓMICO
4p16.3
Xq2817q25.317q218p11.112q14
16q24.3
3p21.335q13-q14
7q21.11
3p21.2 – p21.3
EPÓNIMOHurlerScheieHurler-ScheieHunter
SanFilippo
Morquio
Maroteaux-Lamy
Sly
25
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
Protocolos • Protocolo de actuación en las mucopolisacaridosis

– Trastornos del aprendizaje.
– Retraso mental.
– Hidrocefalia comunicante.
– Compresión de la médula espinal.
– Síndrome del túnel carpiano/mano engarra.
• Manifestaciones oftalmológicas:
– Opacidad corneal.
– Disminución de agudeza visual.
– Ceguera.
– Glaucoma.
– Fotosensibilidad.
• Manifestaciones otorrinolargológicas(ORL):
– Rinorrea.
– Otitis media e infecciones respiratoriasrecurrentes.
– Pérdida de audición.
– Respiración ruidosa.
– Obstrucción de las vías aéreas supe-riores.
– Apnea/hipopnea durante el sueño.
– Astenia y somnolencia diurna.
• Manifestaciones del aparato respiratorio:
– Síndrome restrictivo y obstructivo.
– Disnea.
– Infecciones de las vías respiratorias re-currentes.
– Insuficiencia respiratoria.
– Hipertensión pulmonar, Cor pulmo-nale.
• Manifestaciones del aparato cardiovascu-lar:
– Displasia valvular/insuficiencia aórticay mitral.
– Obstrucción de las arterias coronarias.
– Arritmias.
– Hipertrofia ventricular izquierda.
– Miocardiopatía/insuficiencia cardíaca.
• Manifestaciones del aparato digestivo:
– Hepatosplenomegalia.
– Hernia umbilical e inguinal recurrentes.
– Diarrea/estreñimiento.
• Manifestaciones osteoarticulares:
– Rigidez articular.
– Contracturas articulares.
26
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
Protocolos • Protocolo de actuación en las mucopolisacaridosis

– Disóstosis múltiple.
– Displasia de cadera.
– Genu valgo.
– Cifosis lumbar.
– Baja estatura.
– Atrapamiento de los nervios.
– Mano en garra.
– Limitación de la movilidad y de la capa-cidad de deambulación.
Mucopolisacaridosis tipo II o síndrome de Hunter (OMIM 309900).Está causada por la deficiencia de la enzima li-sosomal, Iduronato 2 Sulfatasa (I2S). Esta enzi-ma es el primer paso en el metabolismo de losGAG, heparan sulfato y dermatan sulfato. Elfenotipo clínico va a estar caracterizado por eldepósito de estos GAG en los diferentes teji-dos y órganos.
Es la única MPS con un patrón de herencia re-
cesivo ligado al cromosoma X. El gen de la I2Sse localiza en Xq28 y se han descrito más de300 mutaciones1. Aunque no cabría esperar elpadecimiento de la enfermedad en el sexo fe-menino, hay descritos unos pocos casos desíndrome de Hunter en niñas2.
Su incidencia está estimada en 1,3 casos porcada 100.000 recién nacidos varones vivos3.
Es una enfermedad multiorgánica y multisis-témica con una variabilidad clínica interindi-vidual considerable entre formas severas yformas más atenuadas (Tabla 2). En la actua-lidad se considera la existencia de un espec-tro clínico entre fenotipos graves y atenua-dos, siendo la afectación del sistema nervio-so central preponderante para clasificar a losdiferentes individuos4. Al nacimiento la apa-riencia puede ser normal. Las característicasfaciales son muy similares a las de otrasMPS, facies tosca, macrocefalia con frenteprominente, naríz ancha, orejas de implan-tación baja, labios gruesos y macroglosiaque puede protuir. Estos rasgos comienzan aser evidentes entre los 18 y 24 meses deedad en formas graves3. En estos casos lamuerte ocurre en la primera o segunda déca-
Tabla 2. Manifestaciones de MPS I según severidad de la enfermedad.
Manifestación clínica Hurler Formas intermedias ScheieRetraso mental +++++ -Hidrocefalia comunicante +++ +/- -Compresión de médula espinal +++ +++ ++Pérdida de audición +++ ++ +/-Opacidad corneal +++ +++ +++Rigidez articular +++++ ++++ +++Patología obstructiva de vías aéreas +++++ +++ ++Patología cardíaca +++++ ++++ +++Síndrome del túnel carpiano +++++ ++++ +++Disóstosis múltiple +++++ +++ +/-Hernia umbilical o inguinal ++++ +++ +++Rasgos faciales toscos +++++ +++ +/-
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
27

da de la vida, habitualmente a causa de en-fermedad respiratoria obstructiva o fallo car-díaco asociado al deterioro de las funcionesneurológicas. En las formas más atenuadaslos signos y síntomas clínicos aparecen mástardíamente siendo la disfunción neurológi-ca mínima. Estos pacientes tienen una inteli-gencia normal y pueden sobrevivir hastaetapas tempranas de la edad adulta (algu-nos individuos pueden tener una supervi-vencia hasta la quinta o sexta década de lavida).
Mucopolisacaridosis tipo III o síndrome deSanFilippo (OMIN MPS IIIA 252900, MPS IIIB25920, MPS IIIC 252930, MPS IIID 252940)Está causada por la deficiencia de varias enzi-mas lisosomales encargadas de la degrada-ción del GAG, heparan sulfato. Dependiendodel enzima deficitario van a clasificarse en 4 subtipos (Tabla 1). En el caso del subtipo D
(déficit de a-N-Acetilglucosamina 6-sulfatasa)también va a ocurrir una alteración en el me-tabolismo del keratan sulfato.
Su incidencia se estima en 1 de cada 70.000recién nacidos vivos, considerándose la MPSmás frecuente en Europa, siendo el subtipoA, el más prevalente en gran parte del conti-nente6,7,8. A pesar de esto, su diagnóstico esdificultoso porque sus rasgos físicos son di-ferentes al de otras MPS. También existe va-riabilidad fenotípica entre los distintos sub-tipos, aunque la distinción entre los mismossuele ser difícil. Generalmente, el subtipo Asuele ser el más grave con un inicio mástemprano y con mayor progresión sintomá-tica. El resto de subtipos tienen mayor hete-rogeneidad en cuanto a la sintomatología.La clínica va a girar entorno a la grave afec-tación del SNC. El inicio de la misma ocurreentre los 2 y 6 años con un retraso en la ad-
Tabla 3. Manifestaciones clínicas de los pacientes con MPS tipo II (Síndrome de Hunter). Datos de pacientesespañoles registrados en Hunter Outcome Survey (HOS) Marzo 2008.
Manifestación clínica Pacientes Porcentaje (N total = 30)Manos en “garra” 19 63%Hipertrofia Amígdalar 24 80%Otitis recurrentes 28 93%Macroglosia 25 83%Hernia (umbilical/inguinal) 25 83%Rigidez articular 30 100%Hepatomegalia 29 97%Esplenomegalia 21 70%Facies toscas 30 100%Enfermedad valvular 17 57%Soplo 12 40%Cardiomiopatía 2 7%Problemas cardiovasculares 21 70%Problemas respiratorios 23 77%Hidrocefalia 4 13%Retraso cognitivo 11 37%Hiperactividad 9 30%Problemas neurológicos 26 87%Síndrome del tunel del carpo 1 3%Rigidez cadera 11 36%Lesiones hipocromas en escápula (típicas de la enfermedad) 8 26%
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
28

quisición de la deambulación y el lenguaje.Es frecuente el inicio posterior a esta etapade una gran hiperactividad que dificultaenormemente la convivencia. La hiperactivi-dad, el hirsutismo y una leve hepatoesple-nomegalia (menos evidente que en las otrasMPS) son muy características de este perio-do aunque pueden faltar. Los rasgos facialesno son tan claros como en las otras MPS pu-diendo tener una fascies normal o sólo leve-mente tosca, destacando lo poblado de lascejas. Los defectos en el sistema esqueléticoson mínimos no viéndose alterada en granmedida la talla final ni el balance articular.La regresión neurológica ocurre entre los 6 y10 años acompañada de un deterioro rápidode las habilidades adquiridas y alteracionesconductuales importantes merman la cali-dad de vida del paciente y de la familia. Enesta etapa de la enfermedad se va a produ-cir un empeoramiento de los episodios con-vulsivos, alteraciones conductuales y delsueño. El lenguaje suele ser pobre, falto dearticulación y contenido, con un curso regre-sivo añadido. En la última etapa se produceun mayor deterioro físico por la falta de con-trol muscular, apareciendo problemas paracaminar o mantenerse sentados, llevándo-los a la postración en cama. En este períodola alimentación se precisa a través de sondanasogástrica y la aspiración de secrecioneses importante. La supervivencia va a depen-der de la afectación neurológica, siendo es-timada entre la segunda y cuarta década dela vida5.
Mucopolisacaridosis tipo IV o síndrome deMorquio. (OMIN MPS IVA 253000 y MPS IVB253010)Está causada por la deficiencia de dos enzi-mas implicadas en el metabolismo del kera-
tan sulfato, galactosa-6sulfatasa en el subti-po A y la galactosidasa en el subtipo B. Estaúltima enzima también se sitúa en el meta-bolismo de los gangliósidos. Estas diferenciasbioquímicas van a ser en muchos casos pri-mordiales en el diagnóstico diferencial deambos subtipos.
La incidencia, en conjunto, estimada es de 1 decada 263.000 recién nacidos vivos, siendo elsubtipo A el más frecuente8.
Las manifestaciones clínicas van a girar en-torno a la afectación esquelética tan impor-tante que se produce en la MPS IV y suelenaparecer en ambos subtipos, considerando alsubtipo A, el fenotipo más grave. Al naci-miento la mayoría de los pacientes suelenpasar desapercibidos, pudiendo presentarocasionalmente, pie zambo o limitación a laabducción de la cadera. Los primeros signosson evidentes al final de primer año de vida,desarrollando giba toracolumbar, claramentevisible sentado. Suele ser el primer motivo deconsulta. En el segundo año se va producien-do el retraso estatural caracterizado por untronco corto con respecto a la longitud de losmiembros. La rigideces articulares tambiénson importantes. Todos los pacientes conMPS IV van a presentar alteraciones denta-rias. La opacidad corneal es frecuente aun-que puede pasar desapercibida en muchoscasos. La hepatoesplenomegalia es poco fre-cuente en el síndrome de Morquio. El des-arrollo psicomotor es normal y se puede verdificultado por la existencia de sordera neu-rosensorial o de conducción. La deambula-ción se va a ver dificultada por el genu valgo.En la primera infancia hay que vigilar los sig-nos de compresión de canal medular (agota-miento rápido de la marcha o signos pirami-
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
29

dales en extremidades inferiores). En la cuar-ta o quinta década de la vida, las importantesdeformidades torácicas producen dificulta-des en la función pulmonar y cardiaca, redu-ciendo la esperanza de vida.
Mucopolisacaridosis tipo VI o síndrome de Maroteaux-Lamy (OMIN 253200)Se produce por la deficiencia de la enzima aril-sulfatasa B, responsable de la degradación deldermatan sulfato.
Su incidencia es menor que el de las anterio-res MPS (1 de cada 455.000 recién nacidosvivos)8.
Las características clínicas son similares a lasdel síndrome de Hurler, aunque en la MPS VI, eldesarrollo mental es normal. La variabilidad clí-nica es importante pudiendo encontrar dife-rentes grados de severidad. Generalmente, enla primera infancia, va a desarrollarse las alte-raciones en la curvatura vertebral, rigidez arti-cular y hernias umbilical e inguinal. La hepa -toesplenomegalia no es un signo constante. Laopacidad progresiva, así como la atrofia ópticason especialmente frecuentes en esta MPS. Elretraso estatural desproporcionado es ya evi-dente entre los 8 y 10 años. El acúmulo de GAGa nivel cardíaco va a producir una miocardiopa-tía hipertrófica y/o insuficiencia valvular, re-presentando la complicación más importanteen la segunda y tercera década de la vida.
DIAGNÓSTICO
Ante la sospecha clínica de que nos encontra-mos ante una MPS, la primera prueba a reali-zar es una determinación de GAG en orina. Pu-de emplearse una determinacion de orina
simple, aunque esta puede fallar en la MPS III.Recientemente se ha desarrollado por los Pro-fesores Sanjurjo y Galdámiz Echevarría un sis-tema de detección de GAG en orina simple a lacabecera del paciente muy barato y fiable, quepuede usarse adecuadamente como test descreening en la consulta.
Si se hallan en cantidades normales, podre-mos descartar en gran medida que se tratede una MPS, a excepción del síndrome deSanfilippo, en el que unos GAG en orina nor-males no descartan el cuadro, siendo precisauna determinación de GAG en orina de 24horas.
Si los GAG en orina se hallan elevados, o existeuna alta sospecha de síndrome de Sanfilipo apesar de unos niveles de GAG normales, habráque continuar con el proceso diagnóstico paradeterminar qué tipo de MPS es la que padeceel paciente, aunque según el tipo de GAG quese encuentre aumentado y la clínica, podamossospechar de qué MPS se trata, como se verámás adelante en el algoritmo diagnóstico (Al-goritmo 1).
Tras una determinación de GAG en orina com-patible con MPS, se debe realizar la determi-nación de la actividad enzimática de aquellaenzima que sospechamos causal de la enfer-medad. Esta determinación se suele realizaren leucocitos o fibroblastos, aunque la técnicamás idónea (sobre todo para cribado neona-tal) es la Dryed Blood Spots (DBS), que es unatécnica fluorimétrica o por espectometría detándem masas en gota de sangre seca.
Una actividad enzimática <10% es muy suges-tiva de MPS, y <1%-2% es diagnóstica de lamisma.
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
30

Una vez que confirmamos el diagnóstico me-diante determinación de la actividad enzimá-tica, conviene realizar el diagnóstico genético,que busca la mutación génica responsable dela enfermedad.
TRATAMIENTO
El tratamiento de las diversas MPS debe incluirtanto un tratamiento específico según el tipode enfermedad de que se trate (trasplante demédula ósea (TMO) si es eficaz, terapia enzi-mática sustitutiva si está disponible) como untratamiento global de las diversas manifesta-ciones clínicas que estas enfermedades multi-sistémicas presenten. Un tratamiento única-mente centrado en administrar terapia enzi-mática sustitutiva o en conseguir un TMO será
necesariamente incompleto si no va acompa-ñado de una actuación global sobre todos losórganos y sistemas afectados.
Sintomático
Problemas esqueléticos El ejercicio físico y las distintas medidas fisiote-rapéuticas (masajes, hidroterapia o electrotera-pia) van a ir dirigidos a mejorar las deformacio-nes óseas y articulares, la estabilidad vertebral,contracturas musculares y en resumen permitirla movilidad del paciente. Habrá que tener es-pecial cuidado con los procedimientos extre-mos de hiperextensión articular, porque podríaproducir cambios degenerativos.
Las indicaciones de uso de distintas ortesis yde cirugía correctora deben seguir un plan de
Algoritmo 1. Algoritmo diagnóstico en MPS.
Presentación clínicacompatible con MPS
Solicitar GAG en orina
(test DMB, Berry)
AlteradoNo alterado
Pensar en otro proceso
OligosacaridosisGlucoproteinosis
Mucolipidosis II / III
Otras enfermedadeshereditarias no
lisosomales
Test y patrón urinariode GAGs
- Heparán sulfato: MPS III (A, B, C, D).- Heparán sulfato + Dermatán sulfato:
MPS I, II, VII, MSD.- Dermatán sulfato: MPS VI.
- Keratán sulfato: MPS IV (A, B)
Estudio de actividad enzimática en leucocitos,fibroblastos, suero
Estudio de mutaciones
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
31

tratamiento individualizado que responda atres preguntas básicas: ¿Cuál es el problemaortopédico?, ¿qué beneficio vamos a obtenercon la cirugía? y ¿cuándo es el mejor momen-to para la misma?
Problemas neurológicos:Los problemas de compresión medular, de ner-vios craneales y periféricos (ej. síndrome de tu-nel del carpo) deben ser valorados por un neu-rocirujano. La colocación de válvulas de deriva-ción ventrículo-peritoneal representa una me-dida paliativa contra la hidrocefalia no influ-yendo en la progresión de la enfermedad8.
El progresivo deterioro de funciones cerebra-les (sobre todo en MPS II y III) va a llevar auna demencia importante acompañada detetraespasticidad generalizada. El uso deneurolépticos, psicoactivos y anticonvulsivosvan a ser necesarios para el control de losproblemas conductuales y los episodios con-vulsivos que se producen en esta periodo. Loscambios aislados en el trazado EEG no indi-can la introducción de antiepilépticos. Espe-cialmente en la MPS III se producen alteracio-nes en el sueño recomendando el uso de sis-temas de fijación a la cama y la administra-ción de melatonina (3 -30 mg/día) van a me-jorar estos síntomas y la calidad de vida delpaciente y de la familia.
Problemas oftalmológicos La opacidad corneal, principalmente en MPS I,VI y VII, va a necesitar un trasplante cornealpara restaurar la capacidad visual. Sin embar-go, la aparición de otros problemas como elglaucoma, la degeneración retiniana y la atro-fia óptica va a mermar el éxito de esta medi-da; de ahí, la importancia de un estudio oftal-mológico exhaustivo (tonometría, fundusco-
pia y si es posible, electrorretinografía). Tam-bién la afectación neurológica va a ser un fac-tor importante.
Problemas ORLEl acúmulo de GAG en tracto respiratorio su-perior produce infecciones respiratorias devias altas y otitis media recurrentes, y secun-dariamente una hipoacusia de transmisión.Por lo cual, medidas como la adenoamigda-lectomía y colocación de tubos de drenajetranstimpánico (DTT) van a mejorar estossíntomas (siempre de forma individualiza-da). El uso de oxígeno nocturno suplementa-rio (BIPAP/CPAP) en el síndrome de apneaobstructiva del sueño también ve a estar in-dicado.
Problemas respiratorios La afectación neurológica por un lado, y laafectación de paréquima pulmonar (hiperten-sión pulmonar) y deformidades torácicas, porotro, van a disminuir la función pulmonar oca-sionando frecuentes episodios de déficit deoxígeno. La adenoamigdalectomia, los DTT yBIPAP/CPAP van a paliar estos episodios. Estasalteraciones también van a provocar un au-mento de infecciones pulmonares con lo cualla fisioterapia respiratoria va a ser imprescin-dible.
Problemas cardiológicosLa esperanza de vida de muchos pacientesestá limitada a causa de las manifestacionescardíacas (cardiomiopatía hipetrófica e insu-ficiencia valvular). La profilaxis antibióticade endocarditis debería realizarse ante pro-cedimientos invasivos, una vez que se com-prueba la afectación cardíaca. Los digitálicosy diuréticos se usarán en la insuficiencia car-díaca.
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
32

Problemas con la anestesia:Los pacientes con MPS van a metabolizar dedistinta manera los anestésicos utilizados. Laintubación endotraqueal se ve dificultada porla macroglosia, la laringe estrecha y la rigidezcervical aumentando las complicaciones delos procedimientos anestésicos. La intubacióncon la ayuda de fibrobroncospio agiliza la mis-ma. Hay que prestar especial atención a la in-estabilidad atlantoaxoidea a la hora de hipe-rextender el cuello durante la intubación, es-pecialmente en el síndrome de Morquio. La in-suficiencia cardíaca, aunque sea leve, deberíaser premedicada antes de cualquier interven-ción que requiere anestesia. Por esta razones,estos procedimientos deberían llevarse a caboen unidades con experiencia.
Trasplante de progenitores hematopoyéticos (TMO)Aunque este tratamiento se ha realizado encasi todos los tipos de MPS, sólo se han com-probado resultados satisfactorios en los pa-cientes afectos de MPS I o síndrome de Hurler-Scheie, en los que es el tratamiento de elec-ción siempre y cuando sean menores de 2-3años y, sobre todo, tengan un CI mayor de 70,y en MPS II cuando se realiza antes del año deedad y sin afectación neurológica ya presente.
Pueden emplearse tanto células madre provi-nientes de médula ósea, como células de san-gre de cordón umbilical. Es el único procedi-miento disponible actualmente capaz de me-jorar la afectación neurológica de aquellas en-fermedades en las que es eficaz.
Ventajas e inconvenientes del TMO:
• Precisa una elevada histocompatibilidad anivel del HLA.
• No es un procedimiento exento de riesgoya que la mortalidad inducida por el proce-dimiento está en torno a un 20% según lasseries consultadas.
• Presenta problemas psicosociales por la di-ficultad de encontrar donantes y el aisla-miento del paciente al que obliga la inmu-nosupresión.
• No mejora sustancialmente los proble-mas musculoesqueléticos ni corneales,pero estabiliza los neurológicos y mejoraen gran medida la hepatoesplenomega-lia, la patología cardíaca, la patologíaobstructiva de las vías aéreas y los tras-tornos del oído.
• Se puede combinar con la terapia enzima-tica sustitutiva para optimizar los resulta-dos, ofreciendo este tratamiento desde elmomento del diagnóstico hasta la realiza-ción del trasplante y permitiendo la esta-bilización de la enfermedad, mejorandoasí la situación en la que el paciente llegaal trasplante. Debe mantenerse tras elmismo hasta que se detecten niveles enzi-máticos normalizados.
Terapia de sustitución enzimática MPS I: nombre de la enzima, Laronidasa.
Forma de administración: 100 Unidades/kg/semana iv, administrado con solución salinafisiológica a lo largo de 3-4 horas, aumentan-do paulatinamente la velocidad de infusiónhasta 30-40 mL/h aproximadamente.
Su indicación es el tratamiento enzimático sus-titutivo de los pacientes afectos de mucopolisa-caridosis tipo I. No atraviesa la barrera hema to-
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
33

encefálica por lo que no es efectiva para el trata-miento del depósito de GAG a nivel cerebral.
Puede requerir premedicación para disminuirla incidencia de efectos adversos. Habitual-mente se emplean antihistamínicos, paraceta-mol y, ocasionalmente, corticoides de 30 a 60minutos antes de la infusión. Ocasionalmentese ha requerido premedicación adicional unas12 horas antes de la infusión.
La mayor incidencia de efectos adversos relacio-nados con la infusión del medicamento se pro-duce entre la 4.ª y 6.ª infusión y suelen desapa-recer con la premedicación y el enlentecimientode la velocidad de infusión. Los más frecuentesson fiebre, rash cutáneo, sensación de ahogo odificultad respiratoria. Habitualmente no songraves y no suelen obligar a la suspensión deltratamiento. Se han descrito casos aislados deshock anafiláctico. Varias semanas tras la infu-sión es habitual la generación de anticuerposcontra el fármaco tipo IgE, con significado in-cierto, aunque no parece que aumenten losriesgos de reacciones adversas ni disminuyansignificativamente la efectividad del fármaco.
MPS II (Hunter): nombre de la enzima, Idursul-fasa.
Forma de administración: 0,5 mg/kg/semanaiv, diluido en 100 mL de solución salina fisioló-gica a lo largo de 3-4 horas, aumentando pau-latinamente la velocidad de infusión hasta 30-40 mL/h aproximadamente.
Los efectos secundarios y la necesidad de pre-medicación son similares a la Laronidasa, des-arrollándose también anticuerpos anti Idursul-fasa en las mismas condiciones que con la La-ronidasa. La premedicación suele ser necesaria
en muchos casos y bien tolerada. Tampocoatraviesa la barrera hematoencefálica por loque no es útil para los síntomas del sistemanervioso central asociados a esta enfermedad.
MPS VI (Maroteaux-Lamy): nombre de la enzi-ma, Galsulfasa.
Forma de administración: 1 mg/kg/semana iv,diluido en 100 mL de solución salina fisiológicapara menores de 20 kg o en 250 ml de soluciónsalina en los mayores de 20 kg. Se administra alo largo de unas 4 horas con un aumento paula-tino de la velocidad de infusión si es bien tolera-da. Se recomienda la administración de preme-dicación como en los medicamentos citadospreviamente. La producción de anticuerpos tipoIgG está también constatada en los tratamien-tos con Glasulfasa pero su significado continúasiendo incierto. Los efectos secundarios máshabituales son dolor abdominal, conjuntivitis ydolor auditivo, que suelen mejorar enlentecien-do la velocidad de infusión. Se han descritotambién reacciones tipo anafilactoides o reac-ciones adversas severas tipo edema angioneu-rótico, dificultad respiratoria o dolores intensosde cabeza que igualmente suelen ceder conuna interrupción temporal del tratamiento y laadministración adicional de antipiréticos,antihis tamínicos o corticoides.
Se recomienda la explicación clara de los posi-bles efectos adversos de la medicación, sus limi-taciones y expectativas mediante la firma de unconsentimiento informado al paciente o su fa-milia.
Actualmente no existe un tratamiento especí-fico eficaz ni para la MPS tipo III ni para la IV.Se encuentran actualmente activos diversosestudios de investigacion animal y en líneas
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
34

celulares, pero ninguno ha dado aún el salto ala experimentación en humanos. Los trata-mientos actualmente en estudio para estos ti-pos de MPS son inhibidores de sustrato, vecto-res virales de terapia génica y terapias enzimá-ticas sustitutivas. No obstante, actualmentelas únicas herramientas terapéuticas disponi-bles son un adecuado enfoque multidisplina-rio que permita minimizar las consecuenciasdel depósito de GAG en estos pacientes.
SEGUIMIENTO (Tabla 4)
El seguimiento de los pacientes con mucopoli-sacaridosis requiere una actuación multidisci-plinar y mantenida en el tiempo. Es conve-niente que este seguimiento se realice en cen-tros con experiencia en este tipo de enferme-
dades, bien de forma exclusiva, bien apoyan-dose en centros más cercanos al domicilio delenfermo pero coordinados con el centro ex-perto (centro de referencia).
Este seguimiento periódico tiene como objetomonitorizar la evolución del paciente, anticipar-se a la aparición de complicaciones y prevenirlassi es posible, corregir las disfunciones que vayanapareciendo y evaluar la efectividad de los trata-mientos aplicados. En caso de mucopolisacari-dosis sin tratamiento eficaz, es igualmente ne-cesario el tratamiento de las complicacionesque se irán produciendo a lo largo del tiempo.
En la tabla 4 exponemos una indicación de se-guimiento en los diversos tipos de mucopoli-sacaridosis, aunque éste debe, no obstante,individualizarse.
Tabla 4. Monitorización mínima en las MPS.
Evaluación inicial Cada 6 meses Cada 12 meses Cada 2 añosEvaluación clínica de MPSNeurológico/SNCRMN cerebral I, II, III I, II, IIIRMN espinal I, II, IV, VI I, II, IV, VIEstudio oftalmológico (Tonometría, agudeza visual, examen de retina y córnea) I, II, III, IV, VI I, II, IV, VI
Audición (Audiometría) I, II, III, IV, VI I, II, III, IV, VIPotenciales evocados somatosensoriales I, II, III, IV, VI I, II, III, IV, VIEstudio cardiológico (ECG, ecografía)*Si alteraciones I, II, IV, VI * I, II, IV, VI I, II, IV, VI
RespiratorioCVF/VEF1*Si alteraciones I, II, IV, VI * I, II, IV, VI
Estudio de sueño I, II, IV, VI I, II, IV, VIGastrointestinalVolumen del hígado I, II, III, IV, VI I, II, VIMusculoesqueléticoExamen rehabilitador I, II, III, IV, VI I, II, III, IV, VISignos vitales y pruebas de laboratorioEstatura y peso I, II, III, IV, VI I, II, III, IV, VIPerímetro craneal I, II, III, IV, VI I, II, III, IV, VIPresión arterial I, II, III, IV, VI I, II, III, IV, VINiveles de actividad enzimática I, II, III, IV, VINiveles de GAG en orina*Si Terapia de sustitución enzimática I, II, III, IV, VI *I, II, VI
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
35

7. BIBLIOGRAFÍA
1. Martin R, Beck M, Eng C, Giugliani R, Harmatz P,Muñoz V et al. Recognition and diagnosis ofMucopolysaccharidosis II (Hunter syndrome).Pediatrics. 2008;121:e377-87.
2. Tuschl K, Gal A, Paschke E, Kircher S, BodamerOA. Mucopolysaccharidosis type II in females:case report and review of literature. PediatrNeurol. 2005;32:270-2.
3. Wraith JE, Scarpa M, Beck M, Bodamer OA, DeMerleir L, Guffon N et al. Mucopolysaccharido-sis type II (Hunter syndrome): a clinical reviewand recommendations for treatment in the eraof enzyme replacement therapy. Eur J Pediatr.2008;167(3):267-77.
4. Muenzer J, Wraith JE, Beck M, Giugliani R, Har-matz P, Eng CM, et al. A phase II/III clinical studyof enzyme replacement therapy with idursulfa-se in mucopolysaccharidosis type II (Huntersyndrome). Gen Med. 2006;8(8):465-73.
5. Neufeld EF, Muenzer J. The Mucopolysacchari-doses. The metabolic and molecular bases ofinherited disease, Chapter 136, Vol III, 8ht ed.New York: Ed. McGraw-Hill; 2001.
6. Baehner F, Schmiedeskamp C, Krummenauer F,Miebach E, Bajbouj M, Whybra C et al. Cumula-tive incidence rates of the mucopolysacchari-doses in Germany. J Inherit Metab Dis.2005;28(6):1011-7.
7. Nelson J. Incidence of mucopolysaccharidosesin Nothern Ireland. Hum Genet. 1997;101(3):355-8.
8. Kircher SG, Bajbouj M, Miebach E, Beck M. Mu-copolysaccharidoses: A guide for physiciansand parents. 2007. Uni-med.
9. Kakkis ED, Muenzer J, Tiller G, Waber L, BelmontJ, Passage M et al. Enzyme-replacement the-rapy in Mucopolysaccharidosis I. N Eng J Med.2001;344:182-8.
10. Casas Fernández C. Actualización clínica delsíndrome de Hunter (MPS II); Rev Neurol. 2007;44(Supl. 1).
11. Tolar J, Grewal SS, Bjoraker KJ, Whitley CB, Sha-piro EG, Charnas L et al. Combination of enzymereplacement and haematopoietic stem celltransplantation as therapy for Hurler syndrome.Bone Marrow Transplant. 2008;41(6):531-5.
Protocolos • Protocolo de actuación en las mucopolisacaridosis
©Asociación Española de Pediatría. Prohibida la reproducción de los contenidos sin la autorización correspondiente. Protocolos actualizados al año 2010. Consulte condiciones de uso y posibles nuevas actualizaciones en www.aeped.es/protocolos/
ISSN 2171-8172
36