SISTEMA DE GESTION DE CALIDAD APOYO DIAGNOSTICO …181.48.57.101/Carpetas/Formatos y Docs/10....
Transcript of SISTEMA DE GESTION DE CALIDAD APOYO DIAGNOSTICO …181.48.57.101/Carpetas/Formatos y Docs/10....

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
TABLA DE CONTENIDO
INTRODUCCION ................................................................................................................. 4
JUSTIFICACION .................................................................................................................. 4
MARCO TEORICO ............................................................................................................... 4
1 ANTICOAGULANTES ................................................................................................ 5
1.1 OXALATO DE AMONIO Y POTASIO ......................................................................... 5
1.2 CITRATO DE SODIO AL 3.8% ................................................................................ 5
1.3 HEPARINA .............................................................................................................. 6
1.4 EDTA (ETILEN DIAMINO TETRA ACETATO) ........................................................ 6
1.5 CPD o ACD (CITRATO FOSFATO DEXTROSA) .................................................... 6
2 HEMATOLOGIA Y COAGULACION ............................................................................. 6
2.1 HEMATOLOGIA ...................................................................................................... 6
2.2 COAGULACION ...................................................................................................... 6
3 CUADRO HEMATICO AUTOMATIZADO ..................................................................... 6
3.1 EQUIPO HORIBA PENTRA XL 80 .......................................................................... 8
3.1.1 PARTES DEL EQUIPO ........................................................................................... 8
3.1.2 INTRODUCCION AL SOFWARE .......................................................................... 12
3.1.3 MODOS DE OPERACION .................................................................................... 16
3.1.4 ESPECIFICACIONES DEL EQUIPO ..................................................................... 17
3.1.5 PARAMETROS ..................................................................................................... 18
3.1.6 ESPECIFICACIONES DEL INSTRUMENTO ........................................................ 25
3.1.7 CONDICIONES GENERALES .............................................................................. 26
3.1.8 INDICACIONES PARA EL PROCESAMIENTO DE MUESTRAS ......................... 26
3.1.9 REACTIVOS DEL EQUIPO ................................................................................... 30
3.1.10 ........................................................................ ALARMAS Y AVISOS DEL EQUIPO
33
4 FROTIS DE SANGRE PERIFERICA ........................................................................... 40
4.1 CARACTERISTICAS MORFOLOGICAS DE LOS GLOBULOS ROJOS ............... 42

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
4.2 CARACTERISTICAS MORFOLOGICAS DE LOS LEUCOCITOS ........................ 43
4.3 CARACTERISTICAS MORFOLOGICAS DE LAS PLAQUETAS .......................... 44
5 RECUENTO DE RETICULOCITOS ............................................................................ 44
5.1 PRINCIPIO ............................................................................................................ 44
5.2 METODOLOGIA .................................................................................................... 44
6 VELOCIDAD DE SEDIMENTACION GLOBULAR ...................................................... 45
6.1 PRINCIPIO ............................................................................................................ 45
6.2 METODOLOGIA .................................................................................................... 45
7 RECUENTO DE PLAQUETAS .................................................................................... 47
7.1 PRINCIPIO ............................................................................................................ 47
7.2 METODOLOGIA .................................................................................................... 47
8 HEMOCLASIFICACION .............................................................................................. 49
8.1 PRINCIPIO ............................................................................................................ 49
8.2 METODOLOGIA .................................................................................................... 49
9 DETERMINACION DEL FACTOR Rh ......................................................................... 50
9.1 PRINCIPIO ............................................................................................................ 50
9.2 PREPARACION DE LOS REACTIVOS ................................................................. 50
9.3 METODOLOGIA .................................................................................................... 50
10 TEST DE COOMBS INDIRECTO ................................................................................ 52
10.1 PRINCIPIO ............................................................................................................ 52
10.2 METODOLOGIA .................................................................................................... 52
11 DETERMINACION DEL ANTIGENO Du ..................................................................... 53
11.1 METODOLOGIA .................................................................................................... 53
12 TEST DE COOMBS DIRECTO ................................................................................... 53
12.1 PRINCIPIO ............................................................................................................ 53
12.2 METODOLOGIA .................................................................................................... 53
13 TIEMPO DE PROTROMBINA ..................................................................................... 54
13.1 PRINCIPIO ............................................................................................................ 54
13.2 FUNDAMENTO ..................................................................................................... 54
13.3 REACTIVOS Y MATERIALES ............................................................................... 54

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
13.4 MUESTRA ............................................................................................................. 54
13.5 METODOLOGIA .................................................................................................... 54
14 TIEMPO DE TROMBOPLASTINA PARCIAL ACTIVADO (PTT) ................................. 55
14.1 PRINCIPIO ............................................................................................................ 55
14.2 FUNDAMENTO .................................................................................................. 56
14.3 REACTIVOS .......................................................................................................... 56
14.4 MATERIALES ........................................................................................................ 56
14.4 MUESTRA ............................................................................................................. 56
14.5 METODOLOGIA .................................................................................................... 56
14.6 INTERVALO DE REFERENCIA ............................................................................ 56
14.7 METODO DE CONTROL DE CALIDAD ................................................................ 57
14.8 INTERFERENCIAS DEL METODO ....................................................................... 57
14.9 INTERPRETACION DE LOS RESULTADOS ....................................................... 57
15. LEISHMANISIS CUTANEA ................................................................................... 57
15.1 METODOS DIAGNOSTICOS EN LEISHMANISIS CUTANEA .............................. 57
16. DIAGNOSTICO MICROSCOPICO DE MALARIA ................................................. 59
16.1 TOMA DE MUESTRA Y ELABORACION DE MUESTRAS ................................... 60
VERIFICACION DE LAS CONDICIONES OPTIMAS DE LAS MUESTRAS ......... 63
LISTA DE CHEQUEO MANUAL DE HEMATOLOGIA .......................................... 64
CONTROL DE CAMBIOS ..................................................................................... 66
BIBLIOGRAFIA ..................................................................................................... 67

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
INTRODUCCION
El hemograma automatizado es el resultado de años de investigación y evolución, en los cuales, paso a paso se fueron realizando mejoras que han beneficiado la técnica y al profesional, y que hoy generan practicidad y especificidad. En él se aborda el análisis de las características sanguíneas, que brindan un esquema del estado fisiológico del paciente, como anemias, hemoconcentración, procesos febriles, infecciosos y cancerígenos. El presente manual ha sido elaborado para que su contenido sea fácil de entender por el personal que labora en el laboratorio ESE ISABU el cual contiene los aspectos más importantes del laboratorio, se exponen las principales técnicas básicas del laboratorio de hematología y las alteraciones más frecuentes de los componentes de la sangre. El manual tiene el propósito de ordenar todos los procedimientos que se realizan y tener un instrumento que facilite el desarrollo adecuado, sistematizado y estandarizado de los procedimientos técnicos en la sección de Hematología de este modo se contribuye a mejorar la calidad de diagnóstico. El laboratorio de hematología cuenta con equipos de alta tecnología siguiendo y cumpliendo las pautas de los controles de calidad interno y externo.
OBJETIVOS
Contar con un documento de consulta y orientación para el personal del laboratorio clínico del HLN y la UIMIST
Determinar y estandarizar las actividades que se deben de seguir y realizar en el Laboratorio Clínico en el área de Hematología, con el fin de obtener resultados confiables que sean útiles para establecer el diagnóstico, evaluar la evolución y/o pronóstico de una enfermedad, así como la valoración de la efectividad de un tratamiento.
Ser una herramienta, práctica, de fácil acceso y fácil compresión para todo el personal que trabaja en el laboratorio clínico
ALCANCE
Este manual ha sido diseñado para el personal de Bacteriología que se encuentre procesando muestras biológicas en el área de Hematología del laboratorio clínico de la ESE ISABU.
GLOSARIO
Amastigotes: Forma aflagelada que se evidencia en los tejidos infectados. Anemia: - una condición en la que hay una disminución en la cantidad de hemoglobina debido a una disminución del número de células rojas de la sangre. Anemia hemolítica: es un grupo de trastornos hemolíticos (sea intravascular como extravascular), que causan la disminución de la masa de glóbulos rojos sanguíneos. Agregacion plaquetaria: Atracción y adhesión de una plaqueta a otras. Cuadro hemático: Análisis cuantitativo y cualitativo de los componentes celulares de la sangre periférica

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Coagulación: Proceso en el que se forman coágulos de sangre. Unas variedades de factores son necesarias para que la sangre tenga una habilidad normal de coagular. La habilidad de coagular es evaluada por varios exámenes de sangre incluyendo el tiempo de protrombina (TP), tiempo parcial de tromboplastina (TPT), y el conteo de plaquetas. Examenes ABO: Exámenes de sangre que clasifican la sangre humana en uno de cuatro grupos: A, B, O, ó AB. Glóbulos Rojos: Células en la sangre que transportan el oxígeno a la sangre y los tejidos. Granulocitos: Un sub-tipo de glóbulos blancos nombrados debido a la presencia de gránulos en la célula. Estas células protegen el cuerpo contra la infección bacteriana. Hematocrito: Parte de la sangre ocupada por glóbulos rojos. Hematopoyesis: Formación de los glóbulos rojos de la sangre, que tiene lugar principalmente en la médula roja de los huesos. Hemoglobina: La parte de los glóbulos rojos que transporta el oxígeno a los tejidos. Hemolisis: Destrucción de los hematíes o glóbulos rojos de la sangre que va acompañada de liberación de hemoglobina. Hemostasia: Contención o detención de una hemorragia mediante los mecanismos fisiológicos del organismo. Incompatibilidad sanguínea: Situación existente entre 2 individuos que pertenecen a grupos sanguíneos diferentes y entre los cuales es imposible realizar una transfusión. Histograma: Los histogramas son gráficos que indican la frecuencia de un hecho mediante una distribución de los datos. Leishmaniasis: Enfermedad de la piel, mucosas y vísceras que afecta al hombre y animales Malaria: Es causada por un parásito que se transmite a los humanos a través de la picadura de mosquitos anofeles infectados. Plaquetas: Células sanguíneas que ayudan a prevenir el sangrado y ayudan cpn la coagulación de la sangre cuando los vasos se rompen. Plasma: Es la fracción líquida y acelular de la sangre. Se obtiene al dejar a la sangre desprovista de células como los glóbulos rojos y los glóbulos blancos. Reticulocito: Son glóbulos rojos que no han alcanzado su total madurez. Trombo aglutininas: Las aglutininas son globulinas de tipo gamma (gammaglobulinas), producidas por las mismas células que producen los anticuerpos frente a antígenos extraños. La mayor parte de las aglutininas son moléculas de inmunoglobulina de tipo IgM e IgG

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
JUSTIFICACION Se busca que el personal pueda familiarizarse con el equipo y pruebas realizadas en la sección de hematología mediante un acercamiento general y didáctico, con el ánimo de generar cohesión y linealidad en su entendimiento, para que se puedan solventar las dudas y puedan resolver asuntos relacionados con los procedimientos de rutina. El presente manual revisa las principales características del equipo de hematología y sus procedimientos, así como las pruebas realizadas y las alteraciones que se puedan presentar en el hemograma con el fin de generar una cultura unificada y generalizada en los operantes
MARCO TEORICO
La sangre es uno de los vehículos más importantes para el transporte de diferentes componentes como el oxígeno y los nutrientes que provienen desde el tracto gastrointestinal, además se encarga de mantener la homeostasis y participa en la defensa contra los agentes patógenos. El cuadro hemático es una de las pruebas más solicitadas en un laboratorio clínico, ya que aporta información importante sobre el estado de salud de una persona. El cuadro hemático o hemograma o biometría hemática se encarga de evaluar los diferentes elementos celulares que conforman la sangre como los glóbulos rojos, leucocitos, plaquetas, plasma y proteínas que en él se encuentren. El manual de hematología tiene como finalidad explicar el manejo del equipo usado para realizar el cuadro hemático automatizado, explicar los procedimientos, fundamentos de las diferentes pruebas realizadas en esta sección.
1. ANTICOAGULANTES
Se utilizan para mantener la sangre fluida. La mayoría de estas sustancias tienen la propiedad de remover o quelar el calcio presente en la sangre para de esta manera impedir que se dispare la cascada de coagulación y se coagule la sangre.
1.1 OXALATO DE AMONIO Y POTASIO
a. ACCION: Los oxalatos actúan sobre la sangre removiendo el calcio en forma de oxalatos de calcio insolubles. b. VENTAJAS Y DESVENTAJAS
Los oxalatos de potasio producen encogimiento de los eritrocitos haciéndolos disminuir su volumen. En cambio, el oxalato de amonio hace que los glóbulos rojos se ingurgiten o aumenten su tamaño.
Por esto no es conveniente utilizar aisladamente ninguno de estos anticoagulantes. La mezcla seca de oxalato de potasio y amonio es bastante buena, pues produce menos distorsión en el tamaño celular.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
1.2 CITRATO DE SODIO AL 3.8%
a. ACCION: Los citratos solubles actúan como anticoagulantes combinándose con el calcio, formando una sal de caldo
insoluble.
b. USO: Estudios de coagulación como: tiempo de protrombina (PT), tiempo parcial de Tromboplastina (PTT), Fibrinógeno, productos degradación del Fibrinógeno (PDF). También se puede utilizar para realizar la velocidad de sedimentación globular.
VSG por el método de Westergren.
Los oxalatos de potasio producen encogimiento de los eritrocitos haciéndolos disminuir su volumen. En cambio, el oxalato de amonio hace que los glóbulos rojos se ingurgiten o aumenten su tamaño.
Por esto no es conveniente utilizar aisladamente ninguno de estos anticoagulantes. La mezcla seca de oxalato de potasio y amonio es bastante buena, pues produce menos distorsión en el tamaño celular.
c. VENTAJAS Y DESVENTAJAS VENTAJA: Es una sustancia isotónica que evita la hemólisis y preserva los factores de la coagulación. DESVENTAJA: Diluye la sangre y por esto no se puede usar para la elaboración del cuadro hemático.
1.3 HEPARINA
a. ACCION: Actúa neutralizando la trombina, factor de gran actividad en el proceso de coagulación.
b. USOS: No altera el tamaño corpuscular de los glóbulos rojos. Reduce al máximo la posibilidad de hemólisis.
Se utiliza más que todo para hacer el estudio celular, fragilidad osmótica y para estudios genéticos.
1.4 EDTA (ETILEN DIAMINO TETRA ACETATO)
a. ACCION: Forma un complejo con el calcio presente en la sangre, impidiendo la coagulación de la muestra.
b. VENTAJAS: No distorsiona la morfología celular y evita la agregación y adhesión plaquetaria.
c. USOS: Es el anticoagulante ideal para la realización de un cuadro hemático para el recuento de plaquetas y la
realización de La VSG.
1.5 CPD o ACD (CITRATO FOSFATO DEXTROSA)
Es el anticoagulante usado en banco de sangre para la recolección de las unidades o bolsas de sangre.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Este anticoagulante, le proporciona todos los nutrientes a la sangre para su conservación en la nevera por espacio de un mes.
2. HEMATOLOGIA Y COAGULACION
2.1 HEMATOLOGIA
Se realizan los siguientes procedimientos.
Cuadro hemático automatizado
Velocidad de sedimentación globular
Recuento de reticulocitos
Extendido de sangre periférica
Hemoclasificación
Determinación del factor Rh
Leishmania
Gota gruesa TIPO DE MUESTRA: Sangre anticoagulada con EDTA, sangre capilar TOMA DE LA MUESTRA: Punción venosa, punción capilar
2.2 COAGULACION
Tiempo de protrombina
Tiempo parcial de tromboplastina activada
Tiempo de sangría
Tiempo de coagulación TIPO DE MUESTRA: Sangre anticoagulada con Citrato TOMA DE LA MUESTRA: Punción venosa Antes de procesar un cuadro hemático a partir de una muestra anticoagulada hay que mezclar bien la muestra por inversión del tubo varias veces. TRANSPORTE Y ALMACENAMIENTO DE LAS MUESTRAS: Máximo 24 horas a 4ºC.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
3. CUADRO HEMATICO AUTOMATIZADO Sin duda alguna el cuadro hemático (CH), es de las pruebas más solicitadas al laboratorio clínico como un perfil de exámenes relacionados con los diferentes elementos celulares en la sangre y seguimiento de entidades hematológicas como no hematológicas. El CH se basa en la determinación de hemoglobina, hematocrito, recuentos celulares, morfología globular, velocidad de sedimentación, e índices eritrocitarios secundarios. Para evaluar los anteriores parámetros, durante años se han desarrollado diferentes principios que le brindan al laboratorista mayor exactitud con los resultados, generando calidad y confianza tanto a la institución como al usuario. Entre estos principios se destaca la impedancia eléctrica, dispersión y absorción de luz; la primera se basa en la propiedad de las células de ser malas conductoras de electricidad, esto significa que si se establece corriente continua entre dos electrodos y al hacer vacío se hacer vacío se hace pasar a través de esta corriente una célula que se encuentra diluida en un solución isotónica, conductora y des particularizada, la mala conducción de electricidad de la célula hace que se produzca un aumento en la resistencia y se genere un impulso. Este impulso se traduce en un cambio de voltaje y su tamaño es proporcional al de la célula, así como el número total de pulsos contados es igual al número de células en la dilución.
3.1 EQUIPO HORIBA PENTRA XL 80
El Horiba Pentra 80 XL es un equipo que realiza cuadros hemáticos automatizados de cuarta generación y puede evaluar 26 parámetros (hemoglobina, hematocrito, recuento de eritrocitos, volumen corpuscular medio, hemoglobina corpuscular media, concentración de la hemoglobina corpuscular media, ancho de distribución de los eritrocitos, recuento total de leucocitos, recuento diferencial de leucocitos, recuento de plaquetas y morfología de sangre periférica por métodos electrónicos y manuales), puede procesar hasta 80 muestras por hora y solo usa 5 reactivos, incluyendo una opción libre de cianuro para la determinación de hemoglobina (lysebio). Utiliza un sistema automático de bandejas o racks, en los cuales caben hasta 10 muestras, y un sistema manual individual en los cuales se puede poner la muestra y enviar la orden de procesamiento, que puede ser CBC o DIFF. El sistema automático de racks solo procesa en modo DIFF.
3.1.1 PARTES DEL EQUIPO HORIBA PENTRA XL 80
VISTA FRONTAL

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
1. Cubierta de los reactivos: acceso a las botellas 2. Cargador de bandejas: capacidad para 10 bandejas de 10 tubos 3. Dispositivo de expulsión de bandejas: capacidad para 10 bandejas 4. Cubierta frontal izquierdo: permite acceder al sistema mecánico de carga de bandejas. 5- Compuerta del soporte de tubos: se abre al ejecutar un análisis manual. 6- Cubierta frontal derecho: permite acceder al sistema mecánico de expulsión de bandejas. VISTA LATERAL IZQUIERDA
1- Acceso a los reactivos: abra está cubierta para sustituir las botellas de reactivo. 2- Banco óptico: asegura el soporte y el ajuste de la célula de flujo, la lámpara y los elementos ópticos y electrónicos. 3- Dispositivo de la jeringa LMNE: – Asegura la proporción correcta de diluyente de parada en la cámara LMNE. – Inyecta la muestra en la célula de flujo. – Inyecta el flujo de la vaina interior y exterior en la célula de flujo. 4- Dispositivo de la jeringa de reactivos: – Asegura la proporción correcta de los reactivos: – Reactivo lisante para hemoglobina (ABX Lyse). – Reactivo de limpieza (ABX Cleaner). – Reactivo lisante para el recuento DIFF (ABX Eosinofix). – Diluyente para las diluciones (ABX Diluent) excepto el diluyente de parada LMNE. – Reactivo lisante para LEU/BASO (ABX Basolyse II). 5- Unidades de disquete y de CD VISTA LATERAL DERECHA

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
1- Jeringa de muestreo: toma de la muestra de sangre total y distribución de porciones de la muestra en las cámaras de dilución. 2- Dispositivo de recuento: – Recibe los diferentes aclarados y diluciones. – Regula la temperatura de las diluciones. – Proporciona las diluciones para LEU/BASO, ERI/PLA y HB. 3- Placa base: – Amplifica, procesa y cuenta las siguientes señales: – Señales de resistividad y señales ópticas LMNE. – Señal ERI y señal PLA. – Señales de LEU/BASO. – Mide la hemoglobina SOPORTE DE TUBOS PARA MODO MANUAL
1- Posición de muestreo 1: para tubos de 5 ml 2- Posición de muestreo 2: para tubos de 3 ml 3- Posición de muestreo 3: para controles/calibradores y material de látex

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
4- Posición de muestreo 4: para microcontenedores 5- Pilotos luminosos
– Cuando se enciende el piloto verde, el instrumento está listo para tomar muestras. – Cuando los dos pilotos parpadean alternativamente, el instrumento está ocupado tomando
muestras. – Cuando se enciende el piloto rojo, el instrumento está analizando.
VISTA POSTERIOR
1- Etiqueta con el número de serie 2- Entrada principal de la alimentación eléctrica 3- Conexiones para diluyentes y residuos 4- Conexión al equipo host 5- Conexión de la impresora BANDEJAS Las bandejas del Horiba Pentra 80 XL se identifican en el sistema mediante etiquetas con código de barras. Estas etiquetas deben colocarse en las bandejas del modo siguiente.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
3.1.2 INTRODUCCION AL SOFWARE
Horiba Pentra 80 XL incluye una estación de control principal, conformado por un computador integrado con pantalla táctil de 12 pulgadas y una resolución de 800 x 600.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
-La barra de herramientas contextual se encuentra en la parte inferior de la pantalla. -La barra de herramientas general se encuentra a la derecha. -Las teclas de acceso del menú principal se muestran en la parte central de la pantalla táctil. -Las teclas de puesta en marcha y lavado final también se muestran en la parte central de la pantalla táctil. DESCRIPCION DE LA BARRA DE HERRAMIENTAS CONTEXTUAL Esta barra se encuentra en la parte inferior de la pantalla y siempre contiene los mismos botones, independientemente del menú abierto.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
DESCRIPCION DE LA BARRA DE HERRAMIENTAS GENERAL A las teclas de funciones de la barra de herramientas general se accede desde la barra de herramientas situada en la parte derecha de la pantalla. Se trata de las teclas de funciones que se usan con más frecuencia a parte de las teclas principales que activan ciclos. DESCRIPCION DEL MENU PRINCIPAL Acceso a las principales funciones del sistema

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
MUESTRAS Se recomienda utilizar el anticoagulante K3EDTA con la proporción adecuada de sangre y anticoagulante indicada por el fabricante de los tubos. También se puede utilizar K2EDTA, siempre que la extracción de muestras se realice en condiciones normales. De lo contrario, pueden producirse coágulos de sangre.
3.1.3 MODOS DE OPERACIÓN DEL EQUIPO HORIBA PENTRA XL 80
MODO CBC

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
En el modo CBC, el sistema aspira 30 μl de sangre total y la transporta a las cámaras de la siguiente manera: Una parte de la muestra va a la cámara de dilución, que se utiliza para la dilución ERI/PLA y para medir la hemoglobina. La otra parte se utiliza para contar LEU/BASO.
MODO DIFF En el modo DIFF, el sistema aspira 53 μl de sangre total y la transporta a las cámaras de la siguiente manera: Una parte de la muestra va a la cámara de dilución, que se utiliza para la dilución ERI/PLA y para medir la hemoglobina. La segunda parte se utiliza para contar LEU/BASO. La última parte de la muestra se utiliza para la cámara LMNE, desde la cual la muestra pasa a la célula de flujo para el recuento de LMNE
3.1.4 ESPECIFICACIONES DEL EQUIPO
Tabla. Especificaciones generales del equipo HORIBA ABX PENTRA 80.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
PARÁMETRO DEFINICIÓN UNIDADES TIPO DE
MEDICIÓN
LEU Leucocitos 10³/uL IMPEDANCIA
LIN% Porcentaje de linfocitos % IMPEDANCIA ABSORCIÓN DE
LUZ LIN# Valor absoluto de linfocitos 10³/uL
MON% Porcentaje de Monocitos % IMPEDANCIA ABSORCIÓN DE
LUZ MON# Valor absoluto de Monocitos 10³/uL
NEU% Porcentaje de Neutrófilos % IMPEDANCIA ABSORCIÓN DE
LUZ NEU# Valor absoluto de Neutrófilos 10³/uL
EOS% Porcentaje de Eosinófilos % IMPEDANCIA ABSORCIÓN DE
LUZ EOS# Valor absoluto de Eosinófilos 10³/uL
BAS% Porcentaje de Basófilos % IMPEDANCIA ABSORCIÓN DE
LUZ BAS# Valor absoluto de Basófilos 10³/uL
LIC% Porcentaje de Células grandes
inmaduras % IMPEDANCIA
ABSORCIÓN DE LUZ LIC#
Valor absoluto de Células grandes inmaduras
10³/uL
ALY% Porcentaje de Linfocitos atípicos % IMPEDANCIA ABSORCIÓN DE
LUZ ALY# Valor absoluto de Linfocitos atípicos 10³/uL
ERI Eritrocitos 106/uL IMPEDANCIA
HB Concentración de hemoglobina g/dL FOTOMETRÍA
HCT Hematocrito % CALCULO
VCM Volumen Corpuscular Medio fL CALCULO
HCM Hemoglobina Corpuscular Media pg CALCULO
CHCM Concentración de Hemoglobina
Corpuscular Media g/dL CALCULO
IDE Índice de Distribución de Eritrocitos % CALCULO
PLA Plaquetas 10³/uL IMPEDANCIA
IDP Índice de Distribución de Plaquetas % CALCULO
VPM Volumen Plaquetar Medio fL CALCULO
PCT Plaquetocritos % CALCULO
3.1.5 PARAMETROS
Cada parámetro analizado en el equipo ABX Pentra 80 posee una forma específica de lectura, la cual se presenta a continuación:

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
ERI/PLA
Los ERI y las PLA se miden según el principio de variación de impedancia electrónica. Esto significa que se genera un campo electrónico alrededor de la microapertura en la cámara a través de la cual pasan las células sanguíneas. La muestra se diluye con un diluyente electrolítico (fluido conductor de corriente electrónica), que la agita y la pasa a través de la microapertura calibrada. A cada lado de la apertura hay dos electrodos entre los cuales no deja de pasar corriente eléctrica. A medida que las células sanguíneas pasan por la apertura, crean resistencia (impedancia) en el campo electrónico entre los dos electrodos. El voltaje que mide las células es proporcional al tamaño de la célula. Dado que la corriente es constante y no se modifica mientras más grande sea la célula, mayor resistencia tendrá. Mientras más pequeña sea la célula, menos resistencia tendrá. Estos voltajes electrónicos varían a medida que las células atraviesan la apertura. Los impulsos se amplifican, se canalizan según su tamaño y umbral, se agrupan, y luego se calculan matemáticamente junto con los coeficientes de calibración para conseguir un valor numérico final de ERI y PLA. Histogramas ERI: curvas de distribución en 256 canales de recuento comprendidos entre 30 fl y 300 fl. PLA: curvas de distribución en 256 canales comprendidos entre 2 fl y un umbral móvil. Este umbral varía de acuerdo con la población microcítica que existe en el área de análisis. - Interferencias ERI:
Eritrocitos aglutinados: pueden causar un recuento inferior de los ERI. Las muestras con esta condición pueden detectarse por sus elevados valores de HCM y CHCM, y comprobarse mediante su examen microscópico.
Aglutininas frías: las inmunoglobulinas M, cuyos valores son mayores en esta enfermedad, pueden disminuir el recuento de ERI y PLA e incrementar el VCM.
-Interferencias PLA:
Los eritrocitos muy pequeños (microcitos), los fragmentos de eritrocitos (esquistocitos) y los fragmentos de LEU pueden interferir en el recuento de plaquetas y causar recuentos elevados de las mismas.
Eritrocitos aglutinados: Pueden atrapar plaquetas y causar un recuento bajo erróneo de las mismas. La presencia de eritrocitos aglutinados puede detectarse observando los valores anormales de HCM y CHCM, y mediante un examen microscópico minucioso.
Un número excesivo de plaquetas gigantes: puede causar un recuento inferior e inexacto de plaquetas, puesto que estas plaquetas grandes pueden exceder el umbral superior del parámetro de plaquetas y no entrar en el recuento.
Quimioterapia: las drogas citotóxicas e inmunosupresoras pueden aumentar la fragilidad de estas células y disminuir los recuentos de PLA. Puede resultar necesario usar métodos de referencia (manuales) para obtener un recuento de plaquetas preciso.
Hemólisis: las muestras hemolizadas contienen estroma de eritrocitos, que puede incrementar los recuentos de plaquetas.
Sangre con A.C.D.: la sangre anticoagulada con ácido citrato-dextrosa puede contener agregados plaquetarios que pueden disminuir el recuento de plaquetas.
Una concentración elevada de lípidos y/o colesterol: puede interferir en el recuento correcto de plaquetas. En pacientes que están siendo sometidos a tratamiento parenteral con intralípidos, se ha informado de una sobreestimación en el recuento de plaquetas que puede ocultar una trombopenia.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
La bilirrubina elevada: puede interferir en el recuento correcto de plaquetas. En pacientes con graves trastornos hepáticos, hígado trasplantado, etc. se ha informado de una sobreestimación en el recuento de plaquetas que puede ocultar una trombopenia.
Aglutinación de plaquetas: los agregados plaquetarios pueden disminuir el recuento de plaquetas y/o incrementar el recuento de LEU. Debería volver a extraerse la muestra en citrato de sodio para asegurar la anticoagulación de la sangre dependiendo de la aglutinación, y volviendo a analizarla sólo para el recuento de plaquetas. El resultado PLA final debe corregirse por el efecto de dilución del citrato de sodio. No obstante, estos agregados plaquetarios provocan las alarmas L1, LL y LL1.
LEU Y DIFERENCIAL (LMNE)
El recuento de LEU se realiza dos veces según dos métodos de análisis distintos que utilizan el recuento de LEU total en ambas áreas:
En la cámara de recuento BAS a la vez que se realiza el recuento BAS.
En la cámara óptica a la vez que se realiza el recuento LMNE. El recuento de LEU de referencia es el que se obtiene en la cámara de recuento de LEU/BASO. LEU/BAS LEU: el número de células contado durante un tiempo determinado por volumen x coeficiente de LEU de calibración. BAS: el número de células contado durante un tiempo determinado por volumen x coeficiente de LEU de calibración como porcentaje del número total de leucocitos (basófilos y núcleos de LEU) El principio de medición es el mismo que para medir ERI/PLA. La diferenciación entre BASO y otros leucocitos se obtiene gracias a la acción lisante específica del reactivo ABX Basolyse II. -Interferencias LEU:
Leucocitos: los resultados de LEU que excedan los límites de linealidad del sistema requerirán una dilución de la muestra de sangre (muestra leucémica seguida de leucopenia). El reproceso de la muestra diluida permitirá obtener el valor del análisis correcto.
Eritrocitos no lisados: en casos excepcionales, los eritrocitos de la muestra de sangre no se lisan completamente. Estos eritrocitos no lisados aparecerán en el histograma de LEU con una alarma L1 o con una línea de base demasiado elevada en el lado correspondiente a la población linfocitaria. La existencia de eritrocitos no lisados provocará un elevado recuento de LEU falso.
Mieloma múltiple: la precipitación de proteínas en pacientes con mieloma múltiple puede generar recuentos de LEU elevados.
Leucemia: esta enfermedad puede generar un recuento de LEU muy bajo debido a una posible mayor fragilidad de los leucocitos, que puede provocar la destrucción de algunas de estas células durante el recuento. Estos fragmentos de glóbulos blancos también interferirán en los parámetros diferenciales de los glóbulos blancos.
Quimioterapia: las drogas citotóxicas e inmunosupresoras pueden aumentar la fragilidad de las membranas leucocitarias, que puede provocar recuentos LEU bajos.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Crioglobulinas: los niveles incrementados de crioglobulina que pueden estar asociados a mieloma, carcinoma, leucemia, macroglobulinemia, desórdenes linfoproliferativos, tumores metastásicos, desórdenes autoinmunes, infecciones, aneurisma, embarazo, fenómeno troboembólico, diabetes, etc., pueden incrementar los recuentos LEU, ERI o PLA y la concentración HB. La muestra debe calentarse al baño maría a 37ºC (99ºF) durante 30 minutos y volver a analizarla inmediatamente después (método automático o manual).
Macrotrombocitos: en excesiva cantidad pueden afectar y aumentar el número de leucocitos.
-Interferencias BAS
Un número excesivo de leucocitos (leucocitosis) puede provocar una subida artificial del recuento de basófilos debido a la desviación de la población de leucocitos en la zona de los basófilos.
Los monocitos y los blastos presentan gránulos mayores y pueden desplazarse al área de recuento de basófilos.
Un número anormalmente bajo de leucocitos (leucopenia) también puede aumentar los resultados relativos a los basófilos. Los elementos presentes en la zona de basófilos se recuperan en una pequeña cantidad total de leucocitos, lo que aumenta el error estadístico y genera variabilidades en el porcentaje.
La debilidad de las células leucocitarias en algunas enfermedades (leucemia linfática crónica) o durante el tratamiento frente al cáncer (quimioterapia) puede revertir en el canal basófilo durante la evaluación de los leucocitos debido a su destrucción, lo que aumenta las estadísticas de los basófilos.
La leucemia hace que los basófilos pierdan sus características citoquímicas y reaccionen anormalmente a los reactivos. La destrucción de los citoplasmas basófilos evita su diferenciación con los otros leucocitos.
Los basófilos de tamaño muy reducido (como consecuencia de los tratamientos) pueden interferir en el recuento de leucocitos dado que no es posible diferenciar los tamaños de las células.
Los basófilos anormales (como consecuencia de la desgranulación provocada por las alergias) pueden interferir en los recuentos de leucocitos porque los tamaños de células no pueden diferenciarse y porque pueden perder el material intracitoplásmico característico.
LMNE
Los recuentos de LEU y del diferencial en 5 partes en la célula de flujo se basan en 3 principios básicos:
El sistema hidrodinámico secuencial doble (DHSS) permite un flujo lineal de las células a través del haz de luz (patentado por HORIBA ABX).
El volumen de la célula se mide mediante la corriente eléctrica (cambios en la impedancia).
La medición de la luz transmitida con un ángulo de 0 aumentos permite una respuesta medida de acuerdo con la estructura interna de cada célula y su absorbancia, porque la luz no absorbida pasa a través de los espacios en el material nuclear de cada célula.
Se proporcionan 25 μl de sangre total a la cámara LMNE en un flujo tangencial de Eosinofix. Este reactivo lisa los ERI, estabiliza los LEU en sus formas originales y tiñe los núcleos de los eosinófilos con una coloración específica para medirlos en la matriz. La solución se estabiliza con

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
diluyente y se transfiere a la célula de flujo LMNE. Se miden la absorbancia (citoquímica) y los cambios en la impedancia de resistencia (volumen) de cada célula. A partir de la medición de la absorbancia y la resistividad de los leucocitos, se crea una matriz en la que aparecen los volúmenes de célula en el eje X y la transmisión óptica en el eje Y. El estudio de la imagen de la matriz permite diferenciar claramente 4 de las 5 poblaciones de leucocitos. Debido al escaso porcentaje de basófilos en comparación con el resto de leucocitos, se miden por separado en vez de incluirlos en la matriz.
Fig. Matriz LMNE
LIN: los linfocitos son células redondas muy pequeñas de citoplasma condensado y núcleo grande. Por su tamaño reducido, estas células suelen colocarse en la parte inferior del eje Y óptico y en la parte inferior del eje X de volumen. El extremo izquierdo del área de linfocitos (LL) debería estar vacía. La detección de las células en el área (LL) indica que hay linfocitos pequeños, agregados plaquetarios, eritroblastos (eritrocitos nucleados) y una alineación mal ajustada de la célula de flujo. También puede percibirse ruido de fondo en esta área si hay muchas interferencias. -Interferencias:
La presencia de eritroblastos, de algunos parásitos y de eritrocitos resistentes a la lisis puede interferir en la precisión del recuento de LIN.
Las limitaciones indicadas para el recuento de LEU también afectan a los recuentos de LIN# y LIN%.
MON: los monocitos son células muy grandes de forma irregular con núcleos muy complejos. El núcleo contiene capas y, a veces, vacuolas. El citoplasma también es grande y está compuesto por material intracelular no granulado. Estas células no se dispersan ni absorben gran cantidad de luz cuando pasan por la célula de flujo. Por lo tanto, se colocan en la parte inferior del eje Y óptico. Dado que los monocitos son células grandes, se colocan a la derecha en el eje X de volumen. -Interferencias:

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
La presencia de linfocitos grandes, de linfocitos atípicos, de blastos y una cantidad excesiva de basófilos puede interferir en la precisión del recuento de monocitos.
Las limitaciones indicadas para el recuento de LEU también afectan a los recuentos de MON# y MON%.
NEU: los neutrófilos son más grandes que los linfocitos. Los neutrófilos contienen material granular en el citoplasma y tienen un núcleo segmentado. Debido a estas características celulares, la luz atraviesa más estas células cuando pasan por la célula de flujo. Esto hace que los neutrófilos se coloquen más arriba en el eje Y óptico y que se distribuyan por el eje X de volumen en función de su grado de madurez. La hipersegmentación y el aumento de los gránulos colocan a estas células más arriba en el eje Y óptico. -Interferencias:
La presencia excesiva de eosinófilos, metamielocitos, mielocitos, promielocitos, blastos y plasmocitos puede interferir en la precisión del recuento de neutrófilos.
EOS: los eosinófilos son parecidos a los neutrófilos. Contienen material granular y núcleos segmentados en el citoplasma. El material granular se colorea con ABX Eosinofix antes de que los eosinófilos pasen por el haz de luz en la célula de flujo. Debido a la coloración del reactivo, los eosinófilos se colocan en la parte más alta del eje Y óptico. La Hipersegmentación y el aumento de los gránulos distribuyen esta población por la parte superior derecha de la matriz. -Interferencias:
La presencia de granulaciones anormales (áreas sin granulación, granulaciones tóxicas, etc.) puede interferir en el recuento de eosinófilos.
LIC y ALY
Las células inmaduras granulocíticas se detectan por su gran volumen y la presencia de más gránulos que aumentan la cantidad de luz que pasa por las células y la intensidad de la luz dispersada. Por consiguiente, las células como los metamielocitos se encontrarán a la derecha de los neutrófilos y casi al mismo nivel. Los mielocitos y los promielocitos aparecerán en posición de saturación en la parte extrema derecha de la matriz. Los metamielocitos, los mielocitos y los promielocitos se clasificarán como (LIC) y los resultados relacionados con ellos se incluirán en el valor de los neutrófilos. Normalmente, los blastos se situarán a la derecha de la población de monocitos y, por este motivo, incrementarán el recuento de LIC. Los blastos pequeños se encontrarán entre los linfocitos normales y las poblaciones de monocitos (ALY). El sistema genera un aviso de blastos cuando aumentan los recuentos dentro del área LIC, en relación con la detección de blastos en el histograma de basófilos. Los linfocitos grandes se detectan normalmente en la zona de los ALY, donde también se encuentran formas linfoides reactivas, linfocitos estimulados y plasmocitos. Los agregados plaquetarios y los restos de fragmentos de los eritrocitos se representan en el área de ruido de fondo situada en el ángulo inferior izquierdo de la matriz. La mayoría de los umbrales de población celular son fijos e indican los límites de la normalidad morfológica de los leucocitos. Los cambios en la morfología de una población concreta se expresarán en la matriz mediante un desplazamiento de la población correspondiente.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
HB
Durante el ciclo de análisis, el reactivo lisante se libera en la cámara de dilución. Alphalyse: Este reactivo rompe la membrana celular de los eritrocitos y libera hemoglobina en el interior de la célula. La hemoglobina liberada por el reactivo lisante se combina con el cianuro de potasio del reactivo lisante para formar un compuesto cromogénico de cianometahemoglobina. A continuación, se mide este compuesto en la parte óptica de la cámara de la primera dilución usando una técnica espectrofotométrica a una longitud de onda de 550 nm. Lysebio: Reactivo para la lisis de eritrocitos y la determinación sin cianuro de la hemoglobina. La adición del agente de lisis produce una liberación de hemoglobina. Todo el hierro hemínico se oxidiza y se estabiliza. Los complejos resultantes de la oxidación se cuantifican por espectrofotometría a una longitud de onda de 550 nm. -Interferencias:
Turbidez de la muestra de sangre: algunos factores fisiológicos y/o terapéuticos pueden incrementar los resultados de la HB. Para obtener resultados de HB precisos cuando existe una turbidez elevada en la muestra de sangre, se debe determinar las causas de esta turbidez y seguir el procedimiento adecuado entre los que se describen a continuación: Número alto de LEU: un valor de LEU muy alto causará una difracción excesiva de la luz. En estos casos, debe usar los métodos de referencia (manuales). La muestra diluida debería centrifugarse y el fluido sobrenadante debería medirse con un espectrofotómetro. Concentración elevada de lípidos: una concentración elevada de lípidos en la muestra de sangre dará al plasma un aspecto “lechoso”. Esto puede ocurrir en casos de hiperlipidemia, hiperproteinemia e hiperbilirrubinemia. Para obtener una determinación precisa de la hemoglobina debe usar métodos de referencia (manuales) y un blanco del plasma.
Turbidez elevada: puede aparecer en casos en que los eritrocitos son resistentes a la lisis. Esto puede conducir a un elevado resultado HB incorrecto, pero se puede detectar observando los valores anormales HCM, CHCM y la línea de base incrementada en el margen superior del histograma LEU. Si los resultados de hemoglobina son erróneos, provocará que los resultados de HCM y CHCM sean también incorrectos.
Sangres fetales: la mezcla de sangre materna y fetal puede producir valores altos y erróneos de la HB.
Todos los impulsos de los eritrocitos se agrupan por tamaños. Luego se calcula el promedio de altura de impulso de cada grupo. A continuación se calcula el promedio de todos los promedios de altura de impulso de eritrocitos. Esta función es una integración numérica de VCM. - Interferencias:
Aglutinación de eritrocitos: puede producir valores HCT y VCM erróneos. La aglutinación de glóbulos rojos puede detectarse observando los valores anormales HCM y MHCM, y mediante examen del frotis de sangre maculada. En estos casos puede resultar necesario usar métodos manuales para obtener un valor HCT preciso.
IDE
El IDE se utiliza para determinar anomalías en los eritrocitos relacionadas con la anisocitosis. El IDE permite al usuario realizar un seguimiento de la evolución de la anchura del histograma ERI en relación con el número y el volumen medio de células.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
El IDE es un cálculo derivado del histograma ERI.
Los cálculos son: IDE = (K x SD) / VCM
Donde: K = Sistema constante SD = Desviación estándar en función de los estudios estadísticos sobre la distribución de células dentro del histograma ERI. VCM = Volumen corpuscular medio de eritrocitos
-Interferencias:
Deficiencia nutricional o transfusión sanguínea: puede causar resultados del IDE elevados debidos a una deficiencia de hierro y/o de cobalamina y/o de folato.
VCM, HCM, CHCM
El VCM se calcula directamente a partir del histograma ERI completo.
La HCM se calcula a partir del valor HB y el recuento de ERI.
El peso medio de hemoglobina en cada ERI se calcula con la fórmula: HCM (pg) = HB/ERI x 10
El CHCM se calcula a partir de los valores ERI y HCT. La concentración ERI media en el volumen total de ERI se calcula con la fórmula:
CHCM (g/dl) = ERI/HCT x 100 -Interferencias:
Aglutinación de eritrocitos: puede producir valores de VCM erróneos. La aglutinación de eritrocitos puede detectarse observando los valores anormales de HCM y CHCM, y mediante su examen microscópico. En estos casos puede resultar necesario usar métodos manuales para obtener un valor de VCM preciso.
Un número excesivo de plaquetas grandes y/o un recuento de LEU demasiado elevado pueden interferir en la determinación exacta del valor del VCM. En estos casos, puede descubrirse el error mediante un examen microscópico minucioso.
El valor HCM se determina según el valor HB y el recuento ERI. Las limitaciones indicadas para HB y ERI tienen efecto en el valor HCM y pueden provocar valores inexactos.
El valor CHCM se determina según los valores HB y HCT. Las limitaciones indicadas para HB y HCT tienen efecto en el valor HCM y pueden provocar valores inexactos.
VPM: El VPM se deriva directamente del análisis de la curva de distribución de plaquetas. -Interferencias:
Las plaquetas gigantes que exceden el umbral máximo del parámetro de plaquetas pueden no ser contabilizadas como plaquetas. En consecuencia, estas plaquetas grandes no se incluirán en el cálculo del instrumento del volumen plaquetario medio.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Los eritrocitos muy pequeños (microcitos), los fragmentos de eritrocitos (esquisocitos) y los fragmentos de leucocitos pueden interferir en el recuento correcto de las plaquetas y en el cálculo de su tamaño.
Eritrocitos aglutinados: pueden atrapar plaquetas y causar un resultado incorrecto del VPM. La presencia de eritrocitos aglutinados puede detectarse observando los valores anormales de HCM y CHCM, y mediante un examen microscópico minucioso.
Quimioterapia: También puede afectar al cálculo del tamaño de las PLA.
Las muestras de sangre recogidas en EDTA no mantendrán un VPM estable. Las plaquetas recogidas en EDTA pueden aumentar su tamaño en función del tiempo transcurrido desde la extracción de la muestra y de la temperatura de conservación.
PCT: Los trombocitos se calculan usando la fórmula: PCT% = PLA (103/mm3) x VPM (μm3) /10.000 IDP: El IDP se calcula a partir del histograma PLA.
3.3.6 ESPECIFICACIONES DEL INSTRUMENTO
ABX PENTRA 80
Velocidad de procesamiento 80 muestras / hora
Volumen mínimo de muestra 53 µl
Relaciones de dilución
LEU/BAS 1/200
LMNE 1/80
ERI/PLA 1/10.000
HB 1/250
Medidas y cálculos
Impedancia para LEU, PLA, ERI, BAS
Fotometría para HB
Impedancia y absorción de luz para LIN, MON, NEU, EOS, ALY y LIC
Cálculos a partir de datos almacenados que se han medido para HCT, VCM, HCM, CHCM, IDE, VPM, PCT e
IDP
Diámetro de las aberturas de recuento
LEU/BAS 80 μm LMNE 60 μm
ERI/PLA 50 μm
Medida de la Hemoglobina
Cámara HB, LED 555 nm
Método Drabkin modificado (cianmethemoglobina)
Fuente de luz Diodo electroluminiscente
Longitud de onda 550 nm +/- 10 nm
Estadísticas y control de calidad
Paquete de control de calidad extendido.
Calibración Procedimiento de calibración automática
Introducción directa de los coeficientes de calibración

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Calibrador Minocal
Reactivos
Diluyente: ABX Diluent (20 o 10 litros)
Solución limpiadora: ABX Cleaner (1 litro, integrado)
ABX Eosinofix (1 litro, integrado)
ABX Basolyse II (1 litro, integrado)
Solución lisante: ABX Lyse (0,4 litros, integrado)
Residuos Eliminación automática
Tratamiento de residuos según las normas locales/nacionales
LINEALIDAD Límite de linealidad: valores máximo y mínimo dentro de los cuales el instrumento no genera ninguna alarma de dilución.
3.1.6 CONDICIONES GENERALES
Estabilidad mx: Las muestras pueden utilizarse en los 15 ó 20 minutos después de la extracción. Los resultados en todos los parámetros dependen del modo de conservación de la muestra. Estabilidad relativa de la muestra durante 48 horas a 4°C Agitación El modo de perforación de tapones ejecuta automáticamente un primer ciclo de agitación efectuando una rotación que dura aproximadamente 1 minuto. En el modo de tubo abierto, las muestras de sangre deberán mezclarse bien con cuidado inmediatamente antes de colocarlas en el soporte de tubos y cerrar la puerta del soporte de tubos. De este modo, se garantiza una mezcla homogénea para la medición.
3.1.7 INDICACIONES PARA EL PROCESAMIENTO DE MUESTRAS
ENCENDIDO

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
ENCENDIDO DEL EQUIPO ABX PENTRA XL80 CARGA Y ANALISIS DE BANDEJAS: MODO AUTOMATICO Previo a activar la función, aliste las muestras en las bandejas provistas con el Equipo
Oprimir Botón de encendido del equipo Pentra 80,
ingresar clave “abx”
Encender el computador qué conecta al equipo y abrir la
comunicación Interfaz smartcom ubicada en el escritorio
Esperar que le equipo realice análisis del sistema interno
del equipo
Oprimir botón verde del menú del equipo para realizar
una Puesta en marcha
Verificar el Blanco realizado con el equipo y
realizar el control de calidad

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
En el menú principal, identificar la opción “modo automático”
Haga clic sobre la opción para iniciar el modo automático. Inmediatamente, las bandejas que haya cargado con muestras empezaran a ser analizadas.
Dentro del equipo, se identificarán las muestras por medio del código de barras

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Serán mezcladas y analizadas.
MODO MANUAL La opción “botón test” ahorra reactivo en los análisis que requieren solo la determinación de parámetros eritrocitarios, en las cuales se usara el modo CBC. Si la muestra requiere recuento diferencial, se usará el modo DIFF, que realizará el recuento total y diferencial de leucocitos
Posterior a la elección del modo, se procederá a identificar la muestra.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Se coloca la muestra en el soporte de análisis manual
El resultado podrá verse en la pantalla
Cuando el Pentra 80 ha iniciado el proceso de análisis de un tubo de muestra, se generará una orden para buscar la lista de trabajo para 2 de los criterios siguientes:
El número de posición en la bandeja en que se ha colocado el tubo:
La ID de muestra del código de barras Cuando se encuentra la orden asociada, el instrumento realiza automáticamente el análisis solicitado, generado a partir de la información en la lista de trabajo, como el tipo de sangre definido y los datos demográficos del paciente asociado a cada muestra.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Identificación con código de barras El modo de identificación con código de barras es el más recomendado para el equipo Pentra 80 porque garantiza un nivel de seguridad y flexibilidad más alto. El código de barras permite asociar fácilmente órdenes de muestreo y tubos de muestras. El campo de ID de muestra corresponde a la etiqueta del código de barras.
3.1.8 REACTIVOS DEL EQUIPO
Los reactivos HORIBA ABX especificados para este instrumento han sido aprobados de conformidad con la directiva europea 98/79/CE (Anexo III) para dispositivos médicos in vitro. – Reactivo lisante para hemoglobina (ABX Lyse). – Reactivo de limpieza (ABX Cleaner). – Reactivo lisante para el recuento DIFF (ABX Eosinofix). – Diluyente para las diluciones (ABX Diluent) excepto el diluyente de parada LMNE. – Reactivo lisante para LEU/BASO (ABX Basolyse II). PROCEDIMIENTOS DE SUSTITUCION DE REACTIVOS 1- ABX Lyse 2- ABX Basolyse II 3- ABX Eosinofix 4- ABX Cleaner 5- ABX Diluent 6- Contenedor de residuos Cuando se pone en marcha el instrumento, el usuario debe comparar la cantidad que queda de cada reactivo con la carga de trabajo diaria definida. Si uno o varios reactivos alcanzan un nivel mínimo durante el día se generará una alarma y aparecerá una ventana de alarma con el siguiente mensaje

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Si aparece en pantalla la alarma de nivel bajo de reactivo, seleccione «Comprobar»
En la ventana Reactivo, seleccione el reactivo que desea reponer. Tras seleccionar el reactivo aparecerá la ventana siguiente
ABX EOSINOFIX

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Haga clic en el campo «Nº Lote» y use el lector de códigos de barras para actualizar algunas de las especificaciones del reactivo: número de lote, fecha de caducidad
Tras seleccionar «OK», el instrumento ceba automáticamente el reactivo
ABX EOSINOFIX

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
3.1.9 ALARMAS Y AVISOS DEL EQUIPO
Cuando el instrumento detecta un error o una alarma, estos aparecerán en la pantalla Alarma. Se activa el botón Alarma y parpadea AVISO DE SOSPECHA «!»:
Se puede generar un aviso de sospecha cuando se detectan anomalías en el recuento, posiblemente por patología, muestra coagulada, células plasmáticas.
Cuando existe una pobre correlación entre las mediciones ópticas y de resistividad en la matriz.
Cuando los recuentos de un determinado parámetro divergen más de los límites predefinidos.
AVISO NO: Significado: ruido de fondo (Background NOise).
Se genera este aviso cuando el número de partículas contadas en el área de ruido de fondo está por encima del límite definido en NO#, o cuando el número de partículas contadas frente al número total de LEU excede el límite NO%.
Anomalías posibles: Agregados plaquetarios, Gran número de plaquetas, membrana de eritrocitos resistente a la lisis (estroma), Eritroblastos, Contaminación.
AVISO LL: Significado: linfocitos izquierda (Left Lymphocytes). Presencia de una población significativamente grande en la parte izquierda del área de linfocitos.
Este aviso se genera cuando el número de partículas contadas está por encima del límite definido en LL#, o cuando el número de partículas contadas frente al número total de LEU excede el límite LL%.
Anomalías posibles: Linfocitos pequeños, Agregados plaquetarios, Eritroblastos, Membrana de eritrocitos resistente a la lisis (estroma),
Este aviso aparece con un (!) en: LIN% LIN#, NEU% NEU#, MON% MON#, EOS% EOS#, ALY% ALY#, LIC% LIC#

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO LL1: Significado: linfocitos a la izquierda 1 (Left Lymphocytes 1). Presencia de una población significativamente grande de células en la parte izquierda del área de linfocitos.
Se genera este aviso cuando el número de partículas contadas está por encima del límite definido en LL1# y cuando el número de partículas contadas en LL frente al número total de linfocitos excede el límite LL1%.
Anomalías posibles: Agregados plaquetarios, Eritroblastos, Membrana de eritrocitos resistente a la lisis (estroma), Estroma, Linfocitos anormales pequeños.
AVISO NL: Significado: Neutro/Linfo. Presencia de una población significativamente grande de células situada en la zona de umbrales de separación entre linfocitos y neutrófilos.
Se genera este aviso cuando el número de partículas contadas en esta zona está por encima del límite definido en NL#, o cuando el número de partículas contadas frente al número total de LEU excede el límite NL%.
Anomalías posibles: Neutrófilos pequeños sin gránulos y/o ligeramente segmentados, Linfocitos con núcleo segmentado o linfocitos activados, Neutrófilos con membrana débil
Este aviso aparece con un (!) en: LIN% LIN# y NEU% NEU#

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO MN: Significado: Mono/Neutro. Presencia de una población significativamente grande de células situada en la zona de umbrales de separación entre monocitos y neutrófilos.
Este aviso se genera cuando el número de partículas contadas en esta zona está por encima del límite definido en MN#, o cuando el número de partículas contadas MN frente al número total de LEU excede el límite MN%.
Anomalías posibles: Monocitos que tienen gránulos en su citoplasma o monocitos hiperbasofílicos, Neutrófilos jóvenes con núcleo no segmentado (bandas).
Este aviso aparece con un (!) en: ALY % ALY # y LIC % LIC # y sustituye: NEU% y #, MON% y # por «---»
AVISO LN: Significado: neutrófilos a la izquierda (Left Neutro). Presencia de una población significativamente grande de células en la parte izquierda del área de neutrófilos.
Se genera este aviso cuando el número de partículas contadas en esta área está por encima del límite definido en LN#, o cuando el número de partículas contadas frente al número total de LEU excede el límite LN%.
Anomalías posibles: Destrucción de neutrófilos a causa de una almacenamiento incorrecto de la muestra o porque la muestra es vieja, Contaminación, estroma o agregados plaquetarios.
Este aviso aparece con un (!) en todos los parámetros diferenciales de LEU.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO NE: Significado: Neutro/Eosino. Presencia de una población significativamente grande de células en el área que separa los neutrófilos y los eosinófilos a causa de una superposición de ambas poblaciones.
Se genera este aviso cuando el número de partículas contadas en esta área está por encima del límite definido en NE#, o cuando el número de partículas contadas frente al número total de LEU excede el límite NE%.
Anomalías posibles: Eosinófilos jóvenes, Neutrófilos hipersegmentados, Eosinófilos hipogranulares, Neutrófilos con granulaciones citotóxicas.
Este aviso aparece con un (!) en: LIC %LIC # y sustituye: NEU %, NEU #, EOS %, EOS # por «----»
AVISO RM: Significado: monocitos a la derecha (Right Mono). Presencia de una población significativamente grande de células en la parte derecha del área de monocitos (LIC bajo).
Este aviso se genera cuando el número de partículas contadas en esta área está por encima del límite definido en RM#, o cuando el número de partículas contadas frente al número total de LEU excede el límite RM%.
Anomalías posibles: Monocitos grandes, Monocitos hiperbasofílicos, Mielocitos o promielocitos, Blastos grandes.
Este aviso con un (!) en: NEU% NEU#, MON% MON#, LIC% LIC#.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO RN: Significado: neutrófilos a la derecha (Right Neutro). Presencia de una población significativamente grande de células en la parte derecha del área de neutrófilos (LIC alto).
Se genera este aviso cuando el número de partículas contadas en esta área está por encima del límite definido en RN#, o cuando el número de partículas contadas frente al número total de LEU excede el límite RN%.
Anomalías posibles: Neutrófilos grandes, Células inmaduras de hemopoyesis con granulocitos (metamielocitos, mielocitos, promielocitos).
Este aviso aparece con un (!) en: NEU% NEU#, LIC% LIC #.
AVISO LIC: Significado: Células inmaduras grandes (Large Immature Cells). Presencia de una población significativamente grande de células en las áreas RN + RM + canal 127.
Se genera este aviso cuando el número de partículas contadas en esta área está por encima del límite definido en LIC#, o cuando el número de partículas contadas frente al número total de LEU excede el límite LIC%.
Anomalías posibles: Monocitos grandes, Monocitos hiperbasofílicos, Mielocitos – metamielocitos – promielocitos, Blastos grandes, Neutrófilos grandes.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO ALY: Significado: linfocitos atípicos (Atypical Lymphocytes). Presencia de una población significativamente grande de células en la parte derecha del área de linfocitos.
Se genera este aviso cuando el número de partículas contadas en esta área está por encima del límite definido en ALY#, o cuando el número de partículas contadas frente al número total de LEU excede el límite ALY.
Anomalías posibles: Linfocitos grandes, Formas linfoides reactivas, Linfocitos estimulados, Plasmocitos.
AVISO EN EL HISTOGRAMA LEU/BAS:
El aviso L1 se establece basándose en la ratio de células contadas entre el canal 0 y BA1.
L1 indica la presencia de una cantidad anormal de células en comparación con los leucocitos.
Anomalías posibles: Agregados de PLA, Eritroblastos, El aviso L1 está asociado a (!) en el valor de LEU y a
valores absolutos de los parámetros diferenciales.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
AVISO EN EL HISTOGRAMA DE ERI:
Los avisos MIC y MAC se generan cuando el porcentaje de células contadas en el área microcítica (MIC) y macrocítica (MAC) supera el límite definido por el usuario para los porcentajes de MIC y MAC en comparación con el número total ERI.
Los umbrales ERI1 y ERI2 definen las áreas microcítica y macrocítica, y se calculan de acuerdo con el IDE y el VCM del histograma ERI.
AVISO EN EL HISTOGRAMA DE PLA:
El histograma PLA tiene 256 canales entre 2fl y 30fl. Existe un umbral (situado por defecto a 25fl) que varía de acuerdo con los ERI microcíticos presentes en el área de análisis de las plaquetas.
Los avisos PLA se generan bajo las siguientes condiciones:
Una presencia excesiva de partículas en la parte derecha del área del umbral (más de 25fl) generará el aviso MIC (microcitos), que aparecerá en el área de alarma de plaquetas. En este caso el umbral móvil busca un valle entre 18fl y 25fl (área estándar). Cuando este umbral no pueda situarse en el área estándar (entre 18fl y 25fl), se generarán un rechazo PLA (*) y un aviso MIC. El resultado PLA no será fiable. Compruebe el resultado usando Plasma Rico en Plaquetas (PRP) o un recuento de plaquetas manual.
Cuando no puede situarse el umbral (no existe valle entre los histogramas PLA y ERI), aparece el aviso SCH (esquisocitos, Sch). Anomalías posibles: Presencia de esquisocitos, Presencia de agregados PLA, Realice un examen microscópico periférico para comprobar la anomalía y confirmar los resultados. El aviso SCL (célula pequeña, Small Cell) indica la presencia de células pequeñas en las áreas 2 fl y 3 fl. Debe realizar un segundo análisis y comprobar el resultado.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
4. FROTIS DE SANGRE PERIFERICA
El diagnostico de muchas enfermedades hematológicas depende de la visualización morfológica de las células sanguíneas en un extendido de sangre periférica. Cada vez que se realiza el extendido de sangre periférica debe haber una mezcla de la muestra de sangre en forma suave, varias veces, tratando que los extendidos no queden muy gruesos ni muy delgados, para así obtener una distribución adecuada de las células sanguíneas en diferentes áreas del frotis y poder observar los eritrocitos en su tamaño, forma y color, así como realizar una buena fórmula leucocitaria o diferencial y una buena observación de plaquetas en su morfología y numero.
1) Homogenizar bien la sangre anticoagulada mediante 10 inversiones manuales.
2) Colocar una gota de sangre a 2 cm del borde esmerilado del portaobjetos
3) Colocar un segundo portaobjetos justo delante de la gota situada en la superficie del primer
portaobjetos, formando un ángulo de 45º y desplazarlo suavemente hacia atrás hasta que
alcance la gota de sangre
4) Esperar que, por capilaridad, toda la sangre se distribuya de forma uniforme
5) Deslizar suavemente y a velocidad moderada un portaobjetos sobre el otro en forma
longitudinal, hasta que la gota de sangre quede bien extendida sobre la superficie del
primer portaobjetos formando una fina película.
6) Dejar secar el extendido de sangre y colorear con colorante de Wright
Una buena extensión realizada mediante esta técnica debe tener entre 3 y 4 cm de longitud, un mínimo aceptable de 2,5 cm y presentar tres áreas de diferente grosor:
Zona gruesa o cabeza: se halla en la región inmediata al punto de partida de la
extensión. En ella siempre se aprecia un aumento del número de linfocitos.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Zona ideal o cuerpo: corresponde a la región situada entre la cabeza y la cola y en
ella existe un reparto equilibrado de las células
Zona fina o cola: corresponde al final de la extensión y termina en un área donde
las células adoptan una disposición acordonada. En esta región se observa un
exceso de granulocitos y monocitos.
Los defectos de una extensión pueden ser, la excesiva longitud y escaso grosor o viceversa, esto se presenta por un inadecuado tamaño de la gota de sangre, un error en la velocidad o a un fallo en el ángulo de extensión de la misma. Otro defecto del frotis puede ser la presencia de escalones o estrías ocasionado por la falta de uniformidad en el deslizamiento de la gota, la existencia de abundantes zonas redondas que carecen de sangre se debe a la presencia de restos de grasa o de suciedad en el portaobjetos.
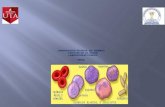
4.1 CARACTERISTICAS MORFOLOGICAS DE LOS GLOBULOS ROJOS
Los glóbulos rojos son células especializadas del cuerpo humano, que se encargan principalmente del transporte de oxígeno a todas las células, y la remoción del dióxido de carbono producto de la oxidación celular.
Entre las alteraciones del glóbulo rojo encontramos: alteraciones en la coloración, alteración en el tamaño y alteraciones en la morfología ALTERACIONES EN LA COLORACIÓN
Hipocromía: eritrocitos muy poco hemoglobinizados con un área exagerada de
palidez. Esta característica resulta del deterioro de la síntesis de hemoglobina.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Hipercromía: los eritrocitos son intensamente coloreados, estos pueden ser el
resultado de alteraciones en el grosor de la célula y disminución de la presión
central y no la concentración media de hemoglobina.
ALTERACIONES EN EL TAMAÑO
Anisocitosis: este término es utilizado para señalar las variaciones en el tamaño
de la célula, están presentes eritrocitos de varios tamaños en el mismo extendido
de sangre periférica.
Microcitos: es una disminución en el diámetro del eritrocito en relación al eritrocito
normal.
Macrocitos: los eritrocitos presentan un diámetro mayor al eritrocito normal.
Acantocitos: son eritrocitos contraídos y densos con múltiples proyecciones especuladas. Los acantocitos son frecuentes en dos trastornos constitucionales muy distintos: abetalipoproteinemia y anemia de células especuladas.
Estomatocito: es un eritrocito unicóncavo que presenta una depresión central alargada que en el extendido de sangre periférica le da el aspecto morfológico de boca o estoma.
Dianocitos: son eritrocitos en los que la palidez central presenta un área densa en su centro. Ello obedece al aumento de la superficie eritrocitaria con relación al volumen, generando una mayor proximidad entre las dos áreas bicóncavas de la membrana, con aumento local de la concentración de hemoglobina.
Equinocito: es un eritrocito que luce de menor tamaño, presentando elongaciones distribuidas regularmente en su superficie, por esta razón también son llamados células en erizo o crenocitos. Su forma característica se debe a un incremento del área externa de la capa bilipídica de la membrana de los eritrocitos con respecto a la interna.
Drepanocito: es un eritrocito con una forma sui generis, el cual se presenta como una célula alargada con extremos puntiagudos o espiculados que semejan una hoz o una media luna.
Dacriocito: es un eritrocito maduro que conserva la zona central pero que en vez de ser redondo adquiere una forma de gotera.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
4.2 CARACTERISTICAS MORFOLOGICAS DE LOS LEUCOCITOS
Neutrófilo: Es el 60-65 % de los leucocitos. Su diámetro está entre 10 y 14 micras. El citoplasma es ligeramente acidófilo, con granulaciones de carácter neutro, distribuidas en el citoplasma. El núcleo de color violeta oscuro y cromatina densa se caracteriza morfológicamente por presentar lóbulos fragmentados o separados entre sí, por puentes de cromatina.
Eosinofilos: es el 1-3 % de los leucocitos. Su diámetro es de 10-12 micras. El citoplasma repleto de granulaciones, constituidas por gránulos redondos y de gran tamaño, casi nunca cubren el núcleo; estos contienen sustancias de carácter básico, fijando colorantes ácidos como la eosina, dando un color pardo o anaranjado. El núcleo posee una coloración violeta, es bilobulado, forma masas simétricas unidas por uno de sus extremos. Basófilos: Su proporción, es inferior al 1% de los leucocitos. Su diámetro es de 12-14 micras. El citoplasma acidófilo, forma gránulos irregulares, fijando colorantes básicos como el azul de metileno. Las granulaciones, cubren el núcleo, el cual es de forma irregular con lobulaciones. Linfocito: Constituye el 20-40 % del total de los leucocitos, su diámetro es de 7-18 micras. El citoplasma es escaso o abundante; su coloración es azul pálida, debido a su Basofilia, que le confiere el contenido elevado de RNA, la granulación azurófila puede ser escasa y se encuentra en el citoplasma. El núcleo redondo, cromatina homogénea. Monocitos: Del 2-10 % del total de leucocitos; el diámetro es de 14-20 micras. El citoplasma es abundante y gris azulado: en ocasiones se halla vacuolado, con granulaciones finas azurófilas. El núcleo localizado en el centro, casi siempre es redondeado con invaginaciones, presentando variaciones dado su gran tamaño, ocupa gran parte del citoplasma y su cromatina es laxa, filamentosa e irregular, formando una trama reticular.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
4.3 CARACTERISTICAS MORFOLOGICAS DE LAS PLAQUETAS
Las plaquetas son fragmentos citoplasmáticos anucleados, no células como erróneamente se hace referencia a ellas, se producen como consecuencia de la ruptura y liberación del citoplasma de los megacariocitos de la médula ósea. Las plaquetas circulan en la sangre en forma de disco biconvexo (discocitos) de aproximadamente 3 μm de diámetro, un volumen (volumen medio plaquetario) de 8,3 a 11,6 fL y 10 pg de peso. Tienen una vida media en la sangre de 7 a 10 días y su concentración oscila entre 150.000 y 450.000 por μL. Entre las alteraciones de las plaquetas encontramos las siguientes situaciones:
Satelitismo plaquetario: las plaquetas se adhieren a otras células circulantes, en
particular a los polimorfo nucleares neutrófilos, a los monocitos y a los linfocitos.
Agregados plaquetarios: Son fenómenos que inducen la formación de agregados
plaquetarios.
Seudotrombocitopenia: es una falsa disminución en el número de plaquetas por
debajo del valor normal cuando su determinación se realiza con analizadores
automatizados. Su incidencia es de 0.09 a 0.21% en los enfermos hospitalizados.
Es secundaria a la agregación plaquetaria inducida por anticuerpos en presencia de
ácido etilendiaminotetracetico (EDTA). Se ha asociado a sepsis, fármacos,
neoplasias y cirugía cardiaca.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
5. RECUENTO DE RETICULOCITOS
PRINCIPIO
Los reticulocitos son eritrocitos no nucleados inmaduros que contienen ácido ribonucleico y que continúan sintetizando hemoglobina después de la pérdida del núcleo. Cuando la sangre se incuba brevemente en una solución de azul de metileno o azul de cresilo brillante recién elaborados, el RNA se precipita como un complejo colorante-ribonucleoproteína, que microscópicamente aparece como una malla (retículo) azul oscura o como gránulos de color azul que permiten identificar y contar los reticulocitos.
METODOLOGIA
A. MATERIALES
Reactivo de Azul de cresilo Brillante
Tubo de ensayo
Baño maría
Lámina portaobjetos
Microscopio Procedimiento
a. Mezclar en un tubo de ensayo 3 gotas del reactivo y 3 gotas de muestra (sangre total)
b. Mezclar suavemente c. Incubar durante 15 minutos en el baño maría a 37°C. d. Mezclar el tubo. e. Realizar extendido en la lámina portaobjeto. f. Dejar secar. g. Contar con objetivo de 100X (10 campos). Son de color azul pálido y contienen un
retículo o material granular azul oscuro y los hematíes se tiñen de color azul pálido o verde azulado.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
B. CALCULO DE RESULTADOS
Reticulocitos (%) = No. De reticulocitos * 100 1.000
Cuando una persona tiene una anemia (disminucion del recuento de hematíes, hemoglobina y hematocrito), el porcentaje de reticulocitos puede parecer elevado en comparación con el número total de hematíes. Esto se debe en parte a que se liberan células inmaduras precozmente desde la médula ósea hacia la circulación y a que tardan hasta tres o cuatro días en acabar de madurar. Para obtener una estimación más exacta del funcionalismo de la médula ósea, se corrige el porcentaje de reticulocitos, expresándose como IR; este índice compara el hematocrito de la persona evaluada con un valor normal de hematocrito.
C. INTERVALOS DE REFERENCIA Adultos: 0.5 – 2.0% Recién nacidos: 2.5 – 5.5% D. INTERFERENCIAS
Error en la toma de la muestra.
6 VELOCIDAD DE SEDIMENTACION GLOBULAR
PRINCIPIO
La velocidad de sedimentación globular es un reactante de fase aguda que indica presencia e intensidad de un proceso inflamatorio, aunque no es un método diagnóstico de una enfermedad específica. Este parámetro depende de la agregabilidad de los eritrocitos, puede aumentar cuando hay una elevación de la concentración plasmática del fibrinógeno o de otras proteínas asimétricas. FUNDAMENTO Cuando se coloca sangre venosa bien mezclada en un tubo vertical, los eritrocitos tenderán a caer hacia la parte inferior. La velocidad de sedimentación globular (VSG) es equivalente a la longitud del recorrido descendente de la parte superior de la columna de eritrocitos en un intervalo de tiempo determinado, y varios factores contribuyen a este valor.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
METODOLOGIA
A. MATERIALES
Pipetas de westergren
Soporte para tubos
Reloj Procedimiento a. Mezclar bien la sangre. b. Insertar la pipeta de Westergren en la muestra, hasta que la sangre llegue a la marca 0
mm. c. Poner el tubo en un soporte en posición vertical. e. Colocar en marcha el reloj y al cabo de una hora leer la velocidad de sedimentación.
Esquema. Velocidad de sedimentación globular-Método westergreen
B. INTERVALOS DE REFERENCIA Hombres: 0 – 15 mm/hr Mujeres: 0 – 20 mm/hr C. INTERFERENCIAS
Concentración de anticoagulante mayor del recomendado.
Presencia de burbujas en el tubo

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Inclinación del tubo
7 RECUENTO DE PLAQUETAS
PRINCIPIO
Es de mucha importancia en clínica, pues la trombocitopenia generalmente va asociada a deficiencia en sus funciones y produce trastornos en la coagulación. En ésta interviene; formando un verdadero tapón hemostático en el sitio de la lesión, adhiriéndose al endotelio lesionado, constituyendo una verdadera adhesividad plaquetaria y también formando fibrina suministrando una sustancia con actividad pro coagulante que se conoce como factor 3 plaquetario. Actúan en la coagulación sanguínea en la actividad del factor X y en la conversión de la protrombina en trombina.
METODOLOGIA
RECUENTO EN LÁMINA Realizar un extendido en lámina a partir de sangre anticoagulada con EDTA (con 5 µl de sangre), colorear con Wright y realizar el recuento con objetivo de 100X en un sitio donde los glóbulos rojos se toquen y exista depresión central en ellos. Se cuenta el número de plaquetas que hay en 10 campos, se saca el promedio de las plaquetas observadas por campo (sumar el número de plaquetas en todos los campos y se divide en 10) y se multiplica por 21.000. En recuentos de plaquetas con número disminuido se aconseja realizar mínimo dos láminas para confirmar o comparar con recuento en cámara. A. INTERVALOS DE REFERENCIA Normal: 150.000 – 450.000 mm3
B. ALTERACION DE LOS PARÁMETROS PLAQUETARIOS
ALTERACIONES CUANTITATIVAS a. Trombocitosis b. Trombocitopenia

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
ALTERACIONES CUANLITATIVAS a. Cambios en forma b. Cambios en tamaño
Plaquetas C. INTERFERENCIAS
Errores propios del operador de la prueba
Al realizar recuento en lámina; láminas demasiado delgadas o demasiado gruesa.
Defectos en la obtención de la muestra
Presencia elevada de plaquetas gigantes
Aglutinación plaquetaria EDTA-dependiente
Existencia de tromboaglutininas frías
8 HEMOCLASIFICACION
PRINCIPIO
La hemoclasificación se considera la reacción antígeno anticuerpo de mayor utilidad en el laboratorio de hematología. Esta prueba aprovecha las características inmunológicas que expresa cada individuo de acuerdo a su particular codificación genética. En dichas pruebas se evidencia los antígenos (Hemoclasificación Directa) y anticuerpos o aglutininas naturales

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
(Hemoclasificación Inversa) del grupo sanguíneo, de acuerdo a su comportamiento in-vitro.
METODOLOGIA
A. MATERIALES
Hemoclasificadores o antisueros anti A, anti B
Glóbulos rojos lavados al 5% de grupo A, B, O.
Solución salina al 0.85%
Láminas, Palillos, Pipetas Pasteur
HEMOCLASIFICACION DIRECTA
GRUPO A GRUPO B CONTROL
Glóbulos rojos paciente 1 gota 1 gota 1 gota
Suero Anti A 1 gota -------- --------
Suero Anti B -------- 1 gota --------
Solución salina0.85% -------- 1 gota 1 gota
Mezclar
Interpretación El paciente es grupo A: Si aglutina solo en el grupo A El paciente es grupo B: Si aglutina solo en el grupo B El paciente es grupo AB: Si aglutina en el grupo A y en el B El paciente es grupo O: Si aglutina en ningún grupo
B. INTERFERENCIAS
Inactividad de los antisueros.
Exceso de muestra produce fenómeno de prozona.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
9 DETERMINACION DEL FACTOR Rh
PRINCIPIO
Aproximadamente un 97% de la población es portadora del antígeno D, lo cual los clasifica como Rh positivos y el 3% restante de la población no posee este antígeno D en la membrana de sus glóbulos rojos por lo cual se catalogan como Rh negativos.
PREPARACION DE LOS REACTIVOS
Suero Anti D: Listo para su uso.
METODOLOGIA
A. MATERIALES
Glóbulos rojos del paciente
Suero Anti D.
Lámina de vidrio
Palillos
Procedimiento 1. Glóbulos rojos del paciente 1 gota 2. Suero anti D 1 gota 3. Mezclar y leer 4. B. INTERPRETACION DE RESULTADOS El paciente es Rh positivo: Si presenta aglutinación El paciente es Rh negativo: No presenta aglutinación NOTA: En el caso que con el anti D no haya aglutinación se debe hacer la prueba utilizando glóbulos rojos lavados y adicionarles el suero Anti CDE, para confirmar la ausencia o presencia de cualquiera de los otros antígenos del sistema Rh. Si después de este procedimiento el resultado sigue dando negativo se debe hacer la investigación de la variante Du. (También llamado Rh positivo débil). C. INTERFERENCIAS

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Reactivos vencidos
Errores propios del operador de la prueba Ejemplos .
10 . TEST DE COOMBS INDIRECTO
PRINCIPIO
Se le llama también prueba de la antiglobulina indirecta. Se utiliza para determinar la presencia de un anticuerpo Ig G incompleto que al unirse al antígeno celular correspondiente (hematíe) in vitro no es capaz de aglutinarlo directamente. Se necesita de la antiglobulina humana para conseguir la aglutinación y así comprobar la existencia del anticuerpo. Su principal uso radica en la detección de anticuerpos anti-D, Ig G incompletos, libres, en el plasma de una embarazada Rh negativo con posible riesgo de sensibilización.
METODOLOGIA
A. MATERIALES
Suero de Coombs
Sangre de la paciente sin anticoagulante (suero)

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Glóbulos rojos O+
Solución salina al 0.85%
Albumina Procedimiento
Agregar dos gotas de la solución salmón de Glóbulos Rojos O+ más dos gotas del
suero del paciente en un tubo de ensayo
Centrifugar
Agregar dos gotas de albumina
Llevar a baño María a 37°C durante 30 minutos
Centrifugar a 1000-2000rpm por 2 minutos y observar aglutinación
Realizar tres lavados, en el tercer lavado descartar la solución salina tanto como
sea posible, resuspender los hematíes sedimentados
Agregar dos gotas de Globulina anti humana de Coombs
Dejar el tubo en reposo durante 15 o 30 minutos
Centrifugar a 1000 rpm durante 2 minutos
Agitar el tubo cuidadosamente y observar si hay aglutinación
Se recomiendan los siguientes controles:
- Control negativo: 2 gotas de anti D + 2 gotas de suspensión de hematíes Rh negativos.
- Control positivo: 2 gotas de anti D (diluido 1:10 con s.s) + 2 gotas de la suspensión de hematíes Rh positivos.
B. INTERFERENCIAS Se pueden dar falsos positivos por contaminación bacteriana de la solución salina, hematíes y/o reactivos también. Por exceso de centrifugación. Y falsos negativos por lavado inadecuado, tiempos de incubación insuficientes, mal control de temperatura.
11 DETERMINACION DEL ANTIGENO Du
METODOLOGIA
Se realiza también un test de Coombs indirecto. 1. Se lava y se prepara la suspensión de hematíes, donde queremos detectar el antígeno
débil que hay que visualizar.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
2. En un tubo se adicionan 2 gotas de la suspensión de hematíes lavada + 2 gotas de anti D (reactivo).
3. Y seguir todos los pasos como en el caso anterior. La lectura será positiva si hay aglutinación por tanto el hematíe posee el antígeno investigado. Una persona que es Du positiva si va a actuar como donante, debe considerarse como Rh positiva, ya que aunque el Du sea débil puede sensibilizar a un Rh negativo; formando anti D. Si por el contrario va a recibir sangre, es preferible considerarla Rh negativa, con el objetivo de que ante un Du muy débil los hematíes donados si son D; estimulen el receptor creando anti D, por lo tanto es mejor trasfundirle hematíes Rh negativos.
12 TEST DE COOMBS DIRECTO
PRINCIPIO
Se le denomina también prueba de la aglutinación directa, sirve para ayudar al diagnóstico de cualquier anemia hemolítica de origen inmunitario. Detecta siempre anticuerpos pegados a la membrana del hematíe, nunca sueltos. El suero de antiglobulina humana (suero de coombs) empleado debe tener alta concentración de anti C3b, o anti C3d, ya que en algunas anemias hemolíticas autoinmunes el hematíe puede estar recubierto por fracciones del complemento activad (C3b, 3d).
METODOLOGIA
Procedimiento 1. Se lavan y se preparan los hematíes como en la técnica anterior 2. Se mezclan dos gotas de la suspensión de hematíes y dos gotas de antiglobulina
humana. Se sigue la técnica como el Test de Coombs indirecto desde el paso 6. Se aplica sobre todo en anemia hemolítica del recién nacido por anticuerpos anti D procedentes de la madre. Se realiza con la sangre del cordón del recién nacido.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
13 TIEMPO DE PROTROMBINA PT
TIPO DE MUESTRA: Sangre anticoagulada con citrato de sodio al 3.8% TOMA DE LA MUESTRA: Se realiza por punción venosa, no ha de ser traumática y debe realizarse con un mínimo de estasis circulatoria. Una extracción dificultosa puede activar la coagulación con consumo de factores. No debe utilizarse muestras capilares.
PRINCIPIO
Es la medida de la coagulación iniciada por el sistema extrínseco. El tiempo de protrombina se alarga por déficit de los factores I, II, V, VII y X. Esta prueba puede también utilizarse para controlar una terapéutica anticoagulante en paciente que reciban cumarínicos.
FUNDAMENTO
La prueba se realiza añadiendo una tromboplastina “completa” (hace el papel de la tromboplastina tisular) a sangre citratada, y efectuando una medida del tiempo de la coagulación tras la adición del Ca.
REACTIVOS Y MATERIALES
Plasma testigo normal
Mezcla de tromboplastina con cloruro de calcio.
Citrato de sodio al 3.8%
Cronómetro
Baño maría
MUESTRA
Plasma citratado en proporción 9 a 1.
METODOLOGIA
Procedimiento 1. Se centrifuga la sangre no coagulada a 2500 rpm, lo más rápido posible después de la
extracción.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
2. Se extrae el plasma y se coloca a temperatura ambiente no más de media hora. 3. Se pipetea 0.2 ml de la mezcla tromboplastínica cálcica en cada uno de los tubos
necesarios y se colocan al baño maría durante un minuto. 4. Se toma el plasma y se incuba 2 a 3 minutos, no debe dejarse en el baño maría más de
cinco minutos. 5. Se pipetea enérgicamente 0.1 de plasma del paciente en uno de los tubos que
contienen la mezcla de tromboplastina calcio y se pone en marcha el cronometro. Se mezcla el contenido del tubo, si esta operación se hace por agitación manual se extrae el tubo del baño maría, se seca la parte exterior y se agita suavemente de adelante hacia atrás, hasta que se forme el coagulo, momento en el cual se detendrá el cronometro. La visualización del coagulo también se puede realizar con la ayuda de un asa redonda de bacteriología.
A. INTERVALO DE REFERENCIA Normal: 10 – 14 segundos Terapia anticoagulante: 35 – 40 segundos B. MÉTODO DE CONTROL DE CALIDAD Se puede realizar con plasmas comerciales normales y/o patológicos. Si no se dispone de plasmas comerciales, se pueden emplear pool de plasmas de pacientes. C. INTERFERENCIA DEL MÉTODO
Material de vidrio rayado y/o con restos de suciedad
Temperatura inadecuada. No debe oscilar más de 0.5 grados centígrados
Anticoagulante diferente al citrato de sodio 3.8%.
No guardar la proporción sangre anticoagulante.
Falta de precisión al disparar el cronometro.
Tiempo prolongado de utilización del torniquete.
Hemólisis de las muestras.
Tiempo prolongado de separación del plasma. D. INTERPRETACION DE LOS RESULTADOS Hay déficit de protrombina y por consiguiente aumento en su tiempo, en la parahemofilia por falta del factor v o proacelerina, en la disminución del factor VII o proconvertina, en el déficit del factor xy en los casos de factores inhibidores de la coagulación, espontáneos o artificiales.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
14 TIEMPO DE TROMBOPLASTINA PARCIAL ACTIVADO (PTT)
TIPO DE MUESTRA: Sangre anticoagulada con citrato de sodio. TOMA DE LA MUESTRA: Punción venosa, con las mismas indicaciones que para el ítem anterior.
PRINCIPIO
Mide la actividad de la coagulación en la vía intrínseca. Sirve para el control de pacientes tratados con heparina y para detectar la presencia de inhibidores adquiridos. Utiliza un reactivo que se extrae con éter de cerebro humano y/o cerebro o pulmón de conejo. Este es un extracto fosfolipídico igual al factor tres plaquetario. Contiene un activador que puede ser caolín, celite, cefalina o sílice micronizada.
FUNDAMENTO
En la sangre el calcio es enlazado por el anticoagulante, l que impide la coagulación. Después de la centrifugación del plasma este contiene todos los factores intrínsecos de la coagulación, excepto el calcio y plaquetas. Se añade al plasma un sustituto o fosfolipídico de las plaquetas y calcio; el resultado del tiempo de tromboplastina parcial activado es el tiempo que tarda en coagular dicho plasma.
REACTIVOS
Cloruro calcio
Tromboplastina parcial.
Plasma testigo normal
MATERIALES
Baño maría
Cronómetro
Tubos de ensayo
MUESTRA
Plasma citratado.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
METODOLOGIA
Procedimiento 1. Se centrifuga la sangre sin coagular 2. Se separa el plasma y se tiene en refrigeración. 3. Se incuba una cantidad de cloruro de calcio 0.025 M a 37ºC. 4. Se pipetea 0.1 ml de plasma a un tubo y se añaden 0.1 ml de reactiva TTPA, se mezcla 5. A los 5 minutos añadir 0.1 ml de solución CaCl2 0.025 M 6. Poner en marcha el cronómetro, mezclar, esperar 20 segundos y determinar el tiempo
de coagulación.
INTERVALO DE REFERENCIA
Prueba mecánica: 27 – 39 segundos Prueba manual: 25 – 43 segundos
METODO DE CONTROL DE CALIDAD
Plasmas comerciales normal y anormal
INTERFERENCIAS DEL METODO
Material de vidrio rayado y/o con restos de suciedad.
Temperatura inadecuada. No debe oscilar más allá de 0.5 grados centígrados.
Anticoagulante diferente al citrato de sodio 3.8%.
No guardar la proporción sangre anticoagulante.
Falta de precisión al disparar el cronómetro.
Tiempo prolongado de utilización del torniquete.
Hemólisis de las muestras.
Tiempo prolongado de separación del plasma.
INTERPRETACION DE LOS RESULTADOS
Esta prueba permite valorar la normalidad o anormalidad de los factores I, II, V, VIII, IX, X y XII
15 LEISHMANIASIS CUTÁNEA (LC)
Las formas clínicas varían desde lesiones cerradas como pápulas, nódulos y placas que
pueden ser de aspecto verrugoso hasta las formas úlceradas. En Colombia la

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
presentación más frecuente es la úlcera indolora con compromiso linfangítico y adenopatía
regional.
La úlcera típica es redondeada, de bordes elevados, eritematosos, acordonados, con
centro granulómatoso limpio y base infiltrada. Regularmente son indoloras, de crecimiento
lento. Cuando hay sobreinfección bacteriana se tornan dolorosas, de fondo sucio,
secreción purulenta, recubiertas por costra de aspecto mielisérico, eritema periférico y
signos inflamatorios locales. Se pueden presentar como lesiones únicas o múltiples y
ocasionalmente como lesiones erisipeloides. La enfermedad puede tornarse crónica luego
de 12 semanas sin cierre de la úlcera o con la transformación de la misma en una placa
verrugosa de bordes elevados recubiertos con escamas y/o costras que coinciden con los
bordes de la cicatriz de la lesión inicial.
15.1 MÉTODOS DIAGNÓSTICOS EN LEISHMANIASIS CUTÁNEA (LC)
Ante la sospecha clínica de leishmaniasis es necesario visualizar el parásito para
corroborar el diagnóstico. Para ello existen diversos métodos.
Examen directo: El examen directo es un método rápido, económico y de fácil realización
en unidades de salud con recursos mínimos. Su sensibilidad varía de acuerdo con el
tiempo de evolución de la lesión (a menor tiempo de evolución mayor sensibilidad), la
técnica de la toma y coloración de la muestra, la capacitación del personal que realiza su
lectura y el interés que se tenga por parte de la entidad y de quien lee las láminas. En
general puede decirse que la sensibilidad del examen directo es de un 85% a 90%,
siempre y cuando el examen sea tomado de la manera adecuada. Se recomienda la toma
de más de una muestra de una misma lesión, tres preparaciones tanto del borde activo
como del centro de la úlcera, lo cual aumenta la sensibilidad. Las lesiones crónicas se
deben diagnosticar por aspirado. Si la úlcera presenta signos de sobre-infección
bacteriana, se debe administrar tratamiento antibiótico durante cinco días previo a la
realización del examen directo. No perder oportunidad cuando se tiene el paciente para la
toma de muestra si esta sobreinfectada. Si el paciente tiene lesiones múltiples se toma
muestra de la más reciente y si tiene lesiones satelitales tomas de esas.
EVOLUCION DE LAS LESIONES
MÁCULA
En el sitio de la picadura aparece
inicialmente una mácula.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
PÁPULA
La mácula evoluciona a pápula.
NÓDULO
La lesión continúa creciendo y se desarrolla
un nódulo. El nódulo es producido por la
masa dérmica que contiene macrófagos
vacuolados con abundantes parásitos de
Leishmania y un infiltrado linfocitario.
ÚLCERA Y CICATRIZ
Los nódulos crecen en tamaño y ocurre
necrosis en el centro de la reacción
granulomatosa, la cual es inducida por la
respuesta inmune, dando como resultado
una ulcera. Las úlceras crecen y se tornan
costrosas, redondeadas, con bordes
levantados y eritematosos, fondo limpio y
son indoloras. Por último, luego de
eliminado el parásito, ya sea porque la
respuesta inmune fue efectiva o por acción
del tratamiento específico contra
Leishmania, se inicia la resolución de la
lesión, dando lugar a la cicatrización.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Procedimiento:
-Con manos enguantadas realice limpieza del sitio de la lesión utilizando algodón
impregnado en alcohol o solución salina y jabón quirúrgico. Si hay costra remuévala
cuidadosamente.
-Sobre la cara interna del borde de la úlcera realice un raspado con el borde romo de una
lanceta o de una hoja de bisturí. Hágalo de manera tal que no sangre mucho.
-El material así obtenido se extiende en forma suave sobre una lámina portaobjetos
previamente limpiada, desengrasada y debidamente rotulada.
-Tome otras tres muestras de la misma manera colocando dos muestras por lámina en
dos láminas portaobjetos.
-Deje secar las muestras a temperatura ambiente.
-Tiña las láminas con colorante de Wright. Para evitar la formación de precipitados de
colorante es aconsejable realizar la tinción con las láminas invertidas sobre una superficie
que tenga el colorante.
-Observe al microscopio de luz con un aumento de 1000 X (objetivo de inmersión), para
buscar los amastigotes que pueden encontrarse intra o extracelularmente.
-Para identificar un amastigote como tal, debe observarse las formas ovaladas o
redondeadas características y distinguirse claramente el núcleo del cinetoplasto.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Interpretación:
Si dos exámenes directos tomando en cada uno dos láminas con dos muestras por lámina
son negativos, y persiste la sospecha clínica de leishmaniasis, debe practicarse biopsia.
La biopsia: es un procedimiento útil en el estudio de las leishmaniasis. Esta indicado
llevar a cabo, después de haberse realizado, en forma adecuada por lo menos tres
exámenes directos, cada uno con tres tomas y cuyo resultado haya sido negativo. Su
utilidad, además, radica en:
- Establece un diagnóstico concluyente al demostrar los parásitos.
- Determina otros procesos con los cuales se confunde la enfermedad clínicamente
- Sugiere el diagnóstico de leishmaniasis aún si los organismos no son demostrables por
microscopía
-Actualmente se puede procesar por métodos de detección de ADN parasitario con una
sensibilidad mayor a 70%.
Cultivo: Indicaciones de cultivo: Pacientes 3 exámenes directos negativos, prueba de
Montenegro reactiva y biopsia no conclusiva, pacientes procedentes de áreas no

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
caracterizadas epidemiológicamente (especie) y con menos de 6 meses de evolución y
pacientes con falla terapéutica.
16 DIAGNOSTICO MICROSCOPICO DE MALARIA
La malaria es una enfermedad ocasionada por un parásito del genero Plasmodium el cual
es transmitido por la hembra del mosquito Anopheles que a su vez ha sido infectada al
alimentarse con sangre de un paciente con gametocitos. Existen cinco especies que
ocasionan la enfermedad P. vivax, P. falciparum, P. malariae, P. ovale y P. knowlesi. Las
tres primeras especies ocasionan malaria en Colombia, sobre P. ovale se considera que
no hay transmisión en el país y sobre P. knowlesi se ha reportado trasmisión en el
continente asiático. Además de la transmisión por el vector, el Plasmodium también se
puede transmitir mediante transfusiones sanguíneas, contaminación accidental con
elementos cortopunzantes con sangre infectada o por vía congénita
Diagnóstico microscópico: Se trata de observar a través del microscopio las formas
parasitarias con las características propias de cada especie. Los estadios parasitarios que
se pueden observar son los asexuados (trofozoitos y esquizontes) y los sexuados
(gametocitos).
La gota gruesa es el examen de elección para confirmar o descartar la malaria, debido a
que es una muestra concentrada y deshemoglobinizada que permite revisar mayor
cantidad de sangre en una pequeña área con muestra, lo que la hace más sensible que el
extendido. Pueden existir casos en los cuales el paciente tenga una baja parasitemia y
cuente con una gota gruesa positiva y un extendido negativo. El extendido es utilizado
principalmente para aclarar dudas de especie o realizar recuentos cuando se presentan
altas parasitemias.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
En el diagnóstico microscópico es posible observar las características morfológicas de
cada especie y realizar el recuento parasitario. Sin embargo, solamente en el extendido es
posible evaluar las características del glóbulo rojo o célula huésped.
16.1 TOMA DE MUESTRA Y ELABORACION DE MUESTRAS
Gota gruesa:
Procedimiento para la toma de muestra y elaboración de la gota gruesa:
• Antes de proceder a la toma de muestra es necesario alistar la papelería o registros que
se lleven en el sitio de atención como pueden ser: registro diario y ficha de notificación,
según sea el caso.
• En un sitio limpio, ordenado, un mesón totalmente horizontal y con elementos de
bioseguridad haga la toma de muestra.
• En el lugar de toma de muestra se debe contar con láminas portaobjetos nuevas, limpias,
esmeriladas y con banda mate, lápiz o marcador de punta fina para marcar la lámina,
lancetas estériles, algodón, alcohol, guantes, guardián para desechar material
cortopunzante y caneca con bolsa roja. Si las láminas nuevas no las adquirió
desengrasadas, puede alistarlas poniéndolas sueltas sumergidas en alcohol antiséptico al
70% por 24 horas, después de lo cual se saca una a una y se secan con un trapo tipo
pañal el cual no suelta hilaza. Luego las arregla envueltas en papel craft por paquetes de
10 láminas. Los paquetes a su vez los puede guardar en una caja que tenga bolsas de
silica gel. Identifique los paquetes como laminas nuevas desengrasadas.
• Identifique las láminas.
• La toma de muestra idealmente debe hacerse por punción capilar debido que así se
obtienen las mejores preparaciones, sin embargo también es posible hacer el montaje de
las muestras con sangre tomada a partir de punción venosa utilizando anticoagulante.
• Las posibles zonas para la punción capilar son: el dedo índice o medio de la mano no
dominante, en el grueso artejo, o en el lóbulo de la oreja.
• Se desinfecta la zona de punción con alcohol antiséptico.
• La punción de hace de manera firme y segura.
• Se hace presión y se limpia la primera gota de sangre. Se empieza a trabajar a partir de
la segunda gota de sangre presionando hasta obtener una gota grande y globosa. Se
coloca la lámina por encima de la gota de sangre evitando tocar la incisión hecha con la
lanceta.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
• Es importante poder elaborar dos láminas por paciente siguiendo el esquema que se
muestra en la figura 3.
• Ayudado con otra lámina portaobjeto se extiende de manera adecuada la muestra de
sangre logrando un área aproximada de 1 cm x 1cm o de 1 cm x 1,5 cm. Ver figura 3. La
muestra debe quedar homogénea (para lo cual siempre se recomienda hacer movimientos
de vaivén). Se reconoce que la concentración de la muestra es adecuada porque al
extender la sangre debe ser suficiente para cubrir el área , es decir, no debe ser tan
escasa que quedan zonas sin sangre o por el contrario con exceso de muestra de tal
forma que después de homogeneizar sigue existiendo movimiento de la sangre.
• Una vez elaboradas las gotas gruesas se dejan secar a temperatura ambiente por 20
minutos, en un mesón horizontal y ordenado. Se debe proteger de los insectos cuando sea
necesario.
• Con las muestras elaboradas a partir de sangre anticoagulada es necesario tener un
especial cuidado en el secado, debido a que tienden a irse o lavarse durante el
procedimiento de coloración. Por lo tanto, se recomienda que después de secar la muestra
a temperatura ambiente, la lámina sea sometida a calor suave (37 °C) por un tiempo de 1
minuto y posteriormente dejarla enfriar muy bien para posteriormente proceder a
colorearla. No exceder el tiempo que se somete la muestra a calor debido a que la sangre
se fija a la lámina y posteriormente no es posible deshemoglobinizar la gota gruesa.
• Para finalizar la toma de muestra del paciente se limpia con algodón embebido en
alcohol en el sitio de punción para finalmente colocar una torunda de algodón seca en esta
zona. Pídale al paciente que sostenga el algodón en esta posición haciendo ligera presión.
• Para evitar la contaminación cruzada entre muestras de pacientes, se recomienda limpiar
con alcohol las láminas que se utilizaron para extender las gotas gruesas y el extendido
entre un paciente y otro. Es importante dejar secar el alcohol.
-Tiña las láminas con coloración de Field. Para evitar la formación de precipitados de
colorante es aconsejable realizar la tinción con las láminas invertidas sobre una superficie
que tenga el colorante.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
EXAMEN MICROSCOPICO DE LA MUESTRA
Realizar la observación microscópica en el objetivo de 100X.. La lectura de la muestra se
empieza a realizar en donde se observe un número adecuado de células sanguíneas,
teóricamente se deben observar entre 10 a 20 leucocitos, sin embargo, algunos pacientes
con bajo recuento de leucocitos pudiendo tener menos glóbulos blancos por campo. Para
iniciar la búsqueda de formas parasitarias, se mueve el carro del microscopio buscando
los campos adyacentes hasta llegar al extremo de la muestra, en donde se mueve el carro
de manera lateral para devolverse por una línea paralela a la ya observada. Es semejante
a un movimiento de zigzag.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
CARACTERISTICAS DEL CITOPLASMA DE LAS ESPECIES PARASITARIAS
LINEAMIENTOS NACIONALES PARA LA LECTURA DE LA GOTA GRUESA
Para considerar una muestra negativa se debe revisar como mínimo 200 campos.
Realizar el recuento con 200 leucocitos, de la siguiente manera:
Si hay menos de 100 parásitos en 200 leucocitos, hacer el recuento hasta 500 leucocitos
así:

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
Si la parasitemia es muy alta contar 500 parásitos y los leucocitos que haya encontrado,
usando la fórmula:
VERIFICACION DE LAS CONDICIONES ÓPTIMAS DE LAS MUESTRAS ANTES DE SU
PROCESAMIENTO Y ANALISIS.
1. Las muestras tomadas son dispuestas en la zona de proceso para su
procesamiento, allí se realiza las siguientes verificaciones:
En todas las muestras recibidas que se toman sin código de barras, se debe
comparar y verificar el nombre escrito en el tubo con el sticker del código del
paciente.
Tubos tapa lila: verificación de coágulos, volumen de la muestra (según
resultados)
Tubos tapa amarilla: se verifica la hemolisis (ausente), coágulos de fibrina
(ausente, volver a centrifugar) y volumen de muestra.
Tubos tapa azul: verificación de volumen de muestra, coágulos o hemolisis de la
misma (ausente)
Orina, materia fecal, esputo y demás líquidos, se realiza la verificación del
volumen de la muestra (si es muy poca el volumen de orina y el paciente no
puede orinar o es recolectada por sonda, se realiza la observación en el
resultado)
2. A continuación, se validan los resultados, para este proceso se debe tener en
cuenta los históricos de los pacientes y la verificación de los resultados (extendidos
de sangre periférica, la observación de las características de los sueros en el área
de química, etc.).
3. El manejo de los resultados críticos se debe realizar de la siguiente manera:
obtenido el resultado crítico se debe subir a la plataforma del Dropbox y de
inmediato se informa a la jefe del centro de salud correspondiente a la zonificación
del paciente en cuestión, para su respectivo manejo.

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
LISTA DE CHEQUEO MANUAL DE HEMATOLOGIA ISABU
Nombre del Profesional: ___________________________ Fecha: _________________________
TEMAS A EVALUAR SI NO OBSERVACIONES
1. El hemograma se basa en la determinación de hemoglobina, hematocrito, recuentos celulares, morfología globular, e índices eritrocitarios secundarios.
2. La sangre control consta de un control Interno Normal, Bajo y Alto con su respectivo número de lote, se debe mantener almacenados a 2 – 8 °C en la puerta de la nevera, y se debe guardar de manera horizontal en sus embalajes originales.
3. El Horiba Pentra 80 XL puede procesar hasta 80 muestras por hora y solo usa 5 reactivos, incluyendo una opción libre de cianuro para la determinación de hemoglobina (lysebio)
4. Las bandejas del Horiba Pentra 80 XL se identifican en el sistema mediante etiquetas con código de barras
5.Las muestras pueden utilizarse en los 15 ó 20
minutos después de la extracción
6. El modo de perforación de tapones ejecuta automáticamente un primer ciclo de agitación

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
efectuando una rotación que dura aproximadamente 1 minuto.
7. En el modo de tubo abierto, no es necesario mezclar las muestras.
8. si el equipo arroja una alarma LN neutrófilos a la izquierda (Left Neutro). Presencia de una población significativamente grande de células en la parte izquierda del área de neutrófilos.
9.Aproximadamente un 97% de la población es portadora del antígeno D, lo cual los clasifica como Rh Negativos y el 3% restante de la población no posee este antígeno D en la membrana de sus glóbulos rojos por lo cual se catalogan como Rh positivos.
10. La prueba de Coombs directo detecta siempre anticuerpos pegados a la membrana del hematíe, nunca sueltos.
ASPECTOS A MEJORAR _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ FIRMA DEL EVALUADO FIRMA DEL EVALUADOR ___________________________ _____________________________

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
17 BIBLIOGRAFIA
Ruiz Argüelles,Guillermo J.Fundamentos de hematología.4ta edición.Mexico: Medica
panamericana,2009.343p
Mitchell Lewis,Shirley;Bain,Barbara;Bates,Imelda.Fundamentos de hematología.10
edicion.España:Elsevier,2008.616p
Vives c,Joan Lluis;Aguilar B,Josep Lluis.Manual de técnicas de laboratorio en
hematología.3ra edición.España:Masson,2006.687p
Instituto Nacional de Salud, guía para la atención clínica e integral del paciente con
leishmaniasis. Convenio 256 de 2009 y numero 237 de 2010.-
Instituto Nacional de Salud,guía protocolo para la vigilancia en salud publica de
leishmaniasis.
http://soporteannardx.com/hesk2/knowledgebase.php?article=48(manual de usuario pentra
80)
https://www.policia.gov.co/sites/default/files/53-LEISHMANIASIS.pdf
http://www.ins.gov.co/temasdeinteres/Documentacin%20Malaria/01%20Protocolo%20Mala
ria.pdf
http://www.ins.gov.co/lineas-de-accion/Red-Nacional-
Laboratorios/Documentos%20de%20inters%20SRNL/Manual%20para%20el%20%20Diag
nostico%20de%20Malaria%20no%20complicada%20en%20puestos%20de%20diagn%C3
%B3stico%20y%20tratamiento%20%20ISBN%202015.pdf
http://www.wiener-
lab.com.ar/VademecumDocumentos/Vademecum%20espanol/soluplastin_sp.pdf
http://www.wiener-
lab.com.ar/VademecumDocumentos/Vademecum%20espanol/apttest_sp.pdf
http://www.wiener-
lab.com.ar/VademecumDocumentos/Vademecum%20espanol/anti_a_anti_b_anti_ab_mon
oclonal_sp.pdf

NIT 800.084.206-2
SISTEMA DE GESTION DE CALIDAD
MANUAL DE HEMATOLOGIA
CÓDIGO M-2007- 05
APOYO DIAGNOSTICO FECHA 28/10/2019
VERSIÓN 2.0
CONTROL DE CAMBIOS
CONTROL DE CAMBIOS
Versión Fecha Motivo del cambio Descripción del cambio
2.0 28/10/2019 Mejoramiento, levantamiento, diagnóstico Se realizan ajustes a las actividades según nuevas normas.
1.0 21/03/2018 Revisión y ajustes al Manual Criterio Manejo
D.E.D. 09/07/2009 Elaboración del Manul
ELABORÓ REVISÓ APROBÓ
Servidores Públicos del Proceso Equipo profesional oficina calidad Comité institucional de gestión y desempeño(CIGD) No.