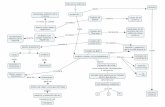
TEORIA ATÓMICA DE DALTON
-
Upload
casey-booth -
Category
Documents
-
view
42 -
download
0
description
Transcript of TEORIA ATÓMICA DE DALTON

TEORIA ATÓMICA DE TEORIA ATÓMICA DE DALTONDALTON
► Los elementos están formados por partículas
elementales extremadamente pequeñas llamadas
átomos. Todos los átomos de un mismo elemento son
idénticos y diferentes a los de otro elemento.
► Los compuestos están formados por átomos de más de
un elemento. En cualquier compuesto, la relación del
número de átomos entre 2 de los elementos presentes
siempre es un número entero o fracción sencilla.
► Una reacción química sólo implica la separación,
combinación o reordenamiento de los átomos; nunca
supone la creación o destrucción de los mismos.

Ley de las Proporciones Ley de las Proporciones DefinidasDefinidas
Ley de las Proporciones Ley de las Proporciones MúltiplesMúltiples
Ley de la conservación de la Ley de la conservación de la materiamateria
Muestras diferentes de un mismo compuesto siempre contienen los mismos elementos y en las mismas proporciones de masa.
Si dos elementos pueden combinarse para formar más de un compuesto, la masa de uno de los elementos que se combina con una masa fija del otro, mantiene una relación de números enteros pequeños.
La materia no se crea ni se destruye.

Masa Masa AtómicaAtómica
ELECTRONES
PROTONES
NEUTRONES
ÁTOMO Partículas extremadamente pequeñas.
Pero existen métodos experimentales para determinar su masa en relación con la de otro.
Masa Atómica
(Peso atómico)
Es la masa de un átomo, en unidades de masa atómica (uma).

Unidad de Masa Atómica
(uma)
Es una masa exactamente igual a un doceavo de la masa de un átomo de carbono – 12.
Carbono – 12Isótopo 6 protones
6 neutrones
12 uma12 uma
Por ej. se ha demostrado que un átomo de hidrógeno tiene sólo un 8.4 % de la masa del átomo de carbono:
0.084 x 12 uma = 1.008 uma

Masa Atómica Masa Atómica PromedioPromedio
La mayoría de los elementos de origen natural, tienen más de un ISÓTOPO.
Para la masa atómica de un elemento, hay que determinar la MASA PROMEDIO de la mezcla de los isótopos.
Por ej.
Carbono – 12 98.90 %
Carbono – 13 1.10 %
Masa atómica promedio = (0.9890 x 12) + (0.0110 x 13.0035)

Para el sistema internacional (SI)
MOLMOLEs la cantidad de una sustancia que contiene tantas unidades elementales (átomos, moléculas u otras partículas) como átomos hay exactamente en 12 g del isótopo de Carbono – 12
El número real de átomos en 12 g de carbono – 12 se determina experimentalmente
NÚMERO DE NÚMERO DE AVOGADROAVOGADRO
NNAANNAA = 6.0221367 X = 6.0221367 X
10102323

1 mol C – 12 = 12 g C – 12 = 6.022 x 101 mol C – 12 = 12 g C – 12 = 6.022 x 102323 átomos de C átomos de C – 12 – 12
Masa Molar
Es la masa (gramos o kilogramos) de 1 mol de unidades (como átomos o moléculas) de una sustancia
Masa Molecular
Peso Molecular
Es la suma de las masa atómicas (en uma) en una molécula.
Ej. H2O
(2 x 1.008) + 16.00 = 18.02 uma
1 mol H1 mol H22O = 18.02 g HO = 18.02 g H22O = 6.022 x 10O = 6.022 x 102323 moléculas de moléculas de HH22O O

6,022x10+23 át. 12C 1mol át. 12C
1 át. 12C x 1mol át. 12C x 12,00 g 12C = 1,993x10–23 g 12C
-23 12-24
12
g 1,993x10 g 1 át C g= x =1,661x10
UMA 1 át C 12 UMA UMA
1 UMA = 1,661x101 UMA = 1,661x10–24–24 g ó 1 g = 6,022x10 g ó 1 g = 6,022x10+23+23 UMA UMA
El número de AVOGADRO permite efectuar conversiones entre El número de AVOGADRO permite efectuar conversiones entre masa y moles de átomos mediante: masa y moles de átomos mediante:
+23
M de X 1 mol de X o
1 mol de X 6,022x10 át de X
PESO ATÓMICO (P.A.)PESO ATÓMICO (P.A.)

EjemploEjemplo: Cuantos moles de He están contenidos en 6,46 g de : Cuantos moles de He están contenidos en 6,46 g de gas noble.gas noble.
1 mol He6,46 g He x = 1,61 mol He
4,003 g He
g de Xmol de X =
P.A. de X
MASA MOLECULAR (M.M. O P.M.)MASA MOLECULAR (M.M. O P.M.)::
• Se define para un compuesto o molécula.Se define para un compuesto o molécula.
P.M. = P.A.

EjemploEjemplo: Calcular el peso molecular para la molécula de agua : Calcular el peso molecular para la molécula de agua (H(H22O).O).
2H O O H
gP.M. =P.A. +2xP.A. =18,02 UMA=18,02
mol
COMPOSICIÓN PORCENTUAL DE LOS COMPUESTOSCOMPOSICIÓN PORCENTUAL DE LOS COMPUESTOS::
• Composición porcentual en masa: Es el porcentaje en masa de Composición porcentual en masa: Es el porcentaje en masa de cada elemento presente en un compuesto.cada elemento presente en un compuesto.
elemento
compuesto
n x P.A.Composición Porcentual de un Elemento= x100%
P.M.
• n = número de moles del elemento contenidos en un mol de n = número de moles del elemento contenidos en un mol de compuesto.compuesto.

EjemploEjemplo: Determine la composición porcentual de H y O en peróxido de : Determine la composición porcentual de H y O en peróxido de hidrogeno.hidrogeno.
1 mol 1 mol moléculas Hmoléculas H22OO22
P.M.= 34,02 P.M.= 34,02 g/molg/mol
2 mol de átomos de H2 mol de átomos de H
2 mol de átomos de O2 mol de átomos de O
gmol
gmol
gmol
gmol
2x1,008%H= x100 = 5,926%
34,02
2x16,00%O= x100 = 94,06%
34,02
FORMULA EMPÍRICA Y FORMULA MOLECUALRFORMULA EMPÍRICA Y FORMULA MOLECUALR::
• Formula Empírica (F.E:): Relación numérica mínima entre los Formula Empírica (F.E:): Relación numérica mínima entre los átomos que conformar la molécula de un compuesto químico.átomos que conformar la molécula de un compuesto químico.
• Formula Molecular (F.M.): Relación exacta entre los átomos que Formula Molecular (F.M.): Relación exacta entre los átomos que conforman la molécula de un compuesto químico.conforman la molécula de un compuesto químico.
EjemploEjemplo: Peróxido de Hidrogeno: Peróxido de HidrogenoF.E.: HOF.E.: HO
F.M.: HF.M.: H22OO22

Porcentaje en masa Porcentaje en masa de cada elementode cada elemento
Cálculo de la masaCálculo de la masade cada elementode cada elemento
Cálculo de los molesCálculo de los molesde cada elementode cada elemento
Determinación de laDeterminación de laFórmula empíricaFórmula empírica
Considere unaConsidere unaMuestra de 100 gMuestra de 100 g
Con las masas Con las masas molaresmolares
Se determina Se determina la fracción la fracción
molar de cada molar de cada elementoelemento

• Determinación de Formula Empírica a Partir de la Composición Determinación de Formula Empírica a Partir de la Composición Porcentual:Porcentual:
40,92% C40,92% C
4,58% H4,58% H
54,50% O54,50% O
Ácido Ácido AscórbicoAscórbico
Elegir una base de Elegir una base de calculo de por calculo de por ejemplo 100 gejemplo 100 g
gmol
gmol
gmol
40,92 g Cmol C = = 3,407 mol C
12,01
4,58 g Hmol H = = 4,54 mol H
1,008
54,50 g Omol O = = 3,406 mol O
16,00
3,407 3,54 3,406C =1 H =1,33 O =1
3,406 3,406 3,406
Dividir por el más Dividir por el más pequeño:pequeño:
CC11HH1.331.33OO11
CC3,4073,407HH4,544,54OO3,4063,406

Búsqueda de un factor escalar para la formula:Búsqueda de un factor escalar para la formula:
1,33 x 1 = 1,33
1,33 x 2 = 2,66
1,33 x 3 = 3,99 4 CC11HH1,331,33OO11 / x 3 / x 3
CC33HH44OO33 F.E.F.E.
• Determinación de Formula Molecular a Partir de Formula Empírica:Determinación de Formula Molecular a Partir de Formula Empírica:
- Requiere conocer el P.M. aproximado y la F.E.Requiere conocer el P.M. aproximado y la F.E.
F.M. F.E.P.M. = n x P.M.
EjemploEjemplo: Ácido Ascórbico.: Ácido Ascórbico.
F.M.
F.E.
P.M.= 2
P.M.

EjemploEjemplo
► La alicina es el compuesto responsable del olor característico del ajo. Un La alicina es el compuesto responsable del olor característico del ajo. Un análisis del compuesto da la siguiente composición elemental porcentual análisis del compuesto da la siguiente composición elemental porcentual en masa: C = 44,4%; H = 6,21%, S = 39,5%; 0: 9,86%. Determine su en masa: C = 44,4%; H = 6,21%, S = 39,5%; 0: 9,86%. Determine su fórmula empírica fórmula empírica MM C = 12,0 g H = 1,0 g S = 32,0 g O = 16,0 gMM C = 12,0 g H = 1,0 g S = 32,0 g O = 16,0 g
Cálculo número de molesCálculo número de moles
R = CR = C66HH1010SS22OO
gmol
gmol
gmol
gm
44,4 g Cmol C = = 3,70 mol C / 0,62 = 6
12,01
6,21 g Hmol H = = 6,16 mol H / 0,62 = 10
1,008
39,50 g Hmol S = = 1,23 mol S / 0,62 = 2
32,00
9,86 g Omol O =
16,00 ol
= 0,62 mol O / 0,62 = 1