VACUNAS CONTRA MENINGITIS: · 2016. 8. 10. · hasta la muerte en 24 horas1,2 Morbilidad...
Transcript of VACUNAS CONTRA MENINGITIS: · 2016. 8. 10. · hasta la muerte en 24 horas1,2 Morbilidad...

MENINGOCO B MENINGOCOCO A,C,W ,Y
MENINGOCOCO C
VACUNAS CONTRA MENINGITIS: :

Bexsero® (vacuna meningocócica grupo B) 2013: autorización (Agencia Europea Medicamento)
Bexsero: Vacuna meningocócica del grupo B (ADNr, de componentes, adsorbida)
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA:
- Proteína recombinante de fusión NHBA de Neisseria meningitidis del grupo B.①
- Proteína recombinante NadA de N. meningitidis grupo B ②
- Proteína recombinante de fusión fHbp de N. meningitidis grupo B ③. Vesículas de la membrana externa (OMV) de N. meningitidis grupo B cepa NZ98/254 medidas como la cantidad total de proteína que contiene el PorA P1.4
① producida en células E. coli mediante tecnología de ADN recombinante
② adsorbida en hidróxido de aluminio (0,5 mg Al3+)
③ NHBA (antígeno de Neisseria de unión a heparina), NadA (adhesina A de Neisseria), fHbp (proteína de unión al factor H)

Aprobado uso a partir de los 2 meses de edad
Indicaciones terapéuticas (Ficha técnica- EMA)
Inmunización activa a partir de 2 meses de edad y mayores contra la enfermedad meningocócica invasiva por Neisseria meningitidis
serogrupo B.
Ficha Técnia de Bexsero®. Agosto 2014;

Situación de Bexsero en España 1 de Octubre de 2015
http://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/vacunas/2015/NI-MUH_23-2015-vacuna-bexsero.htm

Bexsero en España Financiación
Personas con deficiencia de properdina o con deficiencias de factores terminales
del complemento (incluyendo las que reciben o van a recibir eculizumab).
Personas con asplenia o disfunción esplénica grave (anemia de células
falciformes) y en resección quirúrgica programada.
Personas que han sufrido un episodio de EMI.(adenda 9-1-2015)*
Personal de laboratorio (técnicos y microbiólogos) que trabaje con muestras que
potencialmente puedan contener N. meningitidis
http://www.msssi.gob.es/profesionales/saludPublica/prevPromocion/vacunaciones/docs/MenB_situacEspeciales.pdf
http://www.msssi.gob.es/profesionales/saludPublica/prevPromocion/vacunaciones/docs/Adenda_MenB_situacEspeciales.pdf
* Cualquier paciente que haya sufrido una EMI sea cual
sea el serogrupo.

Pauta Vacunal

EJEMPLO DE CALENDARIO SEGÚN EDAD
| ATAGI | 12 October 2011 | Confidential 7

Neisseria meningitidis:
Diplococo gramnegativo encapsulado1
Patógeno exclusivamente humano1
Es común ser portador asintomático
• Prevalencia de portadores: ~1%–35%2
Transmisión3, 4
• Secreciones respiratorias
• Contacto directo
• Período incubación: 2 a 10 días
13 serogrupos
• A,B,C,W e Y provocan la
mayoría de casos
Tinción gram N. meningitidis en LCR. Flecha: células bacterianas absorbidas por un neutrófilo.5
1. van Deuren M, et al. Clin Microbiol Rev. 2000;13:144-166; 2. Brigham KS, et al. Curr Opin Pediatr. 2009;21:437-443; 3. Dull PM, et al. J Infect
Dis. 2005;1919:33-39; 4. WHO. Fact sheet: meningococcal meningitis. 2010; 5. Rosenstein NE, et al. N Engl J Med. 2001;344:1378-1388.
Enfermedad Meningocócica Invasiva

Niños y adolescentes: grupos de riesgo
Lactantes1-2
Población con una mayor incidencia (Aumento de 20 veces por encima de la media3)
Adolescentes4-6
Población con el mayor numero de portadores
(Aumento de 1,8 a 5,3 veces con respecto a los otros grupos de edad7)
Sistema inmunitario inmaduro
Reducción de los niveles de anticuerpos protectores maternos
Contacto cercano con casos
Hacinamiento: dormitorios, conciertos
Infecciones respiratorias
Fumar
Consumo de alcohol
Viajes
1.Rosenstein NE, et al. N Eng J Med. 2001;344:1378-1388; 2. Figueroa JE, et al. Clin Microbiol Rev. 1991;4:359-395; 3. European Centre for
Disease Prevention and Control (ECDC), Stockholm, Sweden, 2007; 4. Bilukha OO, et al. MMWR Recomm Rep. 2005;54:1-21; 5. Imrey PB, et al. J
Clin Microbiol. 1995;33:3133-3137; 6. Neal KR, et al. BMJ. 2000;320:846-849; 7. Christiansen H, et al. Lancet Infect Dis. 2010;10:853–61.
(En niños mayores, un aumento de 7 veces por encima de la media3)

Dificultad para diagnóstico correcto:
• 1º signos y síntomas: ≈ gripe o enfdes víricas comunes
Evolución rápida de enfermedad
• síntomas inespecíficos iniciales (fiebre e irritabilidad), hasta la muerte en 24 horas1,2
Morbilidad significativa a pesar de un tto:
• 20% de supervivientes presentan secuelas significativas 2,3
• ~1 de cada 10 niños que sobreviven a MenB: secuelas importantes4
• 1/3 de supervivientes a la MenB padecen deficiencias leves4
Mortalidad significativa a pesar de tratamiento: ~10%1,3
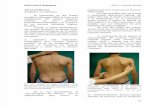
Enfermedad meningocócica tipo B: enfermedad grave y de evolución rápida
Imagen superior: Cortesía de los Centers for Disease Control and Prevention y del Dr Gust. Imagen inferior: Cortesía de la Meningitis Research Foundation UK. Disponible en: www.meningitis.org. 1. Thompson MJ, et al. Lancet. 2006;367:397-403; 2. Meningococcal meningitis factsheet No 141. World Health Organization website. www.who.int/mediacentre/factsheets/fs141/en/index.html; 3. Rosenstein NE, et al. N Engl J Med. 2001;344:1378-1388; 4. Viner RM, et al. Lancet Neurol. 2012;11:774-783.


Incidencia: enfermedad meningocócica invasiva Europa,* 2009
N = 4637.
*Países: Austria, Bélgica, República Checa, Dinamarca, Estonia, Finlandia, Francia, Alemania, Grecia, Hungría, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo, Malta, Países Bajos, Noruega, Polonia, Portugal, Rumania, Eslovaquia, Eslovenia, España, Suecia y Reino Unido. No se dispone de datos de Liechtenstein.
European Centre for Disease Prevention and Control. Surveillance of invasive bacterial diseases in Europe 2008/2009. Stockholm: ECDC; 2011.
Casos p
or
100.0
00
pers
on
as
del gru
po d
e e
dad
0
2
4
6
8
10
12
14
16
18
<1 1–4 5–9 10–14 15–19 20–24 25–44 45–64 ≥65
Edad (años)
Máxima incidencia: primeros 6 meses de edad

| Presentation Title | Presenter Name | Date | Subject | Business Use Only 13

| Presentation Title | Presenter Name | Date | Subject | Business Use Only 14 EXTREMADURA 2012-13: 3 CASOS

Cómo identificar los antígenos de la vacuna: VACUNOLOGÍA INVERSA: enfoque basado en el genoma para el desarrollo de vacunas
1. Tettelin H, et al. Science. 2000; 287:1809-1815; 2. Rappuoli R. Vaccine. 2001;19:2688-2691; 3. Pizza M, et al. Science. 2000; 287:1816-1820.
* · 3 proteínas y la adición de PorA
- La vacunología inversa
permite una
identificación rápida
de nuevos antígenos
candidatos a ser
vacuna.
- Se examinan
secuencias del
genoma.
- Se identifican
antígenos proteicos
potenciales.
- Se comprueban la
expresión en superficie
y la actividad
bactericida
-
Secuencia genómica
completa de
N. meningitidis
Análisis bioinformático Expresión proteica
en
Escherichia coli
Purificación proteica
e inmunización
Vacuna*
Confirmación de la
actividad bactericida
Candidatos finales seleccionados
para el desarrollo de la vacuna
Confirmación de la exposición en superficie

Inmunogenicidad en lactantes Pauta con dosis a los 2, 4, 6 y 12 meses con vacunas rutinarias
*Extracción de sangre a los 7 meses, N = 1149–1152. †Extracción de sangre a los 13 meses, N = 421–424. ‡N=100.
1. Vesikari T, et al. Presented at: 17th International Pathogenic Neisseria Conference (IPNC); 11-16 September 2010; Banff, Canada; Poster #180; 2. Vesikari T, et al. Presented at : 29th Annual Meeting of the European Society for Paediatric Infectious Disease (ESPID); 7-10 June 2011; The Hague, The Netherlands. Poster #749; 3. BEXSERO [summary of product characteristics]. 2014.
Fase III en lactantes Estudios V72P13 y V72P13E1 en
países de la UE
3 4 1
33
100 100
84 84 82
99
22
61
100 100 95
98
0
20
40
60
80
100
% d
e p
ers
on
as c
on
va
lore
s b
acte
ricid
as ≥
1:5
fHbp NadA PorA P1.4 NHBA‡
Valor inicial Primovacunacion (7 m)* Antes de dosis de recuerdo
(12 m)
Tras la dosis de recuerdo
(13 m)†

Inmunogenicidad en Adolescentes 2 dosis separadas por 1, 2 ó 6 meses
Phase IIb/III in Adolescents
Study V72P10 in Chile
Baseline1,2* BEXSERO 0-6§ BEXSERO 0-1† BEXSERO 0-2‡
44
34 35
88 100 100 100 100 100 100 100 100 100 99 100
0
20
40
60
80
100
fHbp1 NadA1 PorA P1.41 NHBA2,‖
NA
*N=1470–1471, fHpb, NadA, PorA P1.4 nivel base para todos los sujetos que recibieron la vacuna a momento 0; N=92, datos de NHBA del nivel base representados para los
grupos 0-1 y 0-2 ; †N=222; ‡N=215; §N=86; ║N=46.
Los datos mostrados son un mes tras finalizar la serie vacunal.
Una alta proporción de sujetos presentaban valores altos de títulos frente a los antígenos de referencia , puede ser debido a que fueran portadores nasofaringeos, sugestivo
de exposición ambiental.
1. Santolaya ME, et al. Lancet. 2012;379:617-624; 2. Data on file, Novartis Vaccines and Diagnostics.
% d
e p
ers
on
as c
on
va
lore
s b
acte
ricid
as ≥
1:4

Inmunogenicidad, eficacia y efectividad (AEP 2015)
Objetivo: estimular la producción de Ac bactericidas frente a Ag incluidos en la misma. Dada la amplia variabilidad entre las cepas de meningococo en la expresión de estos Ag superficie, el MATS (Meningococcal Antigen Typing System) relaciona los perfiles antigénicos de las cepas de meningococo B con el desarrollo de actividad bactericida del suero tras la vacuna.
2007-8: Estudio en Europa: en más de 1000 aislamientos de meningococo B:
73- 87 % de cepas aisladas tenían un perfil de MATS susceptible a la vacuna.
España: 300 aislamientos, resultados MATS: 68,7% (IC 95%: 48-85%)
Ensayos clínicos: es inmunógena, segura e induce memoria inmunológica en niños y adultos. La demostración de eficacia y efectividad en prevención de una enfermedad poco frecuente, (EIM por meningococo B), es complicada. Sólo la introducción en calendarios sistemáticos y el seguimiento epidemiológico permitirán evaluar la efectividad, en población vacunada y no vacunada.
18

EECC apoyan el uso concomitante con:
Uso concomitante con otras vacunas
Difteria
Tetanos
Acellular pertussis
Poliomielitis inactivada
Hepatitis B
Haemophilus influenzae tipo b
Pneumocócica heptavalente
conjugada
Sarampión
Paperas
Rubeola
Varicela

Uso concomitante: Buena respuesta inmunitaria para todos los antígenos
100 100 94 98 95 95 88 97 98 99 100 100 98 100 99 97 94 98 100 100 0
20
40
60
80
100
Difteria Tétanos Pertactina Tosferina FHA Polio 1 Polio 2 Polio 3 HBV PRP-Hib
% P
acie
nte
s c
on
re
sp
ue
sta
sé
rica
Antígenos
% ≥0,15
mcg/ml
% ≥10
mIU/ml % ≥1:8 % ≥0,1
IU/ml
% ≥0,1
IU/ml
-1%‡ (-5, 2)
-5% (-11, -1)
-1%‡ (-4, 2)
-4%‡ (-8, -1)
-2%‡ (-5, -1)
-4%‡ (-8, -1)
0%‡ (-1, 2)
0%‡ (-2, 2)
-2%‡ (-5, -1)
-1%‡ (-3, 1)
•Vacunas ordinarias: Infanrix®Hexa; Prevenar™. †n = 238–248. ‡ Se satisfacen los criterios LL en IC al 95% para la diferencia en pacientes con respuesta sérica > -10%. Extracción de sangre a los 7 meses.
•Vesikari T, et al. Presented at IPNC. Banff, Canada. September 11-16, 2010, Poster #180.
4CMenB más vacunas rutinarias*†
Únicamente vacunas rutinarias*†
Fase III en lactantes. Estudio V72P13 en países de la UE
% de pacientes con respuesta sérica a las vacunas rutinarias cuando
se les administra 4CMenB o la vacuna rutinaria sola a los 2, 4 y 6
meses de edad

0
20
40
60
80
100
Dolor en
lugar de
inyección
Eritema Induración Inflamación
% d
e la
cta
nte
s
Post–dosis 1*
2-4-6 BEXSERO1
3-5-7† PCV72
3-5-7† DTaP-HBV-IPV/Hib2
1. Gossger N, et al. JAMA. 2012;307:573-582; 2. Data on file, Novartis Vaccines and Diagnostics.
Tolerabilidad en lactantes Reacciones locales (Sólo Bexsero vs. vacunas rutinarias)
*No se observó incremento en la incidencia o severidad tras la administración de las siguientes dosis.
Las zonas rayadas muestran el porcentaje de las reacciones consideradas como graves (reacción was >50 o si el sujeto lloraba al mover la extremidad donde le habian vacunado)
Vacunas rutinarias: PCV7 i DTaP-HBV-IPV/Hib; BEXSERO: N=626; Rutinarias: N=613. Phase IIb in Infants
Study V72P12 in EU Countries

0
20
40
60
80
100
% d
e la
cta
nte
s
Cambio en
alimentación Somnolencia Vómitos Diarrea Irritabilidad Llanto
inusual
Sarpullido Fiebre
≥38°C
Rutinarias 3-5-7 †,2
BEXSERO 2-4-6†,1
Grave‡
*No se observó incremento en la incidencia o severidad tras la administración de las siguientes dosis. † Vacunas rutinarias: PCV7 i DTaP-HBV-IPV/Hib; BEXSERO: N=626–627; Rutinarias: N=612. ‡Fiebre categorizada como grave si la temperatura era ≥40°C. el resto de reacciones categorizadas como graves si el sujeto no podia realizar las actividades diarias normales.
1. Gossger N, et al. JAMA. 2012;307:573-582; 2. Data on file, Novartis Vaccines and Diagnostics. Phase IIb in Infants
Study V72P12 in EU Countries
Post–dosis 1*
Tolerabilidad en lactantes Reacciones sistémicas (Sólo Bexsero vs. vacunas rutinarias)

*No se observó incremento en la incidencia o severidad tras la administración de las siguientes dosis † Vacunas rutinarias: PCV7 i DTaP-HBV-IPV/Hib; BEXSERO+Routine: N=2478; MenC+Routine: N=490; Routine: N=659.
‡Fiebre categorizada como grave si la temperatura era ≥40°C. el resto de reacciones categorizadas como graves si el sujeto no podia realizar las actividades diarias normales.
0
20
40
60
80
100
Data on file, Novartis Vaccines and Diagnostics.
Rutinarias 2-4-6†
BEXSERO+Rutinarias 2-4-6†
MenC+Rutinarias 2-4-6†
Grave‡
Cambio en la
alimentación
Somnolencia Vómitos Diarrea Irritabilidad Llanto
inusual
Sarpullido Fiebre
≥38.5°C
% d
e la
cta
nte
s
Phase III in Infants
Study V72P13 in EU Countries
Post–dosis 1*
Tolerabilidad en lactantes Reacciones sistémicas (Uso concomitante Bexsero+Rutinarias)

Tolerabilidad: Patrón de fiebre La fiebre, generalmente siguió una patrón predecible, desapareciendo en la mayoría de casos el día siguiente a la vacunación
0
20
40
60
80
100
Tras la dosis 1*
(pauta de vacunación a los 2, 4 y 6 meses)
% d
e la
cta
nte
s
30 min 6 h Día 2 Día 3 Día 4 Tiempo
Se comunicó fiebre ≥ 40 °C tras cualquier dosis en el 1,2% de los lactantes a los que se administró Bexsero
*Se definió fiebre como una temperatura rectal ≥ 38,5 ºC. No se observó un aumento en la incidencia o la gravedad
de las reacciones adversas con las dosis posteriores de la pauta de vacunación. †Vacunas Rutinarias : PCV7 y DTaP-HBV-IPV/Hib; 4CMenB+ Rutinarias : N = 2433–2478; MenC+ Rutinarias : N = 486–490;
Únicamente Rutinarias : N = 643–659.
1. Vesikari T, et al. Accepted for publication. 2014; 2. Data on file, Novartis Vaccines and Diagnostics;
3. BEXSERO [summary of product characteristics]. 2012.
Fase III en lactantes
Estudio V72P13 en países de la UE
4C
Me
nB
+R
uti
na
ria†
Me
nC
+R
uti
na
ria†
Ru
tin
ari
a†
4C
Me
nB
+R
uti
na
ria†
Me
nC
+R
uti
na
ria†
Ru
tin
ari
a†

Administración conjunta de Bexsero y vacunas rutinarias con o sin paracetamol La profilaxis con paracetamol no influyó en la inmunogenicidad
4CMenB+rutinarias en los valores
iniciales*
La
cta
nte
s c
on
hS
BA
≥1
:5 (
%)
4CMenB+rutinarias+paracetamol en los valores
iniciales†
5 5 1 3 4
1
100 99
78
100 99
75
0
20
40
60
80
100
4CMenB+rutinarias1 mes después de la dosis final* 4CMenB+rutinarias+paracetamol 1 mes después de la dosis final†
fHbp NadA PorA P1.4
Fase II en lactantes
Estudio V72P16 en países
de la UE y de Latinoamérica
*N = 162–171; †N = 157–169.
Cada grupo vacunado siguió una pauta de vacunación acelerada a los 2, 3 y 4 meses.
Vacunas rutinarias: PCV7 y DTaP-HBV-IPV/Hib.
1. Prymula R, et al. Hum Vaccin Immmunother. 2014; 10 (7) (Epub) .

Perfil de Tolerabilidad
Vacunas rutinarias: PCV7 y DTaP-HBV-IPV/Hib
† Debe considerarse la vacunación por separado siempre que sea posible. Si fuera necesario administrarlo de forma simultánea con otras vacunas, deberá hacerse en zonas de inyección separadas.
BEXSERO Ficha técnica 2014.
Reacciones frecuentes
BEXSERO administrado sólo
BEXSERO junto con otras vacunas*,†
Lactantes
Dolor y eritema en el lugar de inyección, fiebre e irritabilidad
La frecuencia de fiebre fue similar a la
observada para las vacunas rutinarias*
Mayor frecuencia de fiebre y reacciones
sistémicas (irritabilidad,....)
Adolescentes
Reacciones adversas más comunes: dolor en el lugar de inyección, malestar y dolor de cabeza; la frecuencia de casos de fiebre fué similar a la del placebo

Conclusiones: BEXSERo: Primera vacuna de amplia cobertura frente al Meningococo B
El serogrupo B afecta principalmente a lactantes, puede ser mortal en 24 horas y provocar discapacidades graves para toda la vida a pesar del tto.
Vacunación: mejor prevención contra enfermedad agresiva que deja poco tiempo de intervención.
Bexsero : 1º vacuna contra el meningococo serogrupo B, autorizada para uso desde los 2 meses de edad.
EECC, Bexsero : respuesta inmunitaria protectora en lactantes, niños, adolescentes y adultos y puede administrarse de manera concomitante con vacunas rutinarias.
Resultados de coberturas de cepas en 9 países europeos, Australia, los EEUU, Brasil y Canadá en 2700 cepas de MenB: el 66- 91% quedarían cubiertas por Bexsero

Con los datos actualmente disponibles, el CAV-AEP recomienda:
1. Administrar la vacuna frente al meningococo B (Bexsero®) separada al resto de las vacunas inyectables de calendario,
pauta de 3, 5 y 7 meses o con un intervalo de, al menos, dos semanas respecto a las vacunas habituales.
2. Con esta pauta no necesario paracetamol profiláctico.
3. Dosis de refuerzo, en primovacunados en el primer año de vida: 13 -15 meses, para evitar coincidencia con vacuna meningococo C.
| ATAGI | 12 October 2011 | Confidential 28
DOSIS PARACETAMOL 10-15 MG/KG DE PESO
1ML=100MG C/ 4-6 HORAS