INSTITUTO POLITÉCNICO NACIONAL -...
Transcript of INSTITUTO POLITÉCNICO NACIONAL -...

INSTITUTO POLITÉCNICO NACIONAL
CENTRO DE BIOTECNOLOGÍA GENÓMICA
“DIAGNÓSTICO Y BIOCONTROL DE LA CAÍDA DEL FRUTO
PEQUEÑO DE LIMÓN DE TAMAULIPAS”
TESIS QUE PARA OBTENER EL TÍTULO DE
MAESTRO EN CIENCIAS DE BIOTECNOLOGÍA GENÓMICA
PRESENTA
I.B.Q. ELISEO TRUJILLO NEGRELLOS
REYNOSA, TAMAULIPAS DICIEMBRE, 2010

INSTITUTO POLITÉCNICO NACIONAL
CENTRO DE BIOTECNOLOGÍA GENÓMICA
“DIAGNÓSTICO Y BIOCONTROL DE LA CAÍDA DEL FRUTO
PEQUEÑO DE LIMÓN DE TAMAULIPAS”
TESIS QUE PARA OBTENER EL GRADO DE
MAESTRO EN CIENCIAS EN BIOTECNOLOGÍA GENÓMICA
PRESENTA:
IBQ. ELISEO TRUJILLO NEGRELLOS
REYNOSA, TAMAULIPAS DICIEMBRE, 2010



El presente trabajo se llevó a cabo en el Laboratorio de
Biotecnología Industrial del Centro de Biotecnología Genómica
del Instituto Politécnico Nacional, bajo la dirección de la Dra.
Claudia Patricia Larralde Corona, y fue financiado por los
proyectos FORDECyT/2RO/2009/08/06-07 (CONACyT) y por el
SIP2010-0928 del Instituto Politécnico Nacional.

ÍNDICE
LISTA DE CUADROS ........................................................................................................ I
LISTA DE FIGURAS ......................................................................................................... II
LISTA DE SIMBOLOS Y/O NOMENCLATURA ......................................................... IV
AGRADECIMIENTOS ..................................................................................................... V
DEDICATORIA ............................................................................................................... VI
RESUMEN ...................................................................................................................... VII
1. INTRODUCCIÓN .......................................................................................................... 9
2. ANTECEDENTES ....................................................................................................... 11
2.1 Los cítricos .............................................................................................................. 11
2.2 Hongos fitopatógenos en cítricos ............................................................................ 12
2.3 El género Colletotrichum ........................................................................................ 13
2.4 La Caída del Fruto Pequeño en cítricos .................................................................. 13
2.5 Sintomatología de la caída del fruto pequeño ......................................................... 14
2.6 Etiología de la caída del fruto pequeño ................................................................... 16
2.7 Variedad morfológica de Colletotrichum acutatum ............................................... 16
2.8 Epidemiología de la caída del fruto pequeño .......................................................... 17
2.9. Análisis moleculares para la identificación de hongos .......................................... 19
2.10 Control químico de hongos fitopatógenos ............................................................ 19
2.11 Control biológico de hongos fitopatógenos .......................................................... 20
2.11.1 Mecanismos de biocontrol ............................................................................. 21
Inducción de resistencia a la planta. ......................................................................... 21
2.12 Las levaduras como agentes de control biológico ................................................ 22
3. JUSTIFICACIÓN ......................................................................................................... 24
4. HIPÓTESIS................................................................................................................... 25
5. OBJETIVOS ................................................................................................................. 25
5.1. Objetivo general ..................................................................................................... 25
5.2. Objetivos particulares ............................................................................................ 25
6. MATERIALES Y MÉTODOS ..................................................................................... 26
6.1 Muestreo y aislamiento de hongos fitopatógenos ................................................... 26
6.2 Extracción de ADN fúngico.................................................................................... 28
6.3 Electroforesis en gel de agarosa .............................................................................. 28
6.4 Amplificación de regiones ribosomales .................................................................. 29
6.4.1Amplificacion de la región 26 S del rADN ...................................................... 29

6.4.2 Amplificación de la región ITS1..................................................................... 30
6.5 Purificación de productos de PCR .......................................................................... 30
6.6 Secuenciación ......................................................................................................... 30
6.7 Pruebas de patogenicidad por aspersión en hojas de limón ................................... 31
6.8 Pruebas de patogenicidad con taquetes de agar en hojas de limón ......................... 31
6.9 Pruebas de patogenicidad en flores de limón .......................................................... 31
6.10 Pruebas de antagonismo en placa ........................................................................ 32
6.11. Microscopia en campo claro ................................................................................ 33
6.12 Microscopia electrónica de barrido (SEM) ........................................................... 33
6.13. Análisis estadístico............................................................................................... 33
7. RESULTADOS............................................................................................................. 35
7.1 Análisis morfológico ............................................................................................... 35
7.2 Identificación molecular ......................................................................................... 38
7.2.1 Diferenciación molecular de especies del género Colletotrichum ................... 39
7.3 Pruebas de patogenicidad con hojas de limón con la prueba de taquete ................ 40
7.4 Visualización de la infección por microscopía electrónica de barrido ................... 41
7.5 Pruebas de antagonismo in vivo .............................................................................. 42
7.6. Pruebas de antagonismo in vitro ............................................................................ 44
7.7 Comprobación de los principios de Koch ............................................................... 48
8. DISCUSIÓN ................................................................................................................. 49
8.1 Diagnóstico de la caída del fruto pequeño .............................................................. 49
8.2 Análisis de patogenicidad ....................................................................................... 50
8.3 Pruebas de antagonismo .......................................................................................... 52
9. CONCLUSIONES: ....................................................................................................... 54
10. RECOMENDACIONES ............................................................................................. 55
11. BIBLIOGRAFÍA ........................................................................................................ 56
12. APÉNDICE ................................................................................................................. 61

I
LISTA DE CUADROS
Cuadro 1. Principales enfermedades de cítricos causados por hongos fitopatógenos ........... 12
Cuadro 2. Biofungicidas que contienen como materia activa bacterias o hongos
comercializados en diferentes países incluyendo los específicos para
cítricos (Fernández y Juncosa 2002) ................................................................... 22
Cuadro 3. Principales estudios realizados aplicando microorganismos antagonistas en
el control de hongos poscosecha in vitro e in vivo (Hernández Lauzardo
et al., 2007) ......................................................................................................... 23
Cuadro 4. Esquema de muestreo y localización de los puntos en los huertos de
limones 6 y 7, ubicados en Nuevo Padilla, Tamaulipas...................................... 27
Cuadro 5. Identificación morfológica y molecular de hongos filamentosos
intracelulares obtenidos en Citrus limon, clasificados de acuerdo al punto
de muestreo y material vegetal de origen............................................................ 35
Cuadro 6. Velocidad de crecimiento radial de los aislamientos pertenecientes a los
géneros Colletotrichum y Glomerella obtenidos de los tejidos de Citrus
limon.................................................................................................................... 37
Cuadro 7. Relación de patogenicidad de los géneros de hongos aislados en los
huertos de cítricos de Nuevo Padilla Tamaulipas ............................................... 41
Cuadro 8. Porcentaje de inhibición de fitopatógenos en pruebas de antagonismo in
vitro. .................................................................................................................... 45
Cuadro 9. Prueba cualitativa de protección con levaduras antagonistas y el
aislamiento Colletotrichum CF-6. ....................................................................... 47
Cuadro 10. Análisis de varianza para la variable crecimiento radial, diseño
completamente al azar con un nivel de confianza del 95%. ............................... 61
Cuadro 11. Comparación de medias del radio de la colonia a los 6 días por el método
de Tukey. ............................................................................................................. 61
Cuadro 12. Análisis estadístico no paramétrico para la relación de patogenicidad por
la prueba de Kruskal-Wallis de una vía ............................................................. 62
Cuadro 13. Comparación de múltiples por pares mediante el procedimiento de Dunn ........ 63
Cuadro 14. Porcentaje de identidad de los aislados fúngicos de Citrus limon en base a
la secuenciación de su región D1/D2 (26S). ....................................................... 67
Cuadro 15. Secuencias del 26 S de los aislamientos de los hongos intracelulares de
Citrus limon en tejidos con síntomas de infección tipo caída del fruto
pequeño. .............................................................................................................. 69

II
LISTA DE FIGURAS
Figura 1. Síntomas en frutos de limón mexicano causado por Colletotrichum
acutatum. Fotografía tomada de Orozco-Santos y Timmer (2005). ...................... 15
Figura 2. Características morfológicas de crecimiento de micelio, conidios y
síntomas en la flor del limón, causado por Colletotrichum acutatum, CFP
(PFD por sus siglas en inglés). Fotografías tomada de Orozco-Santos y
Timmer (2005). ...................................................................................................... 17
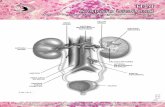
Figura 3. Ciclo de vida e infección de Colletotrichum acutatum. Dibujo tomado de
Orozco-Santos y Timmer (2005). .......................................................................... 18
Figura 4. Posición de los iniciadores utilizados para la amplificación de los genes
ribosomales utilizados en la identificación de hongos (tomado de
Rodríguez et al., 2004). .......................................................................................... 19
Figura 5. Lesiones en hojas y frutos de limón italiano de Tamaulipas, A) Hojas
senescentes con síntomas de crecimientos de hongos B) Limones secos
que no se desarrollaron C) Cálices que quedaron sin el fruto (tachuelas). ............ 26
Figura 6. Crecimiento de micelio de aislados de los géneros
Colletotrichum/Glomerella obtenidos de tejidos de limón italiano con
síntomas de CFP. A) Colletotrichum CF-16, B) Glomerella CF-11 C)
Conidios de Colletotrichum CF-6, y D) Colonia de Colletotrichum CF-6
100X. ...................................................................................................................... 36
Figura 7. Morfología colonial macroscópica de los aislamientos obtenidos en las
muestras de tejidos infectados en limón italiano de Nuevo Padilla
Tamaulipas. ............................................................................................................ 37
Figura 8. Gel de agarosa al 1% para visualizar los productos de PCR de la
amplificación de la región 26S de 17 muestras y dos testigos, uno
negativo y otro positivo. Con un marcador de 1500 pares de bases. ..................... 38
Figura 9. Gel de agarosa al 1% donde se muestra la amplificación selectiva de un
fragmento específico del 26S utilizando los oligonucleótidos: A) CaInt2,
específico para C. gleosporioides, y B) CgInt, específico para C.
acutatum. La columna M es el tamaño del marcador molecular de 1000
pb. ........................................................................................................................... 40
Figura 10. Fotografías de microscopía electrónica de barrido del crecimiento de
micelio en superficie herida de la hoja de limón a los 6 días, izquierda)
Glomerella CF-14, derecha) Glomerella CF-11. ................................................... 42

III
Figura 11. Fotografías de microscopia electrónica de barrido del crecimiento de
micelio en superficie de una hoja de limón a los 6 días a) Glomerella CF-
39, b) Glomerella CF-12, y c) Glomerella CF-14. .............................................. 43
Figura 12. Fotografías de microscopia electrónica de barrido de comparación de la
densidad del crecimiento micelial sobre las heridas en una hoja de limón
de dos aislados y un testigo a los 6 días a) C. acutatum b) Glomerella
CF-11, c) Glomerella CF-14. ................................................................................. 43
Figura 13. Confrontación en placa con la levadura LCBG-03 contra: A) Glomerella
CF-14, B) Glomerella CF-8, y C) Colleotrichum CF-6. ........................................ 44
Figura 14. Prueba de supervivencia de flores de limón de Tamaulipas en agua estéril
por 6 días, donde las flores se mantienen en buen estado después del
tiempo de prueba, no hay lesiones en las estructuras florales como se
puede observar en la imagen. ................................................................................. 46
Figura 15. Prueba cualitativa de antagonismo entre levaduras y hongos en flores de
limones a las 72 h de inoculación. ......................................................................... 47
Figura 16. Comprobación de infección yreaislamiento del patógeno inoculado en la
prueba con flores de limón. Se observa el crecimiento abundante y con el
color salmón típico de Colletotrichum. .................................................................. 48

IV
LISTA DE SIMBOLOS Y/O NOMENCLATURA
A Adenina
ADN Ácido desoxirribonucléico
pb Pares de bases
C Citosina
CFP Caída del Fruto Pequeño
dNTPs Mezcla de trifosfatos de desoxinucleótidos (dATP + dGTP + dCTP +
dTTP)
EDTA Sal disódica del ácido etilendiaminotetraacético
FAO Organización de las Naciones Unidas para la Agricultura y la
Alimentación
FGG Fast Growing Gray, la forma gris y de crecimiento rápido de
Colletotrichum
G Guanina
IGS Espacio intergénico
ITS Espaciador transcrito interno
KLA Key Lime Anthracnose, Antracnosis del limón mexicano
PCR Reacción en Cadena de la Polimerasa
SGO Slow Grow orange, crecimiento lento y de color naranja
SIAP Servicio de Información Agroalimentaria y Pesquera
T Timina
TBE Trizma/ácido bórico/sal disódica del ácido etilendiaminotetraacético
TE Trizma/ ácido clorhídrico/ sal disódica del ácido
etilendiaminotetraacetico.
TEMED N,N,N´,N´-tetrametil-etilendiamino
Tris-HCl Trizma/ácido clorhídrico
Trizma Tris hidroximetilaminometano

V
AGRADECIMIENTOS
Agradezco al Centro de Biotecnología Genómica del IPN por confiar en mí, y por
permitirme ser partícipe en una parte de este proyecto de investigación. Agradezco
profundamente a CONACYT por la beca otorgada, así mismo al Instituto Politécnico
Nacional por la beca PIFI y la beca tesis.
Agradezco a todo el personal del Centro de Biotecnología Genómica, profesores, técnicos
y personal de apoyo. Gracias por su valioso apoyo otorgado a lo largo de mi estancia en
este centro, ha sido una bonita experiencia el poder estar en el centro.

VI
DEDICATORIA
A mis padres y hermanos, aquellos que me han acompañado de cerca, Josafat, Tamar,
Matías, Gris, Chuy, Melina, Elim, a mis amigos de Reynosa, Puebla, San Mateo, Syracuse y
anexas.

VII
RESUMEN
La citricultura en Tamaulipas es una de las actividades generadoras de empleos y divisas,
con una superficie sembrada mayor a 45 mil hectáreas, de las cuales 4 mil corresponden a
limón amarillo o italiano (Citrus limon), cuya producción se procesa en 14 empacadoras
en la zona centro del Estado. Las enfermedades causadas por hongos fitopatógenos
disminuyen la producción citrícola, entre estas se encuentra la enfermedad denominada
“Caída del fruto pequeño” (CFP) cuyo agente causal se ha reportado que es
Colletotrichum acutatum, en limón mexicano. Se han realizado algunos estudios del
diagnóstico de esta enfermedad en México, y como parte de las respuestas a este
problema se ha promovido el uso de fungicidas sintéticos. En este trabajo se realizó el
diagnóstico de la presencia del agente causal de la enfermedad CFP en la región citrícola
de Nuevo Padilla localizado en el estado de Tamaulipas. Se aislaron 39 hongos presentes
en el interior de tejido vegetal que presentaba síntomas de la enfermedad, y se secuenció
su región 26S del ADNr para identificarlos molecularmente, encontrándose tanto al
género Colletotrichum como a otros 10 géneros más de hongos, algunos de ellos
reportados previamente como patógenos, por lo que se realizó la caracterización de
patogenicidad de los mismos, el cual demostró que los aislamientos con mayor respuesta
patogénica fueron los de Glomerella etiquetados como: CF-12, CF-39 y CF-14, siendo
este último el más agresivo, además de Alternaria CF-38 y Fusarium sp. Los escasos
estudios reportados para el control biológico del CFP hasta ahora solo han sido con
bacterias, sin embargo en este trabajo se evaluaron levaduras nativas de los huertos de
Padilla para llevar a cabo un biocontrol. Los resultados de las pruebas de antagonismo
llevadas a cabo, tanto en hojas como en flores con los presuntos hongos patógenos,
mostraron que la levadura LCBG-03 tiene el mejor desempeño alcanzando a inhibir el
crecimiento de los hongos del género Colletotrichum/Glomerella hasta un 93% en los
experimentos in vitro. En este estudio no fue aislado C. acutatum pero si C.
gloeosporioides el cual mostró una alta capacidad de infección en flores y una ligera
infección en hojas, por lo que podría asociarse a un patotipo aislado de patogenicidad, no
obstante no hay reportes de estudios en México para el limón italiano y este es uno de los
primeros trabajos llevados a cabo en esta entidad.

VIII
ABSTRACT
The Tamaulipas citrus industry provides many jobs and finatial benefits to the state, with
a planted area of more than 45 thousand hectares, of which 4000 of them are planted with
Italian lemon (Citrus limon). This crop is processed in 14 packing facilities in the central
area of the state. Unfortunately, the diseases caused by fungal pathogens reduce this
citrus yield, among these, there is a disease called "Postbloom fruit drop" (PFD) caused
by Colletotrichum acutatum according to the reports on Mexican lime, according to some
studies on the diagnosis of this disease in Mexico. In response to the prevalence of this
disease, some researchers have promoted the use of synthetic fungicides. In this work, it
was diagnosed the presence of the causative agent of the PFD in the citrus region of
Nuevo Padilla, located in the state of Tamaulipas, obtaining 39 isolated fungi within the
plant tissue that showed symptoms of the disease. The 26S rDNA region of the fungi
were sequenced to identify them on a molecular level. It was found the genus
Colletotrichum and 10 other genera of fungi, some of them previously reported as
pathogens, and after a characterization of pathogenicity, we found that the most
pathogenic isolates were Glomerella labeled: CF-12, CF-39 and CF-14. The latter was
the more aggressive and after this Alternaria CF-38 and Fusarium sp. A few studies
have reported bacteria to perform the biocontrol of this disease, but in this work a
collection of native citrus´ yeasts from Nuevo Padilla citrus orchards were characterized
against the isolated fungi. The results of the antagonism tests conducted in both leaves
and flowers with all the suspected fungal pathogens showed that yeast LCBG-03 had the
best performance in experiments in vitro, achieving an up to 93 % inhibition of the
growth of fungi of the genus Colletotrichum / Glomerella. In this study C. acutatum was
not isolated but C. gloeosporioides showed a good capacity to infect flowers and leaves,
so that it could be associated with a pathogenic isolate pathotype. To our knowledge this
is one of the firsto reports of studies in Mexico for the Italian lemon concerning this
disease.

9
1. INTRODUCCIÓN
La citricultura en Tamaulipas es una de las actividades generadoras de empleos y divisas,
con una superficie sembrada mayor a 45 mil hectáreas, de las cuales 4 mil corresponden a
limón amarillo o italiano (Citrus limon), cuya producción se procesa en 14 empacadoras
en la zona centro del Estado. Las enfermedades causadas por hongos fitopatógenos
disminuyen la producción citrícola, entre éstas se encuentra la enfermedad denominada
“Caída del fruto pequeño” (CFP) cuyo agente causal se ha reportado que es el hongo
Colletotrichum acutatum, en limón mexicano. Los fungicidas benomyl y captafol han
resultado efectivos para el control de la enfermedad, sin embargo el uso exagerado de
éstos causa deterioro al medio ambiente, una alternativa amigable al medio ambiente es
el control biológico. Hay grandes expectativas en microorganismos antagonistas para
llevar a cabo el control de enfermedades causados por hongos fitopatógenos en cítricos.
El control efectivo de las enfermedades de los cítricos se puede llevar a cabo mediante
una estrategia planeada y dependiendo de las características que presenten tanto el
antagonista, el hospedero y el hongo patógeno. Las levaduras antagonistas tienen el
potencial de ser usados para el control biológico, aunado a una serie de pruebas
moleculares y bioquímicas éstos pueden asegurar la utilidad específica para que esta sea
inocuo al ser humano, así como cumplir los requisitos para permitir su uso en la
citricultura cuidando el medio ambiente. En la actualidad hay un fomento mundial por
cuidar el medio ambiente, no generando residuos químicos, el uso de fungicidas
sintéticos para controlar las enfermedades en los cítricos se ha usado ampliamente
trayendo como consecuencias daños al medio ambiente y así mismo la resistencia de los
fitopatógenos que requieren cada día más y mejores formulaciones químicas para que
sean controlados, por otra parte la exigencia de las normas para asegurar la inocuidad de
los alimentos han llevado a adoptar nuevas legislaciones en muchos países para reducir el
número de ingredientes de pesticidas activos aprobados (Trillas et al., 2006), esto ha
generado también un interés para trabajar con los agentes de control biológico como
alternativas a los métodos químicos, como por ejemplo el uso de biopesticidas,
enmiendas orgánicas, plantas resistentes a determinados patógenos, plantas micorrizadas,

10
rotación de cultivos (Fernández y Juncosa, 2002), para prevenir y controlar
enfermedades de las plantas.
El estudio de control biológico se hace sumamente importante para la citricultura, y una
muestra de ello son las diferentes formulaciones que existen en los mercados de países
que han desarrollado este tipo de productos para control de algunas enfermedades de
cítricos, cabe mencionar que la mayoría de los productos son para aplicaciones de
poscosecha, ya que estas condiciones tienen características donde las estrategias de
biocontrol resultan más eficientes (Wharton y Diéguez, 2004), la caída del fruto pequeño
es una enfermedad en precosecha que afecta a la citricultura mexicana (Orozco-Santos et
al., 2008; Peres et al., 2008), esta enfermedad se ha controlado con estrategias de
químicos sintéticos con fumigaciones en el momento de la floración. Los productos más
eficaces reportados son: benzimidazoles, triazoles y algunos ftalimidas (Kupper et al.,
2003). Sin embargo, en condiciones de alta precipitación o prolongadas precipitaciones,
los fungicidas tienen una eficacia limitada. Teniendo en cuenta los costos, así como las
crecientes restricciones a la presencia de residuos en los frutos, es necesario el estudio de
nuevas alternativas, entre ellos, el control biológico se convierte en una importante y
técnicamente justificable. Es de importancia estudiar el biocontrol ya que a la fecha no
hay productos que puedan ser aplicados para el control de la Caída del Fruto Pequeño.
Pichia guilliermondii es una levadura epifítica antagonista aislada de la región citrícola
de Tamaulipas, que ha mostrado una efectividad aceptable para combatir fitopatógenos
de acuerdo a estudios realizados por Lara Rodríguez (2006).
Primeramente se realiza un diagnóstico del agente causal, y después la medición de la
capacidad de la levadura antagonista en pruebas de patogenicidad in vitro y pruebas de
patogenicidad in vivo, utilizando hojas de limones para medir la capacidad de infección
de los presuntos hongos fitopatógenos aislados en esta región.

11
2. ANTECEDENTES
2.1 Los cítricos
Los cítricos pertenecen a la clase Angiospermae, subclase dicotiledónea, orden rutae,
familia rutaceae y al género Citrus, y algunas especies que se destacan por su importancia
comercial: naranja (Citrus sinensis), mandarina (Citrus reticulata), limones (Citrus
aurantifolia, C. latifolia y C. limon), lima (Citrus aurantifolia) y la toronja (Citrus
paradisi) y otros más. Los cítricos se originan en las áreas subtropicales y tropicales de
Asia, considerándose a China como el centro de origen. La naranja dulce fue el primer
cultivo de cítricos introducido al continente americano por los primeros colonizadores, en
Sudamérica fue introducido a Brasil y en América del Norte a México.
México ocupa el primer lugar en la producción de limón y lima y tercer lugar en la
producción de Toronja y naranja a nivel mundial. Los principales estados que producen
son: Veracruz, San Luis Potosí, Tamaulipas, Nuevo León. Tabasco, Puebla, Yucatán,
Hidalgo, Colima, Oaxaca, Guerreo y Michoacán; con un total de 542 mil hectáreas
plantadas. Las exportaciones de limón mexicano pasaron de 22 mil 275 toneladas en
2002 a 46 mil 542 toneladas en 2009, lo que arroja una tasa de crecimiento de 11.1 por
ciento. El principal destino del limón mexicano en 2009 fue Estados Unidos que absorbió
el 99.6% del volumen total exportado (SAGARPA, 2010).
A nivel nacional los cítricos ocupan el primer lugar en volumen total de producción de
frutales con un 34%, seguido por las uvas (27%), plátanos (21%) y manzanas (18%) Esto
indica que los cítricos son un cultivo de gran importancia en nuestro país, por lo que
cualquier desarrollo y mejora en la producción, será benéfico para la economía del los
productores y del país.
El estado de Tamaulipas, localizado en el noreste de México, es un importante productor
de cítricos con una superficie mayor a las 45,000 hectáreas, donde se cultivan naranjas
dulces, mandarinas, toronjas y limones. (Ruíz et al., 2006). El 60% del limón italiano
que se comercializa en Estados Unidos es producido en Tamaulipas (Secretaria de
desarrollo rural, 2006), este es un rubro importante para la economía de la región sur del

12
estado (Zermeño-González et al., 2007). Uno de los factores más relevantes que hacen
disminuir la producción de los cítricos son las enfermedades, principalmente de hongos
fitopatógenos que atacan a los plantíos en precosecha y poscosecha.
2.2 Hongos fitopatógenos en cítricos
Las enfermedades fúngicas causan problemas significantes en la producción de cítricos
(Timmer et al., 2004). La presencia de estos hongos fitopatógenos que atacan la raíz,
troncos, hojas, frutos y flores, estos son puntos de entrada para los patógenos (Campbell,
1989) y constituyen un factor de riesgo para el desarrollo de los cultivos (Ochoa et al.,
2007). Sus consecuencias son de gran relevancia pues provocan directamente una
disminución de la producción así como una baja calidad del fruto, al modificar sus
características inherentes. A continuación se muestra la siguiente tabla donde se
describen algunas enfermedades en los cítricos causados por los hongos fitopatógenos
(cuadro 1).
Cuadro 1. Principales enfermedades de cítricos causados por hongos fitopatógenos
Enfermedad Agente causal
Pudrición verde Penicillium digitatum
Pudrición azul Penicillium italicum
Roña de los cítricos Sphaceloma fawcetti
Pudrición por Fusarium (Fruta) Fusarium spp.
Pudrición de pie o Gomosis Phytophthora spp.
Mancha foliar de los cítricos Alternaria limícola
Albinismo Alternaria alternata, Aspergillus flavus
Secadera (Damping off) Rhizoctonia solani, Phytophthora spp y Pythium sp.
Caída del Fruto Pequeño Colletotrichum acutatum
Antracnosis Glomerella cingulata, Colletotrichum gloeosporioides
Melanosis Diaporthe citri, Phomopsis citri
Pudrición del moho negro Aspergillus niger
Tomado de http://www.apsnet.org/online/common/names/citrus.asp

13
2.3 El género Colletotrichum
El género Colletotrichum pertenece a los hongos ascomicetos, conteniene especies que
son muy patogénicos a las plantas causando daños económicos a los cultivos tropicales,
subtropicales y regiones templadas (Wharton y Diéguez, 2004), incluyendo a los cítricos
(Citrus spp.). Los cuales son afectados por el hongo Colletotrichum spp. causante de la
enfermedad conocida como antracnosis, considerado un problema serio en las regiones
citrícolas.
Actualmente, la identificación de las especies del género Colletotrichum se basa
principalmente en la morfología, el rango de hospedantes y el modo de parasitismo. La
mayoría de los reportes recientes indican que la especialización del hospedante es un
criterio taxonómico (Wharton y Diéguez, 2004). El ciclo de vida de las especies de
Colletotrichum comprende un estado sexual anomorfo como Colletotrichum y uno
asexual teleomorfo como Glomerella. Tres formas de Colletotrichum son reconocidas
en lo cítricos, la forma gris y de crecimiento rápido, (FGG), diferentes a las otras dos,
crecimiento lento color naranja (SGO) que es el agente causal de la caída del fruto
pequeño y la forma (KLA) Antracnosis de limón Mexicano (Brown et al., 1996).
Colletotrichum gloeosporioides causa antracnosis en frutos de cítricos y es un saprobio
común en plantaciones de cítricos, mientras que Colleotrichum acutatum infecta pétalos
de flores y causa la caída del fruto pequeño (Timmer et al., 1998). Posee los dos tipos de
estrategias de infección descritas para el género Colletotrichum, intracelular
hemibiotrófica y subcuticular – intramural necrotrófica, puede incluso establecer un
periodo de latencia con la finalidad de hacer frente a los mecanismos de defensa del
hospedante. Colletotrichum acutatum generalmente inverna como micelio y/o apresorios
en distintas partes del hospedante (Wharton y Diéguez, 2004).
2.4 La Caída del Fruto Pequeño en cítricos
La caída de fruto pequeño (CFP) se reportó por primera vez en Belice en 1959 y
posteriormente se detectó en 1968 en México (Timmer et al., 2004). Actualmente ocurre

14
en la mayoría de las zonas productoras del estado de Veracruz, Tamaulipas y Tabasco.
De igual forma se ha reportado en otros países productores como Estados unidos, Brasil y
Argentina, entre otros. La enfermedad afecta a todas las especies de los cítricos y se
presenta en regiones que registran lluvias durante los periodos de floración –
fructificación como es el caso de la región citrícola de Tamaulipas. La enfermedad
caracterizada por la abscisión del fruto prematuro, ha sido asociado con un incremento de
la producción de etileno, ácido indol acético (IAA) y cantidades de ácido jasmónico en
los pétalos infectados (Lahey et al., 2004). Se han reportado que puede reducir el
rendimiento en un 49% en huertos de naranja valenciana. En México, en los últimos años
ha cobrado una gran importancia, llegando a ocasionar pérdidas hasta de un 70%
(Orozco-Santos et al., 2008). La “Caída del Fruto Pequeño” causada por el hongo
Colletotrichum acutatum Simmonds (Timmer et al., 1994), se desarrolla en trópicos y
subtrópicos húmedos en las Américas (Ruíz et al., 2006). Los intentos de control
biológico de C. acutatum en algunos países han sido a través de la introducción de
agentes de biocontrol por bacterias del género Bacillus (Kupper et al., 2003).
2.5 Sintomatología de la caída del fruto pequeño
La enfermedad CFP, caracterizada por la caída del fruto, se presenta durante el período
de floración principal que ocurre en los meses de febrero-marzo (Timmer et al., 1994).
Los primeros síntomas se manifiestan en los pétalos como una necrosis acuosa de color
naranja a café; los pétalos necrosados quedan adheridos a la parte basal del disco floral
con apariencia dura, seca y de color café rojizo. En ataques severos, el patógeno afecta
racimos florales enteros cuando las condiciones para su desarrollo son favorables.
Posteriormente, los frutos en desarrollo toman una coloración amarillenta en la base, que
avanza hasta cubrirlos por completo y ocasiona su caída cuando tienen aproximadamente
un centímetro de diámetro. El síntoma característico de esta enfermedad es que al caer el
fruto, tanto el pedúnculo como el receptáculo y cáliz permanecen adheridos a la rama.
Estas estructuras se conocen como "tachuelas" en los estados citrícolas del Golfo de
México. Las tachuelas están rodeadas por hojas levemente distorsionadas y con

15
nervaduras prominentes (Timmer et al., 1994). Las flores y frutos jóvenes que se
encuentran cerca de flores afectadas también están propensas a caer antes del amarre de
fruta y formar tachuelas persistentes. La abscisión del fruto ocasionada por la enfermedad
ocurre en la base del ovario, lo que contrasta con la abscisión provocada por los procesos
fisiológicos normales del árbol, la cual ocurre en la base del pedúnculo. Por otra parte los
efectos de Colleotrichum acutaum pueden causar lesiones a los frutos que logran
quedarse en el árbol, manifestando el problema de adentro hacia afuera como se puede
observar en la figura 1, estas lesiones disminuyen el rendimiento de la producción.
Estas observaciones sugieren que algunas fitohormonas podrían estar involucradas en el
desarrollo de estos síntomas (Wharton y Diéguez, 2004). Estudios recientes han
demostrado la habilidad de C. acutatum para producir IAA y compuestos relacionados, lo
cual puede contribuir parcialmente a incrementar los niveles de esta fitohormona en las
flores de cítricos infectadas (Chung et al., 2003).
Figura 1. Síntomas en frutos de limón mexicano causado por Colletotrichum acutatum. Fotografía
tomada de Orozco-Santos y Timmer (2005).

16
2.6 Etiología de la caída del fruto pequeño
Durante mucho tiempo, el causante de la caída de fruto pequeño fue atribuido a una raza
del hongo Colletotrichum gloeosporioides (Penz.), que produce en medio de cultivo una
colonia de color anaranjado de lento crecimiento. Se han caracterizado razas involucradas
en las enfermedades conocidas como caída de fruto pequeño y antracnosis del limón
mexicano. La primera se atribuyó a la raza SGO (colonias de color naranja y lento
crecimiento) de C. gloeosporioides y la segunda a la raza KLA (antracnosis del limón
mexicano) del mismo hongo. Estudios posteriores con técnicas moleculares demostraron
que ambas razas corresponden a Colletotrichum acutatum Simmonds (Brown et al.,
1996). C. acutatum produce conidios hialinos, unicelulares que miden de 12 a 20 μm de
largo por 4 a 6 μm de ancho y una elevada proporción con un lado redondeado y otro
fusiforme con relación a conidios con ambos lados redondeados. Estas esporas se
producen en estructuras llamadas acérvulos. Así mismo, forman apresorios redondeados
y pequeños (Orozco-Santos et al., 2008).
2.7 Variedad morfológica de Colletotrichum acutatum
Los aislamientos de C. acutatum que causan caída de fruto pequeño y colectados en
naranja Valencia y limón Persa en Tamaulipas, Veracruz y Tabasco presentan micelio
escaso, ligeramente algodonoso, distribuido de manera uniforme, en ocasiones de aspecto
polvoriento y de color blanco (Orozco-Santos et al., 2004), estas características se pueden
observar en la figura 2, asi también se observa el ataque en flores de limón.
El aspecto general de la colonia es de color naranja ligero, acentuándose más en la parte
central. Estos aislamientos presentan mayor porcentaje de conidios con un lado fusiforme
y el otro redondeado en comparación a conidios redondeados y los apresorios son de
forma clavada (Orozco-Santos et al., 2008). Estas características corresponden a las
descritas para la raza CFP de lento crecimiento y de color naranja que causa la caída de
fruto pequeño (Agostini et al., 1992).

17
Figura 2. Características morfológicas de crecimiento de micelio, conidios y síntomas en la flor del
limón, causado por Colletotrichum acutatum, CFP (PFD por sus siglas en inglés). Fotografías tomada
de Orozco-Santos y Timmer (2005).
2.8 Epidemiología de la caída del fruto pequeño
La caída de fruto pequeño se presenta en regiones con lluvias durante el período de
floración. El ciclo de la enfermedad (fig. 3) ocurre de la siguiente manera: los conidios
del hongo se producen de manera abundante en los acérvulos formados sobre los pétalos
de flores infectadas durante la primavera. Estos conidios son lavados por las gotas de
agua de lluvia o rocío y depositados en los tejidos vegetativos del árbol, en donde pueden
germinar para formar apresorios o permanecer sin germinar y ocasionar infecciones
latentes. En ausencia de floración, estos propágulos pierden viabilidad con el tiempo. Sin
embargo, cuando se inicia la floración, los pétalos que caen sobre la superficie de las
hojas proporcionan algunas sustancias que estimulan la germinación del apresorio para
formar conidios, los cuales son diseminados hacia las flores nuevas por el salpique de las
gotas de agua de lluvia, reiniciando de esta manera el ciclo de la enfermedad. Su daño es
más severo y puede manifestarse de manera epidémica cuando se presentan lluvias, o en
períodos prolongados con alta humedad relativa y temperaturas bajas durante la floración
y "amarre" del fruto (Agostini et al., 1993).

18
Figura 3. Ciclo de vida e infección de Colletotrichum acutatum. Dibujo tomado de Orozco-Santos y
Timmer (2005).
La temperatura óptima para la germinación de la espora es de 23 °C y el tiempo mínimo
para la infección y germinación es de 12 a 18 h. Si las condiciones húmedas prevalecen,
alrededor del 90 % de las flores pueden mostrar síntomas a los 3-4 días después de la
infección. Sobre las flores afectadas se producen numerosos acérvulos, lo cual
incrementa drásticamente el número de esporas patogénicas dentro del árbol. Las flores
son resistentes al patógeno cuando los botones presentan de un estado de cabeza de alfiler
a botón en estado redondo y son susceptibles cuando se empiezan a elongar y son
altamente susceptibles una vez que se abren. La enfermedad empieza a aparecer cuando
el botón floral tiene un centímetro de largo. El hongo C. acutatum sobrevive entre
períodos de floración como apresorios y/o infecciones latentes sobre las tachuelas
adheridas, hojas y ramas. Estudios recientes han demostrado que el número de tachuelas
adheridas en ramas de los años previos es el mejor indicador del potencial de la
enfermedad en la próxima floración (Orozco-Santos et al., 2008).

19
2.9. Análisis moleculares para la identificación de hongos
Los ribosomas son complejos ribonucleicos responsables de la síntesis de proteínas.
Debido a su función esencial para la vida, las regiones que los codifican en los genes de
los diferentes organismos se han ido conservando a lo largo de la evolución en una
frecuencia muy superior a otros genes. El ADNr es una formación en tándem de
numerosas copias en el genoma de los todos los hongos. Comprende, entre otras, las
regiones codificantes del gen de la subunidad pequeña ADNr (18S), el gen 5.8S y el gen
de la subunidad grande ADNr (28S o 26S), como se muestra en la figura 4, y otras
regiones interesantes para la identificación de especies fúngicas como los ITS (ITS1 y
ITS2) y los IGS (Soriano del Castillo, 2007).
Figura 4. Posición de los iniciadores utilizados para la amplificación de los genes ribosomales
utilizados en la identificación de hongos (tomado de Rodríguez et al., 2004).
2.10 Control químico de hongos fitopatógenos
El control de la caída de fruto pequeño se basa principalmente en la aplicación de
fungicidas durante los períodos de lluvias frecuentes en la época de floración. Los
fungicidas benomyl y captafol han resultado efectivos para el control de la enfermedad
(Timmer y Zitko, 1992), así como otros productos como bencimidazoles, triazoles, sin
embargo en condiciones de alta precipitación los fungicidas tienen una eficacia limitada
(Kupper et, al., 2003). En condiciones favorables para el desarrollo del patógeno (lluvias,
alta humedad relativa y temperaturas bajas) durante la floración y cuando se espere un
ataque fuerte de la enfermedad se requiere un mayor número de aplicaciones de estos

20
productos y es donde se presenta un impacto de mayor magnitud al medio ambiente. En
localidades con ataques severos son necesarias aplicaciones semanales o cada 10 días. En
todos los casos, los fungicidas que se utilizan son el benomyl y captafol (Orozco-Santos
et al., 2008).
2.11 Control biológico de hongos fitopatógenos
Los microorganismos que han sido usados como antagonistas comprenden bacterias,
hongos y levaduras, por su capacidad de ejercer un efecto de control biológico sobre
diferentes patógenos de interés en frutos y vegetales (Hernández-Lauzardo et al., 2007),
como los que se muestran en el cuadro 2, de biofungicidas que contienen bacterias y
hongos como materia activa y además de ya haber sido comercializados., asi también en
el cuadro 3 se despliegan estudios realizados aplicando microorganismos antagonistas en
el control de hongos fitopatógenos en poscosecha de cítricos.
Las levaduras son organismos eucariotas unicelulares pertenecientes al reino de los
hongos, de forma esférica u oval y que se encuentran ampliamente distribuidas en la
naturaleza. Debido a su gran adaptabilidad a diferentes condiciones ambientales, las
levaduras pueden utilizarse como agentes de control biológico, y estas a su vez pueden
utilizar uno o más mecanismos de antagonismo.
Los productos a base de microorganismos presentan como principales ventajas:
Especificidad en su actuación
Respeto al medio ambiente
Los patógenos tienden a desarrollar menor resistencia a productos microbianos
que a productos químicos.
Las principales barreras con las que se encuentran los productos formulados a base de
microorganismos son: 1) Una efectividad de control en general menor que los productos
químicos; 2) Generalmente su acción no es inmediata; 3) Dificultades de producción a
nivel comercial; 5) Necesidad de resolver problemas técnicos como la sensibilidad a

21
factores (temperatura, radiación UV, humedad) que presentan la mayoría de estos
productos. (Fernández y Juncosa, 2002).
2.11.1 Mecanismos de biocontrol
En general los antagonistas no tienen un solo mecanismo para controlar los patógenos, Se
han reportado mecanismos por los cuales los agentes de control biológico ejercen su
acción, estos son:
Antibiosis. Se refiere a la producción por parte de un microorganismo de sustancias
tóxicas como antibióticos en bajas concentraciones para inhibir el crecimiento o
germinación de los microorganismos patogénicos.
Competencia por nutrientes y espacio. Se refiere a la capacidad de crecimiento y de
obtención de los nutrientes, debe existir escasez de un elemento, de lo contrario no habrá
competencia. La competencia más común es por nutrientes, oxígeno o espacio. La
competencia por espacio y nutrientes son los principales componentes en el modo de
acción de las levaduras antagonistas.
Parasitismo. El término parasitismo se refiere al hecho de que un microorganismo
parasite a otro. Puede ser definido como una simbiosis antagónica entre organismos. El
parasitismo consiste en la utilización del patógeno como alimento por su antagonista.
Generalmente se ven implicadas enzimas extracelulares tales como quitinasas, celulasas,
β-1,3 glucanasas y proteasas, las cuales lisan las paredes de las hifas, conidios o
esclerocios de los agentes causales de enfermedades (Bar-Shimon et al., 2004).
Inducción de resistencia a la planta. Las plantas como otros seres vivos desarrollan
mecanismos de defensa contra sus invasores. De esta forma, se postula que la resistencia
es la regla mientras que la susceptibilidad es la excepción. Si se elige una planta
cualquiera y se compara el inmenso número de microorganismos que existe en su entorno
con el limitado número de microorganismos patógenos de ella se debe concluir que esto
es así en la gran mayoría de los casos.

22
Cuadro 2. Biofungicidas que contienen como materia activa bacterias o hongos comercializados en
diferentes países incluyendo los específicos para cítricos (Fernández y Juncosa 2002)
Agente de control biológico Patógeno Producto comercial
Pseudomonas cepacia Hongos (Fusarium, Phylum,
Rhizoctonia) nematodos
Blue Cirde (Stine Seeds), Deny
(CTT Corp). Intercept (Encore
Technologies)
Pseudomonas syringe ESC 10, 11 Postcosecha Botrytis, Penicillium,
Mucor, Geotrichum
Bio-save 100 y 1000. Bio-save
110 (Eco-Science)
Pseudomonas aureofaciens Tx-1. Antracnosis, Phytium, Michrochium Spot-Less (Eco soil Systems,
Inc.)
Bacillus subtillis Fusarium, Rhizoctonia, Aspergillus,
entre otros
HiStick N/T (MicroBio
Group), Serenade (AgraQuest,
Inc.)
Bacillus subtillis GB03 Rhizoctonia, Fusarium, Alternaria,
Aspergillus y mas
Kodiak (Gustafson), Bactophyt
(NPO Vector) System 3
Trichoderma harziarum KRL AG2
Phytium, Rhizoctonia, Fusarium,
Sclerotinia T-22G, T-22HB (Bioworks),
Trichoderma harziarum
Botrytis, Colletotrichum, Fulvia,
Monilia, y otros
F-Stop (Eastman Kodak),
Supresivi (Borregaard Bio
Plant)
Trichoderma viride
Armillaria, Botryosphaeria, Fusarium,
Nectria y otros
Trichomic (Trichodex),
Trichopel, Trichoject,
Trichodowels, Tricoseal
Trichoderma ligonorum Fusarium sp Trichodermin-3 (compañía rusa
y búlgara)
Trichoderma spp
Rhizoctonia solani, Phytium,
Sclerotium, Fusarium
Promot (J.H. Biotech, Inc.),
Trichopel (Agrimm
Biologicals)
Micorriza Botrytis, Pythium
Vaminoc (AGC Microbiol)
Candida oleophila 1-182 Postcosecha Botrytis spp., Penicillium
Aspire Oncogen
2.12 Las levaduras como agentes de control biológico
Las levaduras se encuentran ampliamente distribuidas en la naturaleza. Debido a su gran
adaptabilidad a diferentes condiciones ambientales, las levaduras pueden utilizarse como
agentes de control biológico, usando uno o más mecanismos de antagonismo. Se han
reportado varias levaduras antagonistas para inhibir con un grado de aceptación el
desarrollo de patógenos poscosecha en diversas frutas (cuadro 3). Entre estas levaduras

23
se encuentra, Pichia guilliermondii US-7 y Candida oleophila Montrocher donde este
último fue desarrollado en un producto comercial para el uso en cítricos y manzanas.
(Droby et al., 1998). Cryptococcus laurentii ha probado ser un antagonista en cítricos
contra el moho verde. Se ha demostrado que la levadura Pichia anomala cepa K, es
eficaz en el control del moho gris de la manzana, y que su producción de exo-β-1,3-
glucanasa se triplica con la presencia de las paredes de B. cinerea en heridas de manzana,
reduciendo el tamaño de la lesión más de la mitad. Esto confirma la hipótesis de que la
exo-β-1,3-glucanasa participa en el biocontrol del moho gris por este antagonista
(Petersson y Schnurer, 1995).
Cuadro 3. Principales estudios realizados aplicando microorganismos antagonistas en el control de
hongos poscosecha in vitro e in vivo (Hernández Lauzardo et al., 2007)
Microorganismo
antagonista Hongo fitopatógeno Efecto
Pseudomonas cepacia Penicillium expansum,y Penicillium
digitatum
Resultados variables dependiendo del tiempo
de almacenamiento (in situ)
P. cepacia
P. cepacia, P. siringe.
Debaryomyces hansennii
Penicillium digitatum
Penicillium digitatum,y
Penicillium italicum
Inhibición del crecimiento del patógeno y
control de la enfermedad en un 80% (in vitro
e in situ)
P. cepacia mostró mejor efecto de biocontrol
evidenciándose mediante la producción de
antibióticos (in vitro).
Candida saitoana
Botrytis cinérea, Penicillium
expansum. Penicillium y
digitatum.
La combinación de la aplicación del
antagonista con 0.2% de 2 – deoxi- D-
glucosa fue efectiva en controlar las
pudriciones (in vitro e in situ)
Candida famata Penicillium digitatum Producción de fitoalexinas y control de la
producción en un 90% (in situ)
Verticillium lecanii Penicillium digitatum Inducción de reacciones de defensa en el
patógeno y antibiosis (in vitro)
Lara Rodríguez (2006), evaluó e identificó a las levaduras antagonistas nativas de la
superficie de los cítricos de la región de Tamaulipas, estas cepas pueden ser usadas para
el biocontrol de algunos hongos fitopatógenos en esa área. Las cepas de levaduras que
ejercieron mayor efecto de inhibición fueron la cepa LCBG-30 y la CIB-A17.

24
3. JUSTIFICACIÓN
En México se ha reportado que la enfermedad de la caída del fruto pequeño ha llegado a
causar hasta un 70% de perdidas en cítricos y este problema no ha sido estudiado en la
región citrícola de Tamaulipas. En los últimos años, esta actividad ha pasado a ocupar un
lugar muy importante en el desarrollo del estado de Tamaulipas al generar más de mil
500 empleos temporales que impactan en los municipios del centro. Actualmente la
producción del limón con 3 401 hectáreas registradas mantiene al estado en el segundo
lugar nacional, cuya exportación se calcula en 40 mil toneladas anuales a los mercados de
Estados Unidos, Japón y Europa. Estos logros deben permanecer y mejorar entre otros
aspectos el estudio de enfermedades que son potencialmente riesgosas a la disminución
de la producción de limón italiano, tal es el caso de la enfermedad conocida como “caída
del fruto pequeño” que ha sido reportado a en diferentes estados de la republica
mexicana pero sin estudios desarrollados en limón italiano en el estado de Tamaulipas,
por lo tanto cualquier información obtenida que ayude a la prevención o mejora de la
producción de limón italiano beneficiará la economía del estado.
Los estándares para obtener un limón con calidad de exportación implican cumplir entre
otros requisitos los limites permisibles de residuos químicos, plaguicidas y ausencia de
patógenos, éstos parámetros son considerados normativos tanto para los países
importadores como para los exportadores y no resulta fácil lograrlos, por consiguiente
lograr algunas ventajas con el control biológico seria bueno ya que hasta ahora solo se
conocen estrategias de fungicidas sintéticos para controlar la enfermedad “caída del fruto
pequeño”. Las estrategias de control biológico con agentes de biocontrol no se han
desarrollado para esta enfermedad en particular en este estado de la república.
A este respecto, el uso de levaduras epifíticas de frutos de cítricos es particularmente
conveniente, debido a su fácil manipulación, propagación y la rápida colonización de los
tejidos vegetales, además de ser inocuas al ser humano. De lograrse avanzar en el
biocontrol de la CFP sería conveniente para los agricultores y para el medio ambiente.

25
4. HIPÓTESIS
El agente causal de la caída del fruto pequeño es inhibido de forma significativa por
levaduras antagonistas.
5. OBJETIVOS
5.1. Objetivo general
Diagnosticar y biocontrolar el agente causal de la caída del fruto pequeño en limón de
Tamaulipas.
5.2. Objetivos particulares
5.2.1. Diagnosticar el hongo fitopatógeno causal de la caída del fruto pequeño del
limón italiano en la región citrícola de Tamaulipas
5.2.2. Determinar la patogenicidad de los aislamientos de los hongos asociados a la
caída del fruto pequeño del limón italiano.
5.2.3. Seleccionar levaduras antagonistas para controlar los hongos fitopatógenos
basado en pruebas in vitro e in vivo.

26
6. MATERIALES Y MÉTODOS
6.1 Muestreo y aislamiento de hongos fitopatógenos
La colecta de las muestras con sintomatologías de antracnosis en cálices, hojas y frutos
de limón (Fig. 5) se llevó a cabo en dos huertos de limón Italiano de la zona citrícola de
Nuevo Padilla (Tamaulipas) en Julio de 2009.
Figura 5. Lesiones en hojas y frutos de limón italiano de Tamaulipas, A) Hojas senescentes con
síntomas de crecimientos de hongos B) Limones secos que no se desarrollaron C) Cálices que
quedaron sin el fruto (tachuelas).
Los huertos muestreados tienen 7 años plantados, la variedad ingertada es limón italiano
en patrón volkameriana, y están en plena etapa de producción, cuentan con detectores de
humedad para el control de riego, y son sometidos a control de fumigación con productos
químicos, aunque durante el muestreo tenían por lo menos 3 meses de haber sido
asperjados con fungicidas.
Las colectas se realizaron en 11 puntos de los huertos 6 y 7 en un área de 4 km2, estos
puntos se determinaron de manera aleatoria y se tomaron las coordenadas (cuadro 4). El
material fue transportado inmediatamente para su análisis.

27
Cuadro 4. Esquema de muestreo y localización de los puntos en los huertos de limones 6 y 7, ubicados
en Nuevo Padilla, Tamaulipas.
Para el aislamiento de los hongos intracelulares presentes en los tejidos colectados, se
cortaron piezas de 2 mm x 2 mm, desinfectados con hipoclorito de sodio al 1% (v/v)
durante 5 min y se lavaron 3 veces con abundante agua destilada estéril. Posteriormente,
los tejidos se colocaron en cajas petri con un medio de cultivo Papa-Dextrosa-Agar
(PDA, BD Bioxon, EEUU), preparado de acuerdo a las instrucciones del fabricante,
incubado por 5 días a una temperatura de 29 °C. Los aislamientos puros se obtuvieron
mediante resiembras en PDA de punta de hifa, mientras que, para la identificación del
hongo, se analizaron las características de la esporulación reportado de acuerdo a
Wharton y Diéguez, (2004) y Orozco-Santos (2008). Los aislamientos fueron mantenidos
en PDA a 4 °C, además de ser conservados en glicerol al 86% (v/v) a -70 °C.
No. Muestra Huerta Localización
1 Pedúnculos 7 AH. 62 m N 24° 04.161’ WO 98° 55.712'
2 Pedúnculos 7 AH.153 m N 24° 04.161’ WO 98° 55.634'
3 Pedúnculos 7 AH.153m N 24° 04.301’ WO 98° 55.597'
4 Fruto amarillo 6 AH. 150m N 24° 04.586’ WO 98° 55.712'
5 Fruto partido y
seco 6 AH. 157m N 24° 04.583’ WO 098° 55.718'
6 Fruto p. seco 6 AH. 157m N 24° 04.583’ WO 98°55.722'
7 Fruto partido 6 AH. 159m N 24° 04.481’ WO 98°55.701'
8 Hojas 6 AH. 146m N 24° 06.257’ WO 98° 56.543'
9 Hojas 6 AH. 150m N 24° 06.263’ WO 98° 56.542'
10 Hojas 6 AH. 146m N 24° 06.823’ WO 98° 56.013'
11 Hojas 6, 7 N/T

28
6.2 Extracción de ADN fúngico
Los aislados fúngicos fueron crecidos en PDA durante 48 h, las colonias aisladas fueron
utilizadas como inóculos en matraces de Erlenmeyer de 250 mL que contenían 50 mL de
medio YPD (Extracto de levadura 5 g L-1
, peptona 3 g L-1
, y glucosa 20 g L-1
), e
incubados a 29 °C a 250 rpm por 72 h. Con la ayuda de una pipeta se tomaron 40 mg de
micelio aproximadamente, ya que estos formaron pellets pequeños, las muestras se
llevaron a nitrógeno líquido por 20 min en tubos Eppendorf estériles de 1.4 mL con la
ayuda de un pistilo fueron maceradas por 5 min, inmediatamente después se añadieron
500 µL de buffer de extracción (200 mM Tris HCL pH 8.5, 250 mM NaCl 25mM EDTA,
0.5% SDS). Las muestras fueron homogenizadas e incubadas por 10 min a temperatura
ambiente. Posteriormente se añadieron 500 µL de fenol-cloroformo (25/25) a 4 °C, se
mezclaron en vortex a máxima velocidad durante 5 min, y se centrifugaron a 1300 rpm
durante 30 min. La fase acuosa se transfirió a otro tubo Eppendorf y se adicionaron 400
µL de cloroformo frío (4 °C) y se mezclaron en vortex a máxima velocidad durante 5
min. Estos fueron centrifugados a 1300 rpm durante 30 min, la fase acuosa se transfirió a
otro tubo eppendorf y se le adicionó 400 μL de cloroformo frio (4 °C). Se mezcló durante
1 min en vortex y se centrifugó durante 5 min a 1300 rpm. Posteriormente la fase acuosa
se transfirió a un nuevo tubo y se le adicionaron 8 µL de RNAasa (10 mg/mL). Se incubó
durante 30 min a 37°C en una placa de calentamiento. Se adicionaron a cada muestra
500 μL de isopropanol frio (4 °C), se mezcló por inversión ligera y se incubó a -20 °C
durante 15 min, se centrifugó durante 5 min. El sobrenadante se desechó, y el ADN fue
lavado con 500 µL de etanol al 70%, se mezcló por inversión y se centrifugó durante 5
min a 1300 rpm. El sobrenadante se desechó y el ADN se secó en papel secante durante
30 min para eliminar los excesos de etanol, y de esta forma se obtuvo el ADN genómico.
El sedimento fue resuspendido en 50 μL de agua mQ estéril y se mantuvo a 4 °C hasta su
uso.
6.3 Electroforesis en gel de agarosa
El gel de agarosa se preparó al 1% (p/v), disolviéndola en solución amortiguadora TBE
1X (1 g de agarosa + 100 mL de sol. amortiguadora), la solución amortiguadora TBE 1x

29
se obtiene de una solución stock TBE 10x (108 g Trisma Base, 55 g ácido bórico, 40 mL
EDTA 0.5 M pH8, se disuelven los reactivos en 800 mL de agua mili-Q estéril y se afora
a 1 L de agua mili-Q estéril). Se disolvió la solución de agarosa en solución
amortiguadora calentándolo en un horno de microondas. La agarosa disuelta se colocó en
un soporte para gel sellado con cinta adhesiva para su gelificación con un peine
incorporado. Se retiró la cinta adhesiva cuando el gel estaba solidificado y se colocó en la
cubeta de electroforesis. Los pocillos se colocaron con proximidad al cátodo (polo
negativo, color negro). Se añadió solución amortiguadora de electroforesis TBE 1X, para
que cubriera totalmente el gel de agarosa. Posteriormente se aplicó la muestra preparada
y el marcador de peso molecular en los pocillos, el volumen de las muestras varió
dependiendo de las necesidades de los protocolos, las muestras se mezclaron con 3 μL de
amortiguador de carga “sybr gold” (Invitrogen), se cargaron en una cámara horizontal de
electroforesis (Bio-Rad, EEUU). Los electrodos se conectaron a la fuente de alimentación
EC105, el tiempo varió de 50 a 70 min aproximadamente dependiendo de las muestras
cargadas. Finalmente se visualizaron los fragmentos de ADN mediante luz ultravioleta y
se tomó la imagen en el programa Kodak Molecular Imaging Ver.5.0.1.27.
6.4 Amplificación de regiones ribosomales
6.4.1Amplificacion de la región 26 S del rADN
Las reacciones se llevaron a cabo utilizando tubos de PCR de 0.2 mL esteriles, 50 ng mL-
1 de ADN genómico, 10 mM de dntp’s, 50mM de MgCl2, 5 μM de los iniciadores NL-1
(5´ GGTCCGTGTTTCAAGACGG 3´) y NL-4 (5´
GCATATCAATAAGCGGAGGAAAAG 3´), solución amortiguadora 10X, 5U μL-1
de
Taq (Promega, EEUU) a un volumen total de 25 μL. Esta reacción se llevo a cabo en un
termociclador i-Cycler (Bio-Rad, EEUU) con las condiciones: 1 ciclo (94 °C, 5 min), 35
ciclos (94 °C, 30 s; 59 °C, 30 s; 72 °C, 1 min) 1 ciclo (72 °C, 7 min) y finalmente se
enfrió a 6 °C. Este producto se visualizó en un gel de agarosa al 1% para todos los
aislamientos.

30
6.4.2 Amplificación de la región ITS1
Las reacciones se llevaron a cabo utilizando tubos de 0.2 mL esteriles, 50 ng mL-1
de
ADN genómico, 10 mM de dntp’s, 50mM de MgCl2, 5 μM de iniciadores, solución
amortiguadora 10X, 5U μL-1
de Taq (Promega, EEUU) a un volumen total de 25 μL. Para
la amplificación de esta región se usaron los iniciadores CgInt, CaInt2 (Brown et al.,
1996), y ITS4 con las condiciones: 1ciclo (94 °C, 5 min), 35 ciclos (94 °C, 1:25 min;
(TD) 58 – 62 °C, 1:30 min; 72 °C, 1 min 1 ciclo (72 °C, 7min), 1X (6 °C, 5min).
6.5 Purificación de productos de PCR
La purificación de los productos de PCR se llevó a cabo utilizando el estuche comercial
Wizard SV Gel and PCR Clean-Up System, se agregaron 25 µL del producto de PCR
obtenido y se mezcló con la pipeta. Se colocó la muestra en la columna de purificación
(Wizard SV Minicolumns) y se incubó por 5 min a temperatura ambiente, posteriormente
se centrifugó a 13000 rpm por 1 min, y se descartó lo filtrado. Se agregaron 125 μL de la
solución “Membrane Wash Solution”. Se incubó por 5 min y se centrifugó a 13000 rpm
por 1 minuto y se descartó lo filtrado nuevamente. Se agregaron 100 µL de la solución
“Membrane Wash Solution” y se incubó por 5 min y se centrifugó a 13000 rpm por 3
min, se descartó lo filtrado. Finalmente se cambió el tubo colector, pero continuando con
la misma columna, se agregaron 50 µL de “Nuclease-Free Water” y se incubó por 5 min,
se centrifugó a 13000 rpm por 1minuto, se recuperó el sobrenadante, el cual contenía el
producto de PCR purificado.
6.6 Secuenciación
La secuenciación del fragmento de ADN se llevo a cabo basado en el protocolo Big Dye
Terminador v3.1, Cycle Sequencing Kit. Applied Biosystems, utilizando el secuenciador
(Applied Biosystems, modelo ABI 3130), siguiendo los protocolos del fabricante,
usando los iniciadores “Forward” a una concentración de 5 μM.

31
6.7 Pruebas de patogenicidad por aspersión en hojas de limón
Los primeros ensayos de infección se llevaron a cabo en hojas separadas del árbol de
limón (Citrus limon), éstas se colocaron en tubos falcon de 50 mL conteniendo agua
estéril, las hojas fueron inoculadas con los hongos del género Colletotrichum/Glomerella
a una concentración de 1 x 105 conidios mL
-1; se aplicaron 200 μL sobre el envés de las
hojas de limón, previamente desinfectadas con 1% de hipoclorito de sodio y enjuagadas
tres veces con abundante agua estéril, estos tratamientos se realizaron por triplicado y un
testigo inoculado con agua. La temperatura fue de 25° C y 85% de humedad, la medición
fue observar la presencia o ausencia de lesiones en la hoja y el crecimiento de micelio.
6.8 Pruebas de patogenicidad con taquetes de agar en hojas de limón
Para conocer el grado de patogenicidad de los aislamientos sobre hojas de Citrus limon
se utilizó la prueba propuesta por Chung et al. (2002) utilizando taquetes de agar que
contenían al hongo probado. Brevemente, los hongos de todos los géneros encontrados
fueron crecidos en PDA a 29 °C por 5 días, por otra parte las hojas fueron sometidas a
desinfección con hipoclorito de sodio al 1% por 5 min y enjuagados tres veces con
abundante agua estéril para finalmente realizar un sacabocado del hongo crecido
(taquete) y por contacto alcanzar tres puntos de la hoja, esto se llevo a cabo con 20 hojas
por cada aislamiento seleccionado. Las hojas se colocaron en cajas petri a temperatura
ambiente, con una luz fluorescente por espacio de 7 días, tomando como testigo positivo
una cepa de C. acutatum y como testigo negativo las hojas con el proceso de desinfección
pero sin inocular las superficie de la hoja (You et al., 2007). Las mediciones de infección
se llevaron a cabo con el criterio de presencia o ausencia de crecimiento de micelio sobre
las áreas tratadas a través del microscopio, contándose el número de infecciones de los
tratamientos.
6.9 Pruebas de patogenicidad en flores de limón
Después de probar la sobrevivencia de las flores por 6 días y la resistencia al daño
causado por la desinfección, se llevo a cabo un experimento cualitativo con tres levaduras

32
antagonistas: LCBG-03, LCBG--14 y LCBG-30 que mostraron las mayores y menores
capacidades de inhibición del crecimiento radial de micelio de los aislados
(Colletotrichum/Glomerella). Brevemente, se preparó una solución de conidios de 1 x 106
conidios/mL (Zulfiqar et al., 1996) del aislamiento Colletotrichum CF-6, y después de
desinfectar las flores de limón con hipoclorito de sodio al 1% por 5 min y de enjuagar
tres veces con abundante agua estéril, se procedió a empapar las flores con una solución
de levaduras a una concentración de 1 x 108 levaduras mL
-1 (Lara Rodríguez, 2006),
inmediatamente después se asperjó la solución de conidios del hongo patógeno. Para este
experimento se contaron con un testigo positivo, la infección de la flor solamente con el
patógeno, y un testigo negativo que fue la inoculación con agua. El experimento se llevo
a cabo a temperatura ambiente 25 °C por 72 h, y para cada tratamiento se usaron 3 flores
con 12 pétalos en total, para finalmente contabilizar los pétalos infectados.
6.10 Pruebas de antagonismo en placa
Una colección de levaduras nativas, previamente aisladas en la región citrícola de Padilla
Tamaulipas (Lara-Rodríguez, 2006) y estudiadas por su capacidad como agentes de
biocontrol (Pérez-Sánchez, 2007; Ramírez-González, 2008) fueron crecidas en medio
YPD (5 g L-1
de extracto de levadura, 3 g L-1
de peptona, 20 g L-1
de glucosa), empleando
matraces Erlenmeyer de 250 mL con 50 mL de YPD. Se incubaron a 34 °C con agitación
por 18 h, y se cuantificó la población en un hematocitómetro (cámara de Neubauer) en un
espectrofotómetro (GBC modelo Cintra 10e). Se ajustó una suspensión a una
concentración de 3x106 células mL
-1 y se tomaron 200 μL de cada inóculo, este fue
dispersado en placas de PDA con la ayuda de un triángulo de vidrio. Por otra parte los
presuntos hongos fitopatógenos se crecieron de forma individual, en PDA, y para la
prueba de antagonismo la placa que contenía al hongo se le hizo una horadación
cilíndrica utilizando la base de una pipeta Pasteur de vidrio estéril (4 mm de diámetro por
3 mm de altura) y se colocó en el centro de la caja que contenía a la levadura a la
concentración ya mencionada. A lo largo de 6 días se observó si el fitopatógeno era o no
capaz de crecer sobre el antagonista, y se midió diariamente el radio de crecimiento de la
colonia del hongo. El porcentaje de inhibición se estimó con base en la diferencia
obtenida entre el crecimiento obtenido de patógeno confrontado con la cepa antagónica y

33
el crecimiento de la cepa del respectivo patógeno sin antagonista, estas pruebas se
realizaron por triplicado y se reportaron los valores promedios obtenidos.
6.11. Microscopia en campo claro
Para realizar las mediciones de los conidios fue usado el programa de toma de imágenes
Image-Pro EXPRESS ver. 6.3 (Media Cybernetics, EEUU) con una cámara digital marca
Infinity1 especificamentre diseñada para las ciencias de la vida, ésta se conectó a un
microscopio Olympus BX41. Se siguieron los procedimientos del programa mencionado
y se usaron las calibraciones respectivas en la toma de mediciones. La caracterización
morfológica se realizó de acuerdo a Barnett y Hunter (1972).
6.12 Microscopia electrónica de barrido (SEM)
Para observar la capacidad de infección del presunto fitopatógeno, se realizó SEM. La
infección se realizó en hojas de limón (Citrus limon), los cuales fueron ligeramente
lesionadas con un palillo estéril y posteriormente se inocularon 20 µL de una
concentración de conidios de Glomerella/Colletotrichum de 1 x 105 conidios mL
-1 así
como el testigo, después de 6 días de incubación a 29 °C se realizó la microscopía
electrónica. Las muestras se prepararon cortando trozos de hojas de 0.5 x 0.5 cm que
presentaban una infección por crecimiento de micelio, éstas fueron fijadas por inmersión
total en solución de glutaraldehído al 5% (v/v) durante 24 h a 4 °C, en seguida las
muestras fueron deshidratadas utilizando una serie de soluciones de acetona al 30, 40, 50,
70, 80, 90 y 100%, y cubiertas con carbón y oro antes de su observación en el
Microscopio Electrónico de Barrido (JEOL JSM-5900 LV).
6.13. Análisis estadístico
Los datos de los experimentos de antagonismo fueron sometidos a un estudio de
estadística paramétrica con un análisis de varianza y la comparación de medias por el
método de Tukey (p ≤ 0.05), para ver si entre los tratamientos había diferencias
significativas. Los datos de las incidencias de patogenicidad en las hojas por el método de

34
taquete de agar fueron evaluados con una ANDEVA al final del bioensayo, se uso la
prueba de ANDEVA Kruskal-Wallis de una vía por rangos para conocer si había
diferencias entre los hongos fitopatógenos y se llevó a cabo una comparación por el
método de Dunn. Los programas utilizados para estos análisis fueron SAS 9.0 y el
Sigmastat ver 3.11 respectivamente.

35
7. RESULTADOS
7.1 Análisis morfológico
Se obtuvieron 39 aislamientos (cuadro 5) monoconidiales de hongos intracelulares,
provenientes de sintomatologías de hojas de limón (Citrus limon (L.) Osbeck).
Cuadro 5. Identificación morfológica y molecular de hongos filamentosos intracelulares obtenidos en
Citrus limon, clasificados de acuerdo al punto de muestreo y material vegetal de origen.
Muestra Tipo de tejido Aislados obtenidos
1 Pedúnculos Fusarium CF-1, Glomerella CF-11 y CF-19
2 Pedúnculos Aspergillus CF-20, Glomerella CF-12 y CF-28
3 Pedúnculos Glomerella CF-2 y Lasiodiplodia CF-21
4 Fruto amarillo Fusarium CF-3, CF-13 y CF-29, Glomerella CF-14,
Alternaria CF-38
5 Fruto partido seco Nigrospora CF-30, Fusarium CF-31
6 Fruto partido seco Fusarium CF-23, ND CF-15y CF-22
7 Fruto partido Dothideomycetes CF-7, Colletotrichum CF-6, CF-4, CF-
5, CF-24, CF-32 y CF-36 Fusarium
8 Hojas Colletotrichum CF-16, Glomerella CF-8, CF-9 y CF-17
9 Hojas Aspergillus CF-10, CF-26 y F-2, Alternaria CF-18, CF-
Lasiodiplodia 25, Pleurostoma CF-37
10 Hojas Glomerella CF-33 y CF-39, Penicillium CF-34,
Exserohilum CF-35
11 Hojas Glomerella CF-39

36
La mayoría de los aislamientos mostraron características del género Colletotrichum, en
cuanto al color del micelio éste fue en tonalidades de naranja (Figura 6).
Figura 6. Crecimiento de micelio de aislados de los géneros Colletotrichum/Glomerella obtenidos de
tejidos de limón italiano con síntomas de CFP. A) Colletotrichum CF-16, B) Glomerella CF-11 C)
Conidios de Colletotrichum CF-6, y D) Colonia de Colletotrichum CF-6 100X.
El largo de las conidias fue en promedio de 4.5 µm de ancho y 14.3 µm de largo (fig. 6),
con ambos extremos redondeados. En la figura 7 se observan algunos aspectos
macroscópicos de los hongos aislados tanto en el aspecto de color como la abundancia de
crecimiento miceliar y de esporulacion. Las tasas de crecimiento de los hongos del
género Colletotrichum y Glomerella variaron de entre 190 y 280 µm h-1
(cuadro 6), ésto
resulta útil debido a que algunas especies de Colletotrichum tienen crecimientos rápidos y
otros muy lentos por lo tanto este criterio ayuda a la identificación en conjunto con otros
aspectos morfológicos, obteniéndose que Glomerella CF-12 fue el de mayor velocidad,
mientras que y el de menor velocidad de crecimiento radial fue el aislado Glomerella CF-
8.

37
Figura 7. Morfología colonial macroscópica de los aislamientos obtenidos en las muestras de tejidos
infectados en limón italiano de Nuevo Padilla Tamaulipas.
Cuadro 6. Velocidad de crecimiento radial de los aislamientos pertenecientes a los géneros
Colletotrichum y Glomerella obtenidos de los tejidos de Citrus limon.
Género Aislamiento Velocidad de crecimiento radial
(µm/h)
Glomerella
CF-12 280
CF-19
CF-39 260
CF-11
250 CF-17
CF-28
CF-9 240
CF-33
CF-2 230
CF-14 220
CF-8 190
Colletotrichum CF-6 250

38
7.2 Identificación molecular
Se obtuvo el ADN de los 39 aislamientos de hongos de las muestras tomadas de la región
citrícola de Nuevo Padilla Tamaulipas, los cuales a través de la PCR se amplificó el gen
26S y se secuenció como prueba de identificación. Los tamaños de los fragmentos
amplificados de la región 26S fueron de entre los 574 pb y 715 pb, y el promedio fue de
662 pb (Figura 8).
Figura 8. Gel de agarosa al 1% para visualizar los productos de PCR de la amplificación de la región
26S de 17 muestras y dos testigos, uno negativo y otro positivo. Con un marcador de 1500 pares de
bases.
Las secuencias obtenidas fueron verificadas y leídas con el programa Bioedit y Mega 4,
posteriormente se llevó a cabo un análisis comparativo de la secuencias obtenida con la
base de datos del banco genómico del NCBI (National Center for Biotechnology
Information, http://www.ncbi.nlm.nih.gov/). Esto permitió la identificación de 10 géneros
que fueron las siguientes: 13 aislamientos de (Colletotrichum/Glomerella, 11
aislamientos de Fusarium, 5 aislamientos de Aspergillus, 2 aislamientos de Alternaria, un
aislamiento de Dothideomycetes, un aislamiento de Exserohilum, un aislamiento de
Lasiodiplodia, un aislamiento de Nigrospora, un aislamiento de Penicillium, un

39
aislamiento de Pleurostoma y dos aislamientos no determinados, siendo el de mayor
número los del género Colletotrichum. Las etiquetas usadas para estos aislamientos
fueron escritos con la clave CF por “Citrus Fungus” seguidos por un guión y un numero
consecutivo. En el cuadro 5 se resume el origen de cada aislado y el porcentaje de
identidad por la comparación del banco de datos se puede consultar en el cuadro 14 del
apéndice.
Se seleccionaron los aislamientos de Glomerella/Colletotrichum para realizar una prueba
de velocidad de crecimiento radial durante 6 días sobre PDA, los resultados obtenidos
muestraron ligeras diferencias como se puede observar en el cuadro 8,
7.2.1 Diferenciación molecular de especies del género Colletotrichum
Se llevó a cabo un análisis molecular para identificar la especie del género
Colletotrichum, usando los oligonucleótidos reportados por Brown (Brown et al., 1996),
dos referencias de C. gloeosporioides (aislados 6 y 20) abreviadas como C.g y dos
referencias de C. acutatum (aislado 93 y 96, pertenecientes al Lab. de Biotecnología
Vegetal del CBG) abreviadas como C.a. En la figura 9 se pueden apreciar que los hongos
aislados no pertenecen a la especie acutatum debido a que éstos no amplifican la región
que se espera según las referencias 490 pb, sin embargo amplifica una banda de
aproximadamente 450 pb muy semejante a la reportada para C.gloeosporioides por lo
tanto se descarta la presencia de C. acutatum.

40
Figura 9. Gel de agarosa al 1% donde se muestra la amplificación selectiva de un fragmento
específico del 26S utilizando los oligonucleótidos: A) CaInt2, específico para C. gleosporioides, y B)
CgInt, específico para C. acutatum. La columna M es el tamaño del marcador molecular de 1000 pb.
7.3 Pruebas de patogenicidad con hojas de limón con la prueba de taquete
Los resultados obtenidos con la prueba de taquetes que contenían micelio activo
mostraron que la capacidad de infección varía, siguiendo este orden: CF-12, CF-39, y
CF-14 con los siguientes porcentajes de infección 83.3%, 76.6%, y 51.6% (cuadro 7).
Aunque se ha descartado la presencia de C. acutatum en las cepas aisladas llevando a
cabo análisis molecular, esto no quiere decir que estos aislados no sean patogénicos, pues
han mostrado patogenicidad en las hojas de limón italiano al grado de pensar en la
posibilidad de su participación en la enfermedad de la Caída del Fruto Pequeño en los
huertos de limón de Tamaulipas. En lo que respecta a C. acutatum, su velocidad de
crecimiento es muy lenta, pero no puede descartarse su poder de infección en otros
tejidos.

41
Cuadro 7. Relación de patogenicidad de los géneros de hongos aislados en los huertos de cítricos de
Nuevo Padilla Tamaulipas
Aislamiento Relación de patogenicidad
a
% de Infección
Glomerella CF-12
83.3
Glomerella CF-39
76.6
Fusarium CF-31
73.3
Alternaria CF-38
68.3
Glomerella CF-14
51.6
Dothideomycetes CF-7
36.6
Glomerella CF-28
31.6
C. acutatum GA
30
Glomerella CF-9
26.6
Penicillium CF-34
20
Exserohilum CF-35
20
Pleurostoma CF-37
16.6
ND CF-22
16.6
Colletotrichum CF-16
15
Aspergillus CF-25
10
Lasiodiplodia CF-21
0
Nigrospora CF-30
0 a De acuerdo al método de Dunn (P<0.05)
7.4 Visualización de la infección por microscopía electrónica de barrido
Mediante microscopia electrónica de barrido se pudo observar la colonización sobre el
tejido vegetal de hojas de limón, (fig. 10), en esta imagen se observa la esporulación del
hongo y el crecimiento de micelio sobre la herida realizada, y tambien se puede apreciar,
de acuerdo a la referencia de medida, que algunos conidios son ligeramente mayores a 10
µm como se reporta en la literatura para este género.
Si bien se observa el crecimiento de micelio en la superficie dañada de la hoja, sin
embargo también se observa crecimiento sobre los tejidos no dañados, esto prueba la
capacidad de estos hongos para infectar las hojas de limón italiano (Figs. 11 y 12). En
algunos casos algunos hongos tienen mayor crecimiento de micelio como en la fig. 12b,
que corresponde al aislamiento Glomerella CF-11 este crecimiento también se extiende a
áreas donde no hay daño físico del tejido.

42
Figura 10. Fotografías de microscopía electrónica de barrido del crecimiento de micelio en superficie
herida de la hoja de limón a los 6 días, izquierda) Glomerella CF-14, derecha) Glomerella CF-11.
7.5 Pruebas de antagonismo in vivo
Se realizó una prueba preliminar con los aislamientos Colletotrichum/Glomerella sobre
las hojas de limón a una concentración de 1 x 105 conidias mL
-1, (Duran et al., 2004)
después de 11 días, una de cada 3 hojas había sido infectada es decir el 33% de las hojas,
siendo el aislado Glomerella CF-14 el de mayor crecimiento de micelio, y de manera
cualitativa se escogieron dos aislamientos más que presentaron mayor patogenicidad, en
este caso el aislado Colletotrichum CF-6 y el aislado Glomerella CF-12, éstos aislados
fueron usadas para llevar a cabo las pruebas de antagonismo contra una colección de
levaduras aisladas en la misma región citrícola con las claves: LCBG-03, LCBG-14,
LCBG-23, LCBG-24, LCBG-27, LCBG-28 y LCBG-30, además de la cepa de referencia
denominada CIB-A17 (Debaryomyces hansenii), perteneciente a la colección de
levaduras marinas del CIBNOR.

43
Figura 11. Fotografías de microscopia electrónica de barrido del crecimiento de micelio en superficie de una hoja de limón a los 6 días a) Glomerella
CF-39, b) Glomerella CF-12, y c) Glomerella CF-14.
Figura 12. Fotografías de microscopia electrónica de barrido de comparación de la densidad del crecimiento micelial sobre las heridas en una hoja de
limón de dos aislados y un testigo a los 6 días a) C. acutatum b) Glomerella CF-11, c) Glomerella CF-14.

44
7.6. Pruebas de antagonismo in vitro
Las pruebas de antagonismo llevadas a cabo en cajas petri dieron como resultado una
clasificación entre las levaduras de acuerdo al porcentaje de inhibición de los hongos
presuntos agentes causales de la caída del fruto pequeño, en el cuadro 10 se concentra la
información obtenida en el experimento donde se observa el mejor comportamiento es la
levadura LCBG-03 con un porcentaje de inhibición de crecimiento radial del micelio de
93%, cabe mencionar que las levaduras que inhiben en un porcentaje mayor al 50% son
considerados como buenos agentes de biocontrol.
Figura 13. Confrontación en placa con la levadura LCBG-03 contra: A) Glomerella CF-14, B)
Glomerella CF-8, y C) Colleotrichum CF-6.
Después de realizar el análisis ANDEVA y una comparación de medias por el método de
Tukey, entre tratamientos con las levaduras y hongos, se separaron en 11 grupos donde
el grupo “I” fue formado por el tratamiento T11 (LCBG-03 vs Glomerella CF-8) (cuadro
11), y fue el de mejor desempeño, y el grupo subsecuente también se encontraba la
levadura LCBG-03. Esto confirma que esta levadura tienen una capacidad aceptable como
agente de biocontrol, además reportes para esta especie reportan que ha sido probado ser
no patogénico en cerdos y ratones (Arras et al., 1999).

45
Cuadro 8. Porcentaje de inhibición de fitopatógenos en pruebas de antagonismo in vitro.
Hongo fitopatógeno – Levadura antagonista
Pruebas de antagonismo
% Inhibicióna
Colletotrichum CF-6 vs LCBG-03 93 ± 1.6
Colletotrichum CF- 6 vs LCBG- 27 92 ± 2.1
Colletotrichum CF-6 vs CIB-A17 91 ± 1
Colletotrichum CF-6 vs LCBG- 30 89 ± 2.1
Colletotrichum CF-6 vs LCBG- 24 87 ± 1.2
Colletotrichum CF-6 vs LCBG- 28 86 ± 0.0
Colletotrichum CF-6 vs LCBG-23 58 ± 10.6
Colletotrichum CF-6 vs LCBG- 14 38 ± 3
Glomerella CF-8 vs LCBG-03 92 ± 1.2
Glomerella CF-8 vs LCBG- 27 89 ± 3
Glomerella CF-8 vs LCBG-30 87 ± 2.4
Glomerella CF-8 vs LCBG-24 85 ± 2.1
Glomerella CF-8 vs LCBG- 28 79 ± 3.2
Glomerella CF-8 vs CIB -A17 64 ± 1.2
Glomerella CF-8 vs LCBG-14 62 ± 3.8
Glomerella CF-8 vs LCBG- 23 41 ± 10.5
Glomerella CF-14 vs LCBG-03 92 ± 0.0
Glomerella CF-14 vs LCBG- 28 88 ± 1.2
Glomerella CF-14 vs LCBG- 23 87 ± 2.1
Glomerella CF-14 vs A-17 84 ± 3.7
Glomerella CF-14 vs LCBG- 30 84 ± 2.1
Glomerella CF-14 vs LCBG-24 82 ± 1.2
Glomerella CF-14 vs CIB- A27 74 ± 6
Glomerella CF-14 vs LCBG- 14 35 ± 2.6
a Valor promedio ± desviación estándar

46
La metodología estándar para probar patogenicidad de Colletotrichum ha sido con hojas
en la mayoría de los casos, por la dificultad de obtener flores fuera de la temporada, sin
embargo, las flores son una de las principales vías de infección para los frutos, ya que a
través de los pétalos los hongos pueden alojarse en el fruto y causar daño en él, no
obstante es importante comprobar la resistencia de las flores despegadas del árbol para
observar si tienen algún cambio después de un tiempo que pueda confundir el
experimento de infección, por consiguiente los resultados obtenidos en este experimento
(Fig. 14) mostraron que las flores no presentaron daños después de 6 días a temperatura
ambiente y aun después de haber sido desinfectadas con hipoclorito se sodio.
Figura 14. Prueba de supervivencia de flores de limón de Tamaulipas en agua estéril por 6 días,
donde las flores se mantienen en buen estado después del tiempo de prueba, no hay lesiones en las
estructuras florales como se puede observar en la imagen.
El desarrollo de una prueba cualitativa de antagonismo con los agentes de biocontrol y
los presuntos patógenos agentes causales del fruto pequeño fue llevada a cabo. En la
figura 15 se puede apreciar el efecto del tratamiento con levaduras y hongos después de
72 h de tratamiento con las flores de limón.

47
Figura 15. Prueba cualitativa de antagonismo entre levaduras y hongos en flores de limones a las 72
h de inoculación.
Los resultados indican que la levadura con mayor capacidad de biocontrol fue la LCBG-
03 como se puede observar en el cuadro 9, donde se observa una menor infección en los
pétalos, seguido de la levadura LCBG-14 y finalmente la levadura LCBG-30.
Cuadro 9. Prueba cualitativa de protección con levaduras antagonistas y el aislamiento
Colletotrichum CF-6.
Levadura Número de
pétalos infectados Porcentaje de inhibición (%)
LCBG-03 5 58
LCBG-14 6 50
LCBG-30 10 17
Testigo positivo (sin levadura,
solamente Colletotrichum CF-6)
12 0
Testigo negativo (agua estéril) 0 100

48
7.7 Comprobación de los principios de Koch
Un fitopatógeno es un organismo capaz de causar enfermedad y completar su ciclo de
vida en un hospedante. Por lo tanto, las estructuras del patógeno deben germinar en la
superficie del hospedante y la hifa resultante penetrara el tejido, colonizará, alterará la
fisiología y causará la muerte de las células. Finalmente, el organismo debe reproducirse
y dispersarse (Sexton y Howlett, 2006) cumpliendo con los postulados de Koch. En éste
estudio, después de haber infectado pétalos de limón italiano, se obtuvo nuevamente un
aislado del fitopatógeno en una caja petri como se puede apreciar en la Figura 16, donde
se confirma claramente el crecimiento y la esporulación del aislamiento Colletotrichum
CF-6.
Figura 16. Comprobación de infección yreaislamiento del patógeno inoculado en la prueba con flores
de limón. Se observa el crecimiento abundante y con el color salmón típico de Colletotrichum.
Entonces, los resultados presentados en esta sección muestran que en las muestras
analizadas no se encontró el agente causal de la caída del fruto pequeño Colletotrichum
acutatum, sin embargo los aislados más patogénicos encontrados son principalmente los
del genero Glomerella/Colletotrichum, que pueden infectar los pétalos de limón italiano,
ésto es relevante debido a que en el ataque de los pétalos se inicia el proceso de infección
para la posterior la caída del fruto pequeño. Por otra parte las pruebas de antagonismo
mostraron que la levadura LCBG-03 ejerce mayor efectividad como agente de biocontrol
para el género Glomerella/Colletotrichum.

49
8. DISCUSIÓN
En éste trabajo, se llevó a cabo un diagnostico del agente causal de la caída del fruto
pequeño, en los huertos de limón italiano ubicados en Nuevo Padilla Tamaulipas, así
como también un análisis de patogenicidad in vivo, en hojas de limón, las pruebas de
antagonismo in vitro, usando como agentes de biocontrol una colección de levaduras
previamente aisladas en los huertos de esta misma región y como presuntos patógenos
involucrados en la CFP los aislamientos de Colletotrichum/Glomerella.
8.1 Diagnóstico de la caída del fruto pequeño
Históricamente, C. gloeosporioides había sido descrito como un hongo con muchas
variantes morfológicas (Sonoda y Pelosi, 1988). Otros autores (Agostini et al., 1992;
Bonde et al., 1991) también notaron diferentes cepas en morfología, crecimiento y
patogenicidad a flores de limón persa (Citrus latifolia). Agostini et al., (1992) y Sonoda
y Pelosi (1988) indicaron que tres cepas diferentes de C. gloeosporioides se encontraban
en cítricos. El primero era saprófito, de crecimiento rápido de color gris (FGG) por sus
siglas en inglés “Fast growing gray” y no era responsable de la CFP, este es el agente
causal de antracnosis en poscosecha (Timmer et al., 1998). La segunda cepa causa
antracnosis en hojas inmaduras, frutos y flores de limón mexicano (Citrus aurantifolia).
La tercera cepa, que se ha reportado como el agente causal de la CFP en todos los cítricos
(Timmer et al., 1998), es una forma especializada de C. gloeosporioides (Fagan, 1979) y
está referido por Agostini et al., (1992) y Sonoda y Pelosi (1988) como una cepa de lento
crecimiento y de color naranja (SGO) por sus siglas en ingles “Slow Growing orange”,
produciendo mayormente micelio blanco con masas conidiales naranjas. La segunda cepa
y la tercera son ahora consideradas como C. acutatum (Brown et al., 1996). En este
estudio se identificaron aislamientos correspondientes a Colletotrichum gloeosporioides
y a su teleomorfo Glomerella cingulata, así como otros géneros de hongos que al parecer
no tienen una relación con la caída del fruto de los cítricos, sin embargo se han reportado
como patógenos en cítricos tal es el caso de Alternaria, Fusarium, Aspergillus y
Penicillium. Las cepas de C. acutatum y C. gloeosporioides son muy similares y ha sido
difícil separarlos por una metodología tradicional taxonómica, por ejemplo en cuanto a la

50
morfología de los conidios se ha reportado que C. acutatum crecido en PDA estas tienen
extremos agudos (Wharton y Diéguez, 2004). Aislamientos de Tamaulipas en limón
mexicano (Citrus aurantifolia) indican que para C. acutatum que causa la caída del fruto
pequeño en naranja dulce y limón persa (C. latifolia), los conidios presentan una mayor
proporción con un lado fusiforme y otro redondeado, mientras que para C.
gloeosporioides los conidios tienen los lados redondeados (Orozco-Santos et al., 2008).
Los resultados obtenidos en este estudio para C. gloeosporioides presentan la morfología
de sus conidios con ambos lados redondeados de manera similar a lo que se ha reportado
en la literatura, esto se puede observar en la figura 6. Los resultados obtenidos mostrados
en la figura 9, también fueron similares a los realizados por Brown et al., (1996),
analizando una región de amplificación del 26S que diferencia claramente a la especie
acutatum de gloeosporioides que permitió confirmar los datos por morfología, quedando
claro que en los aislamientos no se encontró C. acutatum. Otro criterio de clasificación es
la velocidad de crecimiento; un experimento similar llevado a cabo por Orozco-Santos et
al., (2004) con una cepa de C. acutatum aislado del limo mexicano (Citrus aurantifolia)
se observaron velocidades de 174 µm h-1
en medio de PDA, comparados a las
velocidades de entre 190 y 280 µm h-1
en aislamientos de Colletotrichum/Glomerella
obtenidos en este estudio, la velocidad es ligeramente mayor, ésto confirma la cepa de
rápido crecimiento. Sin embargo Timmer et al., (1992) reportaron que la velocidad de C.
gloeosporiodes es de 2 o 3 veces más rápida que la de C. acutatum. Kuramae-Izioka et
al., (1997) obtuvieron velocidades en promedio de 380 µm h-1
sobre PDA a menor
temperatura; ésto demuestra la dificultad para clasificar los hongos en cuando a
morfología, por consiguiente las pruebas moleculares son más precisas (Brown et al.,
1996).
8.2 Análisis de patogenicidad
Los aislamientos monoconidiales obtenidos en este estudio a partir de frutos y hojas
sintomáticas, fueron en su mayoría géneros de hongos reportados como patógenos en
cítricos (Timmer et al., 2002; Tournas y Katsoudas, 2005). Estudios de infección en

51
plántulas de limón italiano, han demostrado la colonización de Penicillium spp. así como
Aspergillus spp. como hongos endofíticos (Duran et al., 2004). Fagan (1979) aisló
consistentemente los hongos C. gloeosporioides y Fusarium spp., de yemas florales
infectadas y de frutos jóvenes de cítricos, determinando a través de pruebas de
patogenicidad que la enfermedad era inducida por una forma especializada de C.
gloeosporioides y encontró a Fusarium spp., probablemente como un colonizador
secundario de tejido fisiológicamente debilitado por ataques de C. gloeosporioides, lo
cual coincide con nuestros resultados ya que el porcentaje de aislamientos de Fusarium
es abundante hasta en un 85% con respecto a los aislamientos de Colletotrichum, además
de mostrar una infección un 73% en hojas de limón. En un estudio de hongos asociados a
la CFP llevado a cabo por Arias-Rivas et al. (2006) en la cual fue aislado Rhizopus sp. en
las temporadas de presencia de la enfermedad de CFP, éste se descartó que fuese el
agente causal debido a su naturaleza saprófita y que por lo general se presenta en tejidos
afectados con otros hongos, además de que el daño que causa es referido a frutos en
poscosecha. En este estudio también se aislaron hongos de los géneros Aspergillus y
Alternaria mismos que son reportados como patógenos en poscosecha (Ochoa et al.,
2007).
Timmer et al. (1992) comprobó que la cepa de crecimiento rápido Colletotrichum
gloeosporioides no infecto flores ni tejido vivo. En nuestro estudio las cepas fueron
capaces de crecer en los tejidos vivos de hojas y cuando se inoculó en las flores de limón,
éstas fueron infectadas rápidamente, lo que les confiere a éstos hongos una capacidad de
infección mayor al reportado por otros autores. Sin embargo, en pruebas prelimanes de
patogenicidad en frutos, al utilizar el aislado Glomerella CF-28 sobre frutos de limón
italiano, éste fue capaz de infectar el flavedo y esporular de manera abundante en él
después de 15 días a temperatura ambiente, con lo cual se demostró que el aislado CF-28
es capaz de causar una antracnosis típica de poscosecha.
De acuerdo a los estudios de patogenicidad podemos afirmar que más del 80% de los
aislamientos tienen efectos patogénicos a las hojas de limón, siendo las más patogénicas:

52
Glomerella CF-12, Glomerella CF-39, así como Fusarium CF-31, Aspergillus CF-38 y
Glomerella CF-14 (Cuadro 9).
8.3 Pruebas de antagonismo
En este trabajo se demuestra que la levadura epifítica LCBG-03 aislada de los huertos de
cítricos en Nuevo Padilla inhibe el crecimiento radial de los hongos patógenos del género
Colletotrichum/Glomerella (aislamientos CF-6, CF-8, y CF-14), ésta levadura tuvo el
mejor desempeño como biocontrolador tanto in vitro como in vivo. La capacidad
antagónica de algunas cepas de levaduras hacia hongos fitopatógenos se puede definir
con base en la destrucción total o parcial de las poblaciones de patógenos. Esta capacidad
es el resultado de la agresividad del antagonista y de la susceptibilidad del patógeno
(Quiroz–Sarmiento et al., 2008).
Por otra parte varias cepas de P. guilliermondii fueron usados en estudios similares a éste
y han demostrado que tienen una eficacia en el control biológico contra varios hongos de
frutos cítricos, pomelos, manzanas, peras, uvas y fresas (Arras et al., 1999; Lima et al.,
1999). En este trabajo encontramos la primera evidencia de que P. guilliermondii puede
controlar a Glomerella/Colletotrichum en las confrontaciones antagónicas in vitro hasta
un 93% de inhibición e in vivo en flores de limón italiano (cuadros 8 y 9,
respectivamente). Experimentos similares llevados a cabo en frutos de limón italiano
dieron como resultado que las cepas LCBG-03 y en menor grado la levadura LCBG-30,
tuvieron un desempeño comparable o superior al recubrimiento fungicida químico
utilizado de manera estándar por el empacador (De la Cruz Arguijo, 2006). Los
resultados indican que LCBG-03 tiene el más alto potencial para ser agentes de
biocontrol contra los hongos Glomerella/Colletotrichum en hojas y flores de limón
italiano. Sin embargo no hay reportes que aislados de ésta especie, P. guilliermondii, se
haya usado como agente de biocontrol contra el hongo Colletotrichum/Glomerella.

53
Los mecanismos involucrados en el control biológico son varios, e incluyen entre otros,
inducción de resistencia, competición por nutrientes y secreción de compuestos
inhibitorios (Guetsky et al., 2002). Un estudio previo con P. guilliermondii demostró que
esta levadura libera metabolitos al medio extracelular, debido a la presencia de las
paredes celulares de Penicillium sp, y tienen la capacidad de inhibir temporalmente la
formación del tubo germinal en las esporas en P. digitatum. (Pérez Sánchez, 2007). Las
quitinasas y β-1,3- glucanasas hidrolizan las paredes de las células de los hongos e
inhiben el crecimiento de muchos hongos patógenos (Schlumbaum et al., 1986; Sela–
Buurlage et al., 1993). Es posible que estas enzimas hidrolíticas de P. guilliermondii
jueguen un rol importante en la degradación de las paredes de los hongos
Colletotrichum/Glomerella, especialmente porque se ha demostrado que las levaduras se
adhieren a la hifa del patógeno. Modos similares de acción son los que se enfatizan en
otras levaduras antagonistas incluyendo los productos comerciales (Droby et al., 1998;
Droby, 2006).
La información sobre los modos de acción es esencial para aumentar las posibilidades de
que esta levadura se utiliza con éxito para el control biológico, por ejemplo, el modo de
comprensión de la acción puede facilitar el registro para uso comercial y puede ser útil
para optimizar los sistemas de formulación. Por otra parte, P. guilliermondii ha
demostrado que no es tóxico y aceptado por muchos investigadores como el agente de
control biológico de muchas podredumbres de poscosecha de frutas, (Arras et al., 1999;
Wisniewski et al., 1991). Los resultados sugieren que P. guilliermondii podrá ser uno de
los agentes de control biológico de la CFP a escala piloto en los huertos de limón italiano
en la región citrícola de Tamaulipas.

54
9. CONCLUSIONES:
En el presente trabajo se realizaron aislamientos de hongos a partir de muestras
sintomáticas de hojas y frutos de limón italiano de dos huertos localizados en Nuevo
Padilla (Tamaulipas). Los hongos encontrados pertenecieron en su mayoría al género
Glomerella / Colletotrichum, y de otros géneros como Fusarium, Aspergillus, Alternaria
y Penicillium, pero no se detectó al agente causal reportado en la literatura de la caída del
fruto pequeño que es Colletotrichum acutatum. Esto no es una determinación de que este
fitopatógeno no esté presente en los huertos, sin embargo este resultado es benéfico para
los agricultores al mostrar que por lo menos en estos huertos no está presente de manera
consistente. Sin embargo las cepas aisladas mostraron una cierta patogenicidad cuando se
inocularon en hojas y cuando el aislado Colletotrichum CF-6 infectó a las flores de
limón, mientras que en las pruebas de infección en hojas por aspersión los aislados más
patogénicos fueron los Glomerella CF-12, CF-39, y CF-14.
Por otra parte la colección de levaduras que fueron probadas como agentes de biocontrol
en placa de antagonismo contra 3 cepas de Glomerella / Colletotrichum (CF-14, CF-8 y
CF-6) dando como resultado un porcentaje de inhibición de crecimiento de micelio de
entre un 35 a 93% siendo el de mejor desempeño la levadura CBG-03 identificada
previamente como Pichia guilliermondii que ha sido probada con resultados promisorios
en frutos y ahora en flores. Esto confirma el éxito de biocontrol de esta levadura nativa de
la región citrícola de Nuevo Padilla, y la levadura LCBG-30 presentó una menor
capacidad como agente de biocontrol comparado con el antagonismo con hongos de
poscosecha previamente estudiados.

55
10. RECOMENDACIONES
En este trabajo de llevó a cabo un diagnostico y biocontrol de hongos fitopatógenos
aislados con agentes de biocontrol nativos de la misma región. Los cuales en su mayoría
han mostrado resultados positivos y estos deben de probarse en campo con diferentes
formulaciones. Esto resultaría innovador ya que hasta ahora los agentes de biocontrol
para precosecha son escasos, sin embargo es tiempo de llevar a cabo estudios con
comparación con diferentes fungicidas sintéticos para determinar la eficacia con respecto
a estos en la etapa de precosecha y su repercusión en poscosecha.

56
11. BIBLIOGRAFÍA
Agostini J. P., Timmer L. W., Mitchell D. J. 1992. Morphological and pathological
characteristics of strais of Colletotrichum gloeosporioides from citrus.
Phytopathology 82: 1377-1382.
Agostini J.P., Gottwald T.R., Timmer L.W. 1993. Temporal and spatial dynamics of
postbloom fruit drop in Florida. Phytopathology 82: 1377-1382.
Arias Rivas B., Yáñez V., Carrizales L., Sánchez M. 2006. Hongos asociados a la caída
prematura de frutos en lima persa (Citrus latifolia tan.) y evaluación de su control
químico. Bioagro 18(1): 31-39.
Arras G., Nicolussi P., Ligios C. 1999. Non-toxicity of some antifungal yeasts (Pichia
guilliermondii, Rhodotorula glutinis and Candida oleophila) in laboratory animals.
Annali di Microbiologia ed Enzimologia 49: 125-131.
Bar-Shimon M., Yehuda H., Cohen L., Weiss B., Kobeshnikov A., Daus A., Goldway
M., Wisniewski M., Droby S. 2004. Characterization of extracellular lytic enzymes
produced by the yeast biocontrol agent Candida oleophila. Current Genetics 45:
140-148.
Barnett H.L., Hunter B.B. 1972. Illustrated genera of imperfect fungi. Burgess Publishing
Company, 3rd
edition, MI (USA). 241 pp.
Bonde M.R., Peterson G.L., Maas J.L. 1991. Izozyme comparisons for identification of
Colletotrichum species pathogenic to strawberry. Phytopathology 81: 1523-1529.
Brown A.E., Sreenivasaprasad S., Timmer L. W. 1996. Molecular characterization of
slow-growing orange and Key lime anthracnose strains of Colletotrichum from
citrus as C. acutatum. Phytopathology 86 (5): 523-527.
Campbell R. 1989. Biological control of microbial plant pathogens. En: Biocontrol of
diseases of flowers and fruits. 1ª Edition. Great Britain. Pp. 161-168.
Chung K.-R., Shilts T., Li W., Timmer L.W. 2002. Engineering a genetic transformation
system for Colletotrichum acutatum, the causal fungus of lime anthracnose and
postbloom fruit drop of citrus. FEMS Microbiol. Letters 213: 33-39.
Chung K.-R., Shilts T., Ertürk Ü., Timmer L. W., Ueng P.P. 2003. Indole derivatives
produced by the fungus Colletotrichum acutatum, causing lime anthracnose and
postbloom fruit drop of citrus. FEMS Microbiology Letters 226: 23-30.
De la Cruz Arguijo E. 2006. Antagonismo in vivo de levaduras contra mohos causantes
de pudriciones poscosecha en cítricos. Tesis de licenciatura de Químico
farmacéutico biólogo. Universidad Autónoma de Tamaulipas. 51 p.
Droby S., Cohen L., Daus A., Weiss B., Horev B., Chalutz E., Katz H., Keren-Tzur M.,
Shachnai A. 1998. Commercial Testing of Aspire: a yeast preparation for the
biological control of postharvest decay of citrus. Biological Control 12 (2): 97–101.
Droby S. 2006. Yeast Metschnikowia fructicola NRRL Y-30752 for inhibiting
deleterious microorganisms on plants. US Patent 6994849.

57
Duran E.L., Ploper L.D., Ramallo J.C., Azevedo J.L. 2004. Ensayos de inoculación in
vitro de Colletotrichum gloeosporioides Aislado de hojas asintomáticas de Citrus
limón. Boletin Micológico 19: 81-86.
Fagan H.J. 1979. Postbloom fruit drop, a new disease associated with a form of
Colletotrichum gloeosporioides. Annals of Applied Biology 91:13-20.
Fernández C., Juncosa R. 2002. Biopesticidas: ¿La agricultura del futuro?. Phytoma 141:
14-19.
Guetsky R., Shtienberg D., Elad Y., Fischer E., Dinoor A. 2002. Improving biological
control by combining biocontrol agents each with several mechanisms of disease
suppression Phytopathology 92: 976-985.
Hernández Lauzardo A. N., Bautista Baños S., Velázquez del Valle M. G., Hernández
Rodríguez A. 2007. Uso de microorganismos antagonistas en el control de
enfermedades postcosecha en frutos. Revista Mexicana de Fitopatología 25 (001):
66-74.
Kupper K.C., Gimenes-Fernandes N., Goes A. 2003. Controle biológico de
Colletotrichum acutatum, agente causal da queda prematura dos frutos cítricos.
Fitopatología brasileira 28 (3): 251-257.
Kuramae-Izioka E.E., Lopes C.R., Souza N.L., Machado M.A. 1997. Morphological and
molecular characterization of Colletotrichum spp. from citrus orchards affected by
postbloom fruit drop in Brazil. European Journal of Plant Pathology 103: 323-329.
Lahey K.A., Yuan R., Burns J.K., Ueng P.P., Timmer L.W., Chung K. R. 2004. Induction
of phytohormones and differential gene expression in citrus flowers infected by the
fungus Colletotrichum acutatum. Plant Microbe-Interact 17: 1394-1401.
Lara Rodríguez E. 2006. Aislamiento y caracterización de levaduras antagonistas de
hongos fitopatógenos post-cosecha de cítricos. Tesis de Maestría en Ciencias en
Biotecnología Genómica, Centro de Biotecnología Genómica, Instituto Politécnico
Nacional. Reynosa, Tamaulipas México. 62 p.
Lima G., Arru S., De Curtis F., Arras G. 1999. Influence of antagonist, host fruit and
pathogen on the biological control of postharvest fungal diseases by yeasts. Journal
of Industrial Microbiology and Biotechnology 23: 223-229.
Ochoa J.L., Hernández Montiel L.G., Latisnere Barragan H., León de la Luz J.L.,
Larralde Corona C.P. 2007. Aislamiento e identificación de hongos patógenos de
naranja Citrus sinensis L. osbeck cultivada en Baja California Sur. México. Ciencia
y Tecnología Alimentaria 5: 352-359.
Orozco-Santos M., Manzo-Sánchez G., Guzmán-González S., Farías-Larios J., Timmer
L. W. 2004. Crecimiento y Cambios Morfológicos de Colletotrichum acutatum
Simmonds, Agente Causal de la Antracnosis del Limón Mexicano (Citrus
aurantifolia Christm. Swingle) Incubado en Diferentes Medios de Cultivo Sólido y
Líquido. Revista Mexicana de Fitopatología 22 (003): 423-428.
Orozco-Santos M., Robles-González M.M., Vázquez-Jiménez J.L, Timmer L.W. 2008.
Biología y manejo integrado de antracnosis de los cítricos en México. Memorias de

58
la segunda semana internacional de la citricultura, 24–28 de noviembre, Instituto
Nacional de Investigaciones Forestales, Agrícolas y Pecuarias. Campo
Experimental Tecomán. Tecomán, Colima, México.
Peres N.A., Mackenzie S.J., Peever T. L., Timmer L.W. 2008. Postbloom fruit drop of
citrus and Key lime anthracnose are caused by distinct phylogenetic lineages of
Colletotrichum acutatum. Phylopathology 98: 345-352.
Pérez Sánchez G. 2007. Identificación de EST’s Diferenciales de Pichia guilliermondii
durante la inducción con paredes celulares de Penicillium sp. Tesis de Maestría en
Ciencias en Biotecnología Genómica, Centro de Biotecnología Genómica, Instituto
Politécnico Nacional. Reynosa, Tamaulipas México. 51 p.
Petersson S., Schnurer J. 1995. Biocontrol of mold growth in high-moisture wheat stored
under airtight conditions by Pichia anomala, Pichia guilliermondii, and
Saccharomyces cerevisiae. Applied and Environmental Microbiology 61 (3):
1027-1032.
Quiroz-Sarmiento V.F., Ferrera-Cerrato R., Alarcon A., Lara Hernández M.E. 2008.
Antagonismo in vitro de cepas de Aspergillus y Trichoderma hacia hongos
filamentosos que afectan al cultivo del ajo. Revista Mexicana de Micología 26: 27-
34.
Ramírez González M.S. 2008. Análisis del perfil génico de Pichia guilliermondii durante
su interacción in vivo con Penicillium digitatum. Tesis de Maestría en Ciencias en
Biotecnología Genómica, Centro de Biotecnología Genómica, Instituto Politécnico
Nacional. Reynosa, Tamaulipas. México. 78 p.
Rodríguez Tovar A., Xoconostle Cásarez B.,y Valdés M. 2004. Ecología molecular de los
hongos ectomicorrizicos. Revista Fitotecnia Mexicana 27 (3): 267-278.
Ruíz E., Coronado J.M., Myartseva S.N. 2006. Situación actual del manejo de las plagas
de los cítricos en Tamaulipas, México. Manejo Integrado de Plagas y Agroecología
78: 74-100.
Schlumbaum A., Mauch F., Vogeli U., Boller T. 1986. Plant chitinases are potent
inhibitors of fungal growth. Nature 324: 365-367.
Sonoda R.M., Pelosi R. R. 1988. Characteristics of Colletotrichum gloeosporioides from
lesions on citrus blossoms in the Indian River of Florida. Proc Fla State Hortic Soc
101: 36-38.
Sela-Buurlage M.B., Ponstein A.S., Bres-Vloemans B., Melchers L.O., Van den Elzen,
P., Cornelissen B.J.C. 1993. Only specific tabacco chitinases and β-1,3-glucanases
exhibit antifungal activity. Plant Physiology 101: 857-863.
Sexton A. C., Howlett B.J. 2006. Parallels in fungal pathogenesis on plant and animal
host. Eukariotic Cell 12: 1941-1949.
Soriano del Castillo J. M. 2007. Micotoxinas en Alimentos. Ediciones Díaz de Santos.
396 p.
Timmer L.W., Zitko S.E. 1992. Timing of fungicide applications for control of
postbloom fruit drop of citrus in Florida. Plant Disease 76: 820-823.

59
Timmer L.W., Agostini, J.P., Zitko S.E., Zulfiqar M. 1994. Postbloom Fruit Drop, an
increasingly prevalent disease of citrus in the Americas. Plant Disease 74 (4): 329-
334.
Timmer L.W., Brown G.E., Zitko S.E. 1998. The role of Colletotrichum spp. in
postharvest anthracnose of citrus and survival of C. acutatum on fruit. Plant Dis.
82:415-418.
Timmer L.W., Gransey S.M., Graham J.H. 2002. Plagas y enfermedades de los cítricos.
Segunda edición. The American Phytopathological Society, St. Paul, 96 p.
Timmer L.W., Mondal S.N., Peres N.A.R., Bhatia A. 2004. Fungal diseases of fruit and
foliage of citrus trees. Diseases of Fruits and Vegetables I: 191-227.
Timmer L.W., Orozco-Santos M. 2005. V Congreso Argentino de Citricultura Concordia,
Entre Rios, Argentina 30 de Noviembre al 2 de Diciembre del 2005.
Tournas V. H., Katsoudas E. 2005. Mould and yeast flora in fresh berries, grapes and
citrus fruits. International Journal of Food Microbiology 105 (1): 11-17.
Trillas M.I., Casanova E., Cotxarrera L., Orgovás J., Borrero C., Avilés M. 2006.
Compost from agricultural waste and the Trichoderma asperellum strain T-34
suppress Rhizoctonia solani in cucumber seedlings. Biological Control 39: 32-38.
Wharton P., Diéguez J. 2004. The biology of Colletotrichum acutatum. Anales del Jardín
Botánico de Madrid 61 (1): 3-22.
Wisniewski M., Biles C., Droby S., MeLaughlin R., Wilson C., Chalutz E. 1991. Mode of
actin of the postharvest biocontrol yeast, Pichia guilliermondii. I. Characterization
of attachment to Botrytis cinerea. Physiological and Molecular Plant Pathology 39:
245-258.
You B.J., Choquer M., Chung K.R. 2007. The Colletotrichum acutatum gene encoding a
putative pH-responsive transcription regulator is a key virulence determinant during
fungal pathogenesis on citrus. The American Phytopathological Society 20(9):
1149–1160.
Zermeño-González A., García-Delgado M.A., Castro-Meza B.I., Rodríguez-Rodríguez
H.R. 2007. Tensión de humedad del suelo y rendimiento de fruto en limón italiano.
Revista Fitotecnia 30(3): 295-303.
Zulfiqar M., Brlansky R. H., Timmer L.W. 1996. Infection of flower and vegetative
tissues of citrus by Colletotrichum acutatum and C. gloeosporioides. The New
York Botanical Garden. Mycologia 88 (1): 121-128.
Páginas electrónicas consultadas
Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación
(SAGARPA). 2010. Disponible en http://www.sagarpa.gob.mx. Fecha de consulta:
23 de Octubre de 2009.

60
Secretaría de Desarrollo Rural. 2006. Disponible en
http://www.tamaulipas.gob.mx/saladeprensa/boletines/boletin.asp?no_bol=131&fec
ha=23/10/2006&secre=SDRUR. Fecha de consulta: 23 de Octubre de 2009.
http://www.ncbi.nlm.nih.gov/)
http://www.apsnet.org/online/common/names/citrus.asp

61
12. APÉNDICE
Cuadro 10. Análisis de varianza para la variable crecimiento radial, diseño completamente al azar
con un nivel de confianza del 95%.
Suma de Cuadrados
Fuente de Variación DF cuadrados medios F-Valor Pr > F
Tratamientos 26 90.22610617 3.47023485 99.35** <.0001
Error 54 1.88613333 0.03492840
Total 80 92.11223951
CV = 17.96%
Cuadro 11. Comparación de medias del radio de la colonia a los 6 días por el método de Tukey.
AGRUPAMIENTO MEDIA N TRATAMIENTO
A 3.8200 3 T1 (Colletotrichum CF-6)
A 3.6000 3 T19 (Glomerella CF-14)
A 3.3000 3 T10 (Glomerella CF-8)
B 2.3667 3 T3 (LEV-14 vs Colletotrichum CF-6)
C B 2.0833 3 T21 (LEV-14 vs Glomerella CF-14)
C D 1.6333 3 T15 (LEV-23 vs Glomerella CF-8)
C D E 1.5000 3 T6 (LEV-23 vs Colletotrichum CF-6)
F D E 1.2500 3 T12 (LEV-14 vs Glomerella CF-8)
F G E 0.9667 3 T13 (LEV-17 vs Glomerella CF-8)
F G H 0.8667 3 T23 (LEV-27 vs Glomerella CF-14)
I G H 0.5667 3 T17 (LEV-28 vs Glomerella CF-8)
I G H 0.5167 3 T22 (LEV-17 vs Glomerella CF-14)
I G H 0.5000 3 T8 (LEV-30 vs Glomerella CF-8)
I G H 0.5000 3 T27 (LEV-30 vs Glomerella CF14)
I G H 0.4667 3 T7 (LEV-24 vs Colletotrichum CF-6)
I G H 0.4000 3 T16 (LEV-24 vs Glomerella CF-8)
I G H 0.4000 3 T9 (LEV-30 vs Colletotrichum CF-6)
I G H 0.4000 3 T24 (LEV-23 vs Glomerella CF-14)
I H 0.3667 3 T14 (LEV-27 vs Glomerella CF-8)
I H 0.3667 3 T25 (LEV-24 vs Glomerella CF-14)
I H 0.3667 3 T26 (LEV-28 vs Glomerella CF-14)
I H 0.3667 3 T18 (LEV-30 vs Glomerella CF-8)
I H 0.3500 3 T4 (LEV-17 vs Colletotrichum CF-6)
I H 0.3000 3 T5 (LEV-27 vs Colletotrichum CF-6)
I H 0.3000 3 T20 (LCBG-03 vs Glomerella CF-14)
I H 0.2833 3 T2 (LCBG-03 vs Colletotrichum CF-6)
I 0.2667 3 T11 (LCBG-03 vs Glomerella CF-8)
Medias con la misma letra no son significativamente diferentes. α = 0.05

62
Cuadro 12. Análisis estadístico no paramétrico para la relación de patogenicidad por la prueba de
Kruskal-Wallis de una vía
Grupo N M
CF-21 30 0 CF-22 30 0 CF-25 30 0 CF-30 30 0 CF-31 30 0 CF-35 30 0 CF-37 30 0 CF-38 60 0 CF-16 60 0 CF-7 60 0
CF-34 60 0 CF-9 60 0
CF-12 60 0 CF-14 60 0 CF-28 60 0 CF-39 60 0
A 60 0
Grupo Media 25% 75%
CF-21 0 0 0
CF-22 0 0 0
CF-25 0 0 0
CF-30 0 0 0
CF-31 1 0 1
CF-35 0 0 0
CF-37 0 0 0
CF-38 1 0 1
CF-16 0 0 0
CF-7 0 0 1
CF-34 0 0 0
CF-9 0 0 1
CF-12 1 1 1
CF-14 1 0 1
CF-28 0 0 1
CF-39 1 1 1
A 0 0 1

63
Cuadro 13. Comparación de múltiples por pares mediante el procedimiento de Dunn
Comparación Diferencia de rangos p* Q** P<0.05
CF-12 vs CF-30 337.5 17 7.69 Yes
CF-12 vs CF-21 337.5 16 7.69 Yes
CF-12 vs CF-25 297 15 6.76 Yes
CF-12 vs CF-16 276.75 14 7.72 Yes
CF-12 vs CF-22 270 13 6.15 Yes
CF-12 vs CF-37 270 12 6.15 Yes
CF-12 vs CF-35 256.5 11 5.84 Yes
CF-12 vs CF-34 256.5 10 7.16 Yes
CF-12 vs CF-9 229.5 9 6.4 Yes
CF-12 vs A 216 8 6.03 Yes
CF-12 vs CF-28 209.25 7 5.84 Yes
CF-12 vs CF-7 189 6 5.27 Yes
CF-12 vs CF-14 128.25 5 3.58 Yes
CF-12 vs CF-38 60.75 4 1.69 No
CF-12 vs CF-31 40.5 3 0.92 No
CF-12 vs CF-39 27 2 0.75 No
CF-39 vs CF-30 310.5 16 7.07 Yes
CF-39 vs CF-21 310.5 15 7.07 Yes
CF-39 vs CF-25 270 14 6.15 Yes
CF-39 vs CF-16 249.75 13 6.97 Yes
CF-39 vs CF-22 243 12 5.53 Yes
CF-39 vs CF-37 243 11 5.53 Yes
CF-39 vs CF-35 229.5 10 5.23 Yes
CF-39 vs CF-34 229.5 9 6.4 Yes
CF-39 vs CF-9 202.5 8 5.65 Yes
CF-39 vs A 189 7 5.27 Yes
CF-39 vs CF-28 182.25 6 5.08 Yes
CF-39 vs CF-7 162 5 4.52 Yes
CF-39 vs CF-14 101.25 4 2.82 No
CF-39 vs CF-38 33.75 3 0.94 No
CF-39 vs CF-31 13.5 2 0.31 No
CF-31 vs CF-30 297 15 5.86 Yes
CF-31 vs CF-21 297 14 5.86 Yes
CF-31 vs CF-25 256.5 13 5.06 Yes
CF-31 vs CF-16 236.25 12 5.38 Yes
CF-31 vs CF-22 229.5 11 4.53 Yes
CF-31 vs CF-37 229.5 10 4.53 Yes
CF-31 vs CF-35 216 9 4.26 Yes
CF-31 vs CF-34 216 8 4.92 Yes
CF-31 vs CF-9 189 7 4.3 Yes
CF-31 vs A 175.5 6 4 Yes

64
CF-31 vs CF-28 168.75 5 3.84 Yes
CF-31 vs CF-7 148.5 4 3.38 No
CF-31 vs CF-14 87.75 3 2 No
CF-31 vs CF-38 20.25 2 0.46 No
CF-38 vs CF-30 276.75 14 6.3 Yes
CF-38 vs CF-21 276.75 13 6.3 Yes
CF-38 vs CF-25 236.25 12 5.38 Yes
CF-38 vs CF-16 216 11 6.03 Yes
CF-38 vs CF-22 209.25 10 4.77 Yes
CF-38 vs CF-37 209.25 9 4.77 Yes
CF-38 vs CF-35 195.75 8 4.46 Yes
CF-38 vs CF-34 195.75 7 5.46 Yes
CF-38 vs CF-9 168.75 6 4.71 Yes
CF-38 vs A 155.25 5 4.33 Yes
CF-38 vs CF-28 148.5 4 4.14 Yes
CF-38 vs CF-7 128.25 3 3.58 No
CF-38 vs CF-14 67.5 2 1.88 No
CF-14 vs CF-30 209.25 13 4.77 Yes
CF-14 vs CF-21 209.25 12 4.77 Yes
CF-14 vs CF-25 168.75 11 3.84 Yes
CF-14 vs CF-16 148.5 10 4.14 Yes
CF-14 vs CF-22 141.75 9 3.23 No
CF-14 vs CF-37 141.75 8 3.23 No
CF-14 vs CF-35 128.25 7 2.92 No
CF-14 vs CF-34 128.25 6 3.58 No
CF-14 vs CF-9 101.25 5 2.82 No
CF-14 vs A 87.75 4 2.45 No
CF-14 vs CF-28 81 3 2.26 No
CF-14 vs CF-7 60.75 2 1.69 No
CF-7 vs CF-30 148.5 12 3.38 No
CF-7 vs CF-21 148.5 11 3.38 No
CF-7 vs CF-25 108 10 2.46 No
CF-7 vs CF-16 87.75 9 2.45 No
CF-7 vs CF-22 81 8 1.84 No
CF-7 vs CF-37 81 7 1.84 No
CF-7 vs CF-35 67.5 6 1.54 No
CF-7 vs CF-34 67.5 5 1.88 No
CF-7 vs CF-9 40.5 4 1.13 No
CF-7 vs A 27 3 0.75 No
CF-7 vs CF-28 20.25 2 0.56 No
CF-28 vs CF-30 128.25 11 2.92 No
CF-28 vs CF-21 128.25 10 2.92 No
CF-28 vs CF-25 87.75 9 2 No

65
CF-28 vs CF-16 67.5 8 1.88 No
CF-28 vs CF-22 60.75 7 1.38 No
CF-28 vs CF-37 60.75 6 1.38 No
CF-28 vs CF-35 47.25 5 1.08 No
CF-28 vs CF-34 47.25 4 1.32 No
CF-28 vs CF-9 20.25 3 0.56 No
CF-28 vs A 6.75 2 0.19 No
A vs CF-30 121.5 10 2.77 No
A vs CF-21 121.5 9 2.77 No
A vs CF-25 81 8 1.84 No
A vs CF-16 60.75 7 1.69 No
A vs CF-22 54 6 1.23 No
A vs CF-37 54 5 1.23 No
A vs CF-35 40.5 4 0.92 No
A vs CF-34 40.5 3 1.13 No
A vs CF-9 13.5 2 0.38 No
CF-9 vs CF-30 108 9 2.46 No
CF-9 vs CF-21 108 8 2.46 No
CF-9 vs CF-25 67.5 7 1.54 No
CF-9 vs CF-16 47.25 6 1.32 No
CF-9 vs CF-22 40.5 5 0.92 No
CF-9 vs CF-37 40.5 4 0.92 No
CF-9 vs CF-35 27 3 0.61 No
CF-9 vs CF-34 27 2 0.75 No
CF-34 vs CF-30 81 8 1.84 No
CF-34 vs CF-21 81 7 1.84 No
CF-34 vs CF-25 40.5 6 0.92 No
CF-34 vs CF-16 20.25 5 0.56 No
CF-34 vs CF-22 13.5 4 0.31 No
CF-34 vs CF-37 13.5 3 0.31 No
CF-34 vs CF-35 0 2 0 No
CF-35 vs CF-30 81 7 1.6 No
CF-35 vs CF-21 81 6 1.6 No
CF-35 vs CF-25 40.5 5 0.8 No
CF-35 vs CF-16 20.25 4 0.46 No
CF-35 vs CF-22 13.5 3 0.27 No
CF-35 vs CF-37 13.5 2 0.27 No
CF-37 vs CF-30 67.5 6 1.33 No
CF-37 vs CF-21 67.5 5 1.33 No
CF-37 vs CF-25 27 4 0.53 No
CF-37 vs CF-16 6.75 3 0.15 No
CF-37 vs CF-22 0 2 0 No
CF-22 vs CF-30 67.5 5 1.33 No

66
CF-22 vs CF-21 67.5 4 1.33 No
CF-22 vs CF-25 27 3 0.53 No
CF-22 vs CF-16 6.75 2 0.15 No
CF-16 vs CF-30 60.75 4 1.38 No
CF-16 vs CF-21 60.75 3 1.38 No
CF-16 vs CF-25 20.25 2 0.46 No
CF-25 vs CF-30 40.5 3 0.8 No
CF-25 vs CF-21 40.5 2 0.8 No
CF-21 vs CF-30 0 2 0 No
*p = Número de comparaciones
**Q = Estadístico de Prueba
A= C. acutatum

67
Cuadro 14. Porcentaje de identidad de los aislados fúngicos de Citrus limon en base a la
secuenciación de su región D1/D2 (26S).
Etiqueta Nombre del aislado referenciado
en el GenBank
Porcentaje de
identidad (%)
CF-1 Fusarium (EF453193) 100
CF-2 Glomerella (DQ286183) 99
C F-3 Fusarium (EF453171) 96
CF-4 Fusarium ( EF453193) 99
CF-5 Fusarium ( EF453193) 100
CF-6 Colletotrichum (FJ890373) 99
CF-7 Dothideomycetes (GQ153063) 96
CF-8 Glomerella (DQ286183) 99
CF-9 Glomerella (DQ286183) 100
CF-10 Aspergillus (AB363747) 97
CF-11 Glomerella (DQ286183) 100
CF-12 Glomerella (DQ286183) 100
CF-13 Fusarium (EF453193) 99
CF-14 Glomerella (DQ286183) 99
CF-15 ND ND
CF-16 Colletotrichum (EU552111) 84
CF-17 Glomerella (DQ286183) 100
CF-18 Alternaria (GQ865634) 95
CF-19 Glomerella (DQ286183) 99
CF-20 Aspergillus (GQ382274) 99
CF-21 Lasiodiplodia (FN645641) 99
CF-22 ND ND
CF-23 Fusarium (EF453171) 100
CF-24 Fusarium (AY234909) 100
CF-25 Aspergillus (AB363747) 100

68
Continuación…. Cuadro 14. Porcentaje de identidad de los aislados fúngicos de Citrus limon en base a la
secuenciación de su región D1/D2 (26S).
Etiqueta Nombre del aislado referenciado
en el GenBank
Porcentaje de
identidad (%)
CF-26 Aspergillus (AB363747) 99
CF-27 Aspergillus (AB363747) 99
CF-28 Glomerella (DQ286183) 100
CF-29 Fusarium ( EF453171) 100
CF-30 Nigrospora (GQ328855) 100
CF-31 Fusarium (EF453171) 100
CF-32 Fusarium (EF453171) 98
CF-33 Glomerella (DQ286183) 99
CF-34 Penicillium (GQ169739) 89
CF-35 Exserohilum (AB245087) 90
CF-36 Fusarium (AY234909) 100
CF-37 Pleurostoma (AB363797) 99
CF-38 Alternaria (FJ755240) 100
CF-39 Glomerella (DQ286183) 100

69
Cuadro 15. Secuencias del 26 S de los aislamientos de los hongos intracelulares de Citrus limon en
tejidos con síntomas de infección tipo caída del fruto pequeño.
CF- 1 Fusarium
AGGCCATTGCCCTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCTCGG
GCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGAACGGG
ACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTTCGACG
AGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAATACCG
GCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGAGA
GTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGGTTAAT
CATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGGGGAT
AAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCTGGCG
GGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTTGAAA
AAGGCGCACAAACCAAATCGCCAGATCTTGCAGATGCGCGAACCTCAGTCCCCGCCAGGGTA
TTACGCAACGGGCTATACACTCCCGGAGAGAGCCCATTCCCGAAGCCTTTATCCCGGGGGAAA
CTGAT
CF-2 Glomerella
CGGGGCATTGCCTCAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCC
AGGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCG
ACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATA
CCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAG
AGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGT
GAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCG
GGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCC
TTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTCT
GAAACACGGGCCAAAAACATGCCAGCATCCTTGCGGAGCGCGTACCTCAGCCCGCCGAAGGG
TATTGTGCACAGGCTATAACACTCCCCGAAGAGAGCTACTTCCTGAAGCTTTTGGCCCGACAG
CGAGCTGATGCTGGCCTGGAC
CF-3 Fusarium
ATGACGTTTTGCCTTAGTACCGGCGAAGTGAACGGCAACGCTCAATTCGAATCTAGCTCTGGG
CCCAGTCGTAATTGTAGAGGATGTTTCCGTGCGGTGCTTCCGAGTTCCCTGGACGGGACGCCA
TAGAGGGTAGAGCCAGTCCGGTCGGACGCAAATTCCGTAAAGCTCCTCGACGAGTCGAGTAG
TTCAGGATGCTGCTCTAACGGAGGTATTGTCTCTAAAGCYAATACCGGCCAGAGACCGATAGC
GCACAAGTAGAGTGATCGAAAGATGATAAGCACTTTGATTAGAGAGTTAAAAAGTACGTGAA
ATTGTTGATAGGGAAGCGTTTATGACCAGACTCGGGCTCGGATAATCATCTGGGGTTCTCCCC
AGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTTCGCCGGGGGGAAAAGGGTTTCGGGAAT
GTGGCTCTCTCCGGGGGTGTGTTATAGCCCGTTTGCGTAATACCCGGGCGGGGACTGAGGTTC
GCGCATCTGCAARGATGCTGGCGTAATGGTCATCAACGACCGCCGAAAGAGAAAAAAACAAG
GCCAGATCTTTGGAAAAGCGCGAACCTCAGTCCCCGCAGGGTATTACGCACGGGCTATACACT
CCCGGAGAGAGCACATTCCCGAAGCTTTATCCCTGGSAAAACTGATGTGGC

70
CF-4 Fusarium
ATGGGCATTGCCCTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCTCG
GGCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGAACGG
GACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTTCGAC
GAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAATACC
GGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGAG
AGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGGTTAA
TCATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGGGGAT
AAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCTGGCG
GGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCTTGAA
CACACGGACCAGATTACGCCAGCATCCTTGAGATGCGCGAACCTCAGTCCCGCCAGGTATACC
CAACGGCTATAACCTCCCGGAGAAGCCCATTCCGAGCTTATCCCGGGAAAACTGATTGGCCGG
CA
CF-5 Fusarium
AAGGTATTGCCCTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCTCGG
GCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGAACGGG
ACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTTCGACG
AGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAATACCG
GCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGAGA
GTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGGTTAAT
CATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGGGGAT
AAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCTGGCG
GGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCTGAGC
ACCCCGGGCCTAAGATCCGCCAGATCTTGCAGATGCGCGAACCTCAGTCCCCGCCAGGGTATT
ACGCACGGGCTATACACTCCCCGGAGAGAGCACATTCCCGAAGCCTTATCCCCGCGAAACCTG
ATGCTGCCTG
CF- 6 Colletotrichum
CCGGGCATTGCCTCAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCT
AGGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCG
ACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATA
CCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAG
AGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGT
GAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCG
GGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGGTTGCATAATACC
CTTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTC
TAAAAACACTACCAAAAAGGCCAGTTCCTTGCGGAGCGCGTACCTCAGCCCCCGAAGGTATT
ATGCACAGGCTATACACTCCCGAAGAGAGCTACGTTTCTGAAGCTTTTGTCCCCGAACGCAAA
CTGATGCTGGCCTGAGCC
CF-7 Dothideomycetes
CTGAGGTATATGCTTCTTGTAACGGCGTGGTGAACAGCAATAGCTTAAATTTGATATCTGGCG
TCTTCGARGTCGAGTTGTAATTGTAGAGGACGTTCTGAGTAACCACCGACCMAGTTCCTCGGA
CAGGAGTCATAGAGGGTAGAATCCGTATGCGGTCGGAAGGGCCTAACGTAGCTCCTCGACGA
GTCGAGTCTTGGGAAGCAGCTCTAATGGGAGGTAAATTCTTCTAAGCTAAATATTGGCCAGAG
ACCGATAGCGCACAAGTAGAGTGTCGAAAATGAAAAGCACTTTGGAAGAGAGTTAAAAAGCA
CGTGAAATGTTAAAGGGAAGGGATWCAACCAGATTGCTCGCGGTTTCCGCCGGCTTCTACCG

71
GTCACTCGCCGCGTTCAGGCAGCATCGTCTGGTCCGCTGGTAAACTTGAGGAWGTAGCTCCCT
CGGAGGGTATAGCCTCTAGGATGAGCGAGCGCCGGGCGAGTCCGCGCTCGGTAGAAGCTGCG
TAAGGTCGATCCGCCTCCGAAAAAAAACAAACAAGCACGCATCTAGCGAACGGGCTCGCCGC
GTCGTGCTCAAAGGTATAAATCCAGGGACTCATTTAATCTATCGGGCCCAAGTTTGGTGGC
CF-8 Glomerella
TCAGGCATTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCCA
GGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACGG
GACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATAC
CGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGA
GGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGTG
AATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGG
GGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCT
TCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTCTG
ACAAACACGGGCCCACATGTGCCAGCATCCTTGCGGAGCGGCGTACCTCAGCCCGCCGAAGG
TATTGTGCAACAGGCTATACACTCCCGAAGAGAGCTACGTTCCTGAAGCTTTTGTCCCGACAG
CGAGCTGATGCTGGCTGAGCCGGCAGTC
CF-9 Glomerella
ACGAGGTATTGCCTCAGTACGGCGAAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCC
CAGGCCCGAGTTGTAATTTTGCAGAGGATGCTTTTCGGTGCGGTGCCTTCCAAGTTCCCTAGA
ACGGGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCT
TCGACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAA
ATACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAA
AGAGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCG
GTGAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGT
CGGGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATAC
CCTTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCGCC
AAAAAACGGCAAAAAAGGCCAGATTTTTGCGGAGCGCGTACCTCAGCCCGCCGAAGGGTATT
GAGCACAGGCTATACACTCCCCGAAGAGAGCTACGTTCCTGAAGCTTTTTGTCCCCGACAGCG
AGCTGATGCTGGGCTG
CF-10 Aspergillus
ACAGCGGAAAGGCTCAGTAACGGCGTGAGGAAGCGGCAATGCTCAAATTTGAATACTGGCTC
CTTCGGAATTCTAAGTAATTTGCAGAGGTTGCTCTGGGTGCGGCCCCGTCTAAGTGCCCTGGA
ACGGGCCGTCAGAGAGGGTGAGAATCCCGTCTTGGGCGGGGTGTCCGTGCCCGTGTAAAGCT
CCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAAAGC
TAAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTG
AAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCGCCC
GCGGGGTTCAGCCGGCATTCGTGCCGGTTACTTCCCCGTGGGCGGGCCAGCGTCGGTTTGGGC
GGCCGGTCAAAGGCCCCTGGAAGTAGTACCCTCCGGGGTACCTTATAGCCAGGGGTGCAATG
CGGCCAGCCTGGACCGAGGAACGCGCTTCGGCACGGACGCTGGCATAATGGTCGTAAACGCC
GTCGAAAAAAGACCAACCAATGCCAGCGTCGTGCGAAGCGCGTTCCTCGTCAGCTGGCCGCA
TTGCACCCCTGGCTATAAGGTACCCGAGGTACTCATTCCAGGGCTTTGACGGCGCCAACCGAC

72
CF-11Glomerella
AACAGGTATTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCC
AGGCCCGAGTTTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACGG
GACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATAC
CGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGA
GGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGTG
AATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGG
GGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCT
TCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGCTG
AAAACCCGGGCAAAATGTGCCAGATCCTTGGGAGCGGGACCTTCACCCCCCAAGGTATTGTG
AACGGGTATAAACTCCCCGAAAAAGCTCTTCTGAATTTTGTCCCAAAGCCACTGATCTGCCTT
ACGGC
CF-12 Glomerella
TCGTCCATTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCCAG
GCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACGGG
ACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGAC
GAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATACC
GGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGAG
GGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGTGA
ATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGGG
GACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCTT
CGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGCTGA
AAAACCGGAACCAAAGTGCCAGCATCTTGCGAACGCGTACCTCACCCGCCAAAGGTATGTGC
ACAGCTATACCTCCCCGAGAGACTACTTCCTGAACTTTTGCCCCACGCCACTAGCCTGCTTAAC
CGGC
CF-13 Fusarium
AAGAGGTATTGCCCTAGTAACGGCGAAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCT
CTCGGGCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGA
ACGGGACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTT
CGACGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAA
TACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAA
GAGAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGG
ATAATCATCTGGGGTTCTCTCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGG
GGATAAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCT
GGCGGGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTC
GAAAATGACGCACAAACCAAATGCCCAGATCTTGCAGATGCGCGAACCTCAGTCCCCGCCAA
GGTATTACGCAACGGGCTATACACTCCCGGAGAGAGCCCATTCCCGGAGCTTTTTCCCCGGGG
GAAACTGAT
CF-14 Glomerella
AGCACGTATGGCCTCAGTAACGGCGAAGTGAAGCGGCACAGCTCAAATTTGAATCAGGCCCC
AGGCCCGAGTTGTATTTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGA

73
CGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTTAAAGCTAAATACC
GGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATAAAAGCACTTTGAAAGAGGG
TTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGGGAAT
CACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGGGGA
CAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCTTCG
GCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCGCTCGAAA
AAAAAAAAACCATATGCCCCATCTTGCGGAACGCCGACCTCAGCCCGCAAAGGTATGTGCGC
GGTATACATCCTCGAAGAGACTCGTTCTGAACCTTTGTCCCGACGGATGAGCTGCTG
CF-15 ND
ACAGGGGCAATGCCTCAGTACGGCGAGTGAAGCGGCAAGAGCTCAAATTTGAAAGCTGGCTC
CTTCGGAGTCCGCATTGTAATTTGCAGAGGATGCTTTGGGTGCGGCCCCCGTCTAAGTGCCCT
GGAACGGGCCGTCAGAGAGGGTGAGAATCCCGTCTTGGGCGGGGTGTCCGTGCCCGTGTAAA
GCTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAA
AGCTAAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACT
TTGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCG
CCCGCGGGGTTCAGCCGGCATTCGTGCCGGTGTACTTCCCCGTGGGCGGGCCAGCGTCGGTTT
GGGCGGCCGGTCAAAGGCCCCTGGAATGTAGTGCCCTCCGGGGCACCTTATAGCCAGGGGTG
CAATGCGGCCAGCCTGGACCGAGGAACGCGCTTCGGCACGGACGCTGGCATAATGGTCGTAA
ACGACCGTCTGAAAACCCGGGCACAATGCCAGCGTCGTGCCGAAGCCGTTCCTCGTCCAGCTG
GCGCATGCACCCTTGGTATAAGTGCCCGGAGGACTTCTTCAAGGGCTTTTACCGGCCCAACC
CF- 16 Colletotrichum
CCGGGCATTGCCTCAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCT
AGGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCG
ACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATA
CCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAG
AGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGT
GAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCG
GGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGGTTGCATAATACC
CTTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTC
TAAAAACACTACCAAAAAGGCCAGTTCCTTGCGGAGCGCGTACCTCAGCCCCCGAAGGTATT
ATGCACAGGCTATACACTCCCGAAGAGAGCTACGTTTCTGAAGCTTTTGTCCCCGAACGCAAA
CTGATGCTGGCCTGAGCC
CF-17 Glomerella
CCAGTGTCATTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCC
AGGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCG
ACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATA
CCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAG
AGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGT
GAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCG

74
GGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCC
TTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTCT
TAAAACCCGGACAACGTGTCAGCATCTTGTGGAAGTGCGTACCTCAGCCCGCCCAAGGGTATT
GTGCAACAGGCTATAACACTCCCGAAGAGAGCTACGTTCTGAAGCTTTTGTCCCCGACGATGG
CTGATGCTG
CF-18 Alternaria
CCCGGGTATTGCCCTAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCT
TTTAGAGTCCGAGTTGRAATTTGCAGAGGGCGCTTTGGCTTTGGCAGCGGTCCAAGTTCCTTG
GAACAGGACGTCACAGAGGGTGAGAATCCCGTACGTGGTCGCTGGCTATTGCCGTGTAAAGC
CCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGAGGTACATTTCTTCTAAAG
CTAAATATTGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTT
GGAAAGAGAGTCAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCAGCCAGACTTGCT
TACAGTTGCTCATCCGGGTTTCTACCCGGTGCACTCTTCTGTAGGCAGGCCAGCATCAGTTTGG
GCGGTAGGATAAAGGTCTCTGTCACGTACCTCCTTTCGGGGAGGCCTTATAGGGGAGACGACA
TACTACCAGCCTGGACTGAGGTCCGCGCATCTGCTAGGATGCTGGCGTAATGGCTGTAAGCGG
CCCGTCTTGAAACACAAGGAC
CF-19 Glomerella
ACGAGGTATTGCCTCAGTACGGCGAAGTGAAGCGGCACAGCTCAAATTTGAAATCTGGCCCC
AGGCCCGAGTTGTAATTAGCAGAAGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACG
GGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCG
ACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATA
CCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAG
AGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGT
GAATCACCCAGCTCTCGCGGCTGGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTC
GGGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACC
CTTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGCT
GAAAACCCCGGCAAAAATTGCCACTTCTTGCGAACGCGACCTCACCGCCAAAGGGATTGTGC
AAAGGTATACMYTCCCGAAAAGCTACTTTCTGAACTTTTTCCCGAAGCACCGATGTGCCGAAC
C
CF-20 Aspergillus
ACGGGGGGTATTGGCCTCAGTAACGGCGTGGTGAACGGCAGTGCTCAAATTTGAAGCTTGGCT
CCTTCGGAGTYGTATTGTAATTTGCAGAGGATGCTTTGGGTGCGGCCCCCGTCTAAGTGCCCT
GGAACGGGCCGTCAGAGAGGGTAGAATCCCGTCTCGGGCGGGGTGTCCGTGCCCGTGTAAGC
TCCTTCGACGAGTCGAGTCGTTTAGGATGCAGCTCTAAATGGGTGGTAAATTTCATTAAAGCT
AAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGGATCGAAAGATAAAAGCACTTTGAAA
AGAGAGTTAAACAGCACGTGAATTGTTGAAAGGGAGCGCTTGCGACCAGACTCGCCCGCGGG
GTTCAGCCGGCATTCGTCCGGTTACTTCCCCGGGGCGGGCCAGCGTCGGTTTGGGGGCCGGTC
AAGGCCCCGGGAATGAGGGCCTCCGGGGCACCTTATAGCCAGGGGTGCAATGCGGCCAGCCT
GGACCGAGAACGCGCTTCGCACGACGTGGCATAATGGTCGTAAACGACCGTCAAAAACGGAC
AAACAAAGCAGCGTCGTGCGAGCCGTCCTCGGTCAGGTGCCGATGACCCGGTATAAGTGCCC
GAGGGATCTTCCGGGCTTGAGGCGCCAAGAAC

75
CF-21 Lasiodiplodia
GCGGGGTATTGCCTTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAAGCTGGCCCTT
TTAGGGTCCGCGTTGTAATTTGTAGAGGATGATTCGGCGAGGGCTCCTGCCTAAGTCCCCTGG
AACGGGGCGTCATAGAGGGTGAGAATCCCGTATGCGGTAGGTTGCCTTAGCCATGTGAATCTC
CTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGAGGTAAATTTCTTCTAAAGCT
AAATACTGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGG
AAAGAGAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGCTTGCAACCAGACTTGTCCG
CAGTTGCTCAGCCGGTCTCCTGACCGGCGTACTCTTCTGCGGCCAGGCCAGCATCAGTTCGGG
CGGTCGGATAAAGGCCTCGGGAATGTAGCTCCTCTCGGGGAGTGTTATAGCCCGGGGTGGAA
TGCGACCAGCCTGGACTGAGGATCTCGCTTCGGCAAGGATGCTGGCGTAATGGTTGTAAGCGG
CCCGTCTGAAAAACCCGAACAACAAAGTTCACCTTTTCGGCCAGCAYCCTTGCGAAASSGAGG
TCCTCAGTCCGGGGGGGTCGAATTCCCCCCGGGGTTTAAACTCCCCAGAAGGGGATTCATTCC
CAAGCCTTTTTCC
CF-22 ND
ACTGGGTGATTGCCTCAGTAACGGCGAAGTGAACGGCAAGAGCTCAAATTTGAAAGCTGGCT
CCTTCGGGGTTCGTATGTAATTTTGCAGAGGATGCTTCGGGAGCGGCCCCCATCTAAGTGCCC
TGGAACGGGCCGTCATAGAGGGTGAAAATCCCGTCTGGGATGGGGTGTCCGCGCCCGTGTGA
AGCTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTA
AAGCTAAATATTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCAC
TTTGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAGGGGAAGCGCTTGCGAACAGACTC
GCCCACGGGGTTCAGCCGGCATTCGTGCGGGTGTACTTCCCCGCGGGCGGCCAGCGTCGGTTT
GGGCGGCCGGTCAAGGGCCCTCGGAATGTAACGCCCCCCGGGGCGTCTTATAGCCGAGGGTG
CCTTGCGGCCAGCCCAGACGGAGGGACGCGCTTCGGTTCGGACGCTGGGATAATGGTCGTAA
GCGCCCTGTAAAAAAAAACGGAACAAGGRSSTYYAACRAAMRSTTYCYKGGTRGGSYKGSCS
MATGGCCCATACTTTAAAAGGCCCCGGGGGTTGGTTTCCAGGGCTTTRACGGCCCCAAMCMR
MSG
CF-23 Fusarium.
ACGGGCCATTGCCTCAGTACGGCGAGTGAAGCGGCAAGAGCTCAAATTTGAAAGCTGGCTCC
TTCGGGGTCCGCATTGTAATTTGCAGAGGATGCTTCGGGAGCGGCCCCCATCTAAGTGCCCTG
GAACGGGCCGTCATAGAGGGTGAAAATCCCGTCTGGGATGGGGTGTCCGCGCCCGTGTGAAG
CTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAAA
GCTAAATATTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTT
TGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCGC
CCACGGGGTTCAGCCGGCATTCGTGCCGGTGTACTTCCCCGCGGGCGGGCCAGCGTCGGTTTG
GGCGGCCGGTCAAAGGCCCTCGGAATGTAACGCCCCCCGGGGCGTCTTATAGCCGAGGGTGC
CATGCGGCCAGCCCAGACCGAGGAACGCGCTTCGGCTCGGACGCTGGCATAATGGTCGTAAG
CGACCCGTCTGAAAAACCCGGAACAAA
CF-24 Fusarium
TCGGGCCATTGCCCTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCTC
GGGCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGAACG
GGACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAATAC

76
CGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGA
GAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGGTTA
ATCATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGGGG
ATAAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCTGG
CGGGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCTTG
AAACCAGGGACACTGCTGCTCCGGATCTTGCGATGCGCCACCTCATCCCCGCGGGGATTCGAA
CGGCTTAACCTCCCCGAAAAGCCCTTTCCAACCCTTTCCCCGGGGAAACGATGTGGC
CF-25 Aspergillus
ACCGGGGGATTGCCTCAGTACGGCGAGTGAAGCGGCAAGAGCTCAAATTTGAAAGCTGGCTC
CTTCGGAGTCCGCATTGTAATTTGCAGAGGATGCTTTGGGTGCGGCCCCCGTCTAAGTGCCCT
GGAACGGGCCGTCAGAGAGGGTGAGAATCCCGTCTTGGGCGGGGTGTCCGTGCCCGTGTAAA
GCTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAA
AGCTAAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACT
TTGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCG
CCCGCGGGGTTCAGCCGGCATTCGTGCCGGTGTACTTCCCCGTGGGCGGGCCAGCGTCGGTTT
GGGCGGCCGGTCAAAGGCCCCTGGAATGTAGTACCCTCCGGGGTACCTTATAGCCAGGGGTG
CAATGCGGCCAGCCTGGACCGAGGAACGCGCTTCGGCACGGACGCTGGCATAATGGTCGTAA
ACGACCCGTCTTGAAAAACCGGGCACAAAAGATGCCAGCGTCGTGCCGAAGCCGTTCCTCGG
TCAGGTGGCCGCATTGTGCCCCTGGCTATAAGGTCCCCGAAGGTATTCCTTCAGGGGCTTTTA
CCGG
CF-26 Aspergillus
AACGGGGATGGCCTCAGTAACGGCGAAGTGAAGCGGCAAGAGCTCAAATTTGAAAGCTGGCT
CCTTCGGAGTTGGAATTGTATTTTGCAGAGGATGCTTTGGGTGCGGCCCCCGTCTAAGTGCCCT
GGAACGGGCCGTCAGAGAGGGTGAGAATCCCGTCTTGGGCGGGGTGTCCGTGCCCGTGTAAA
GCTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAA
AGCTAAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACT
TTGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCG
CCCGCGGGGTTCAGCCGGCATTCGTGCCGGTGTACTTCCCCGTGGGCGGGCCAGCGTCGGTTT
GGGCGGCCGGTCAAAGGCCCCTGGAATGTAGTACCCTCCGGGGTACCTTATAGCCAGGGGTG
CAATGCGGCCAGCCTGGACCGAGGAACGCGCTTCGGCACGGACGCTGGCATAATGGTCGTAA
ACGACCCGTCTTAAAACACGGACAACCAATTGGCCAGCGTCGTGCGAAGCGCGTTCCTCGGGT
CAGGCTGGCCGCATTGCACCCCTGGCTATAAGGTACCCGGAGGTACTCATTTCAGGGGCTTTG
ACGGCCCCCCAAC
CF-27 Aspergillus
CCCGGGGCATTGCCTCAGTAACGGCGAGTGAAGCGGCAAGAGCTCAAATTTGAAAGCTGGCT
CCTTCGGAATTTGAGTTGTCATTTGCAGAGGATGCTTTGGGTGCGGCCCCCCGTTTAGTGCCCT
GGAACGGGCCGTCAGAGAGGGTGAGAATCCCGTCTTGGGCGGGGTGTCCGTGCCCGTGTAAA
GCTCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAA
AGCTAAATACTGGCCGGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACT
TTGAAAAGAGAGTTAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCGACCAGACTCG
CCCGCGGGGTTCAGCCGGCATTCGTGCCGGTGTACTTCCCCGTGGGCGGGCCAGCGTCGGTTT

77
GGGCGGCCGGTCAAAGGCCCCTGGAATGTAGTACCCTCCGGGGTACCTTATAGCCAGGGGTG
CAATGCGGCCAGCCTGGACCGAGGAACGCGCTTCGGCACGGACGCTGGCATAATGGTCGTAA
ACGACCCGTCTAAAAAACCGGCCAATGCGCAGCGTCGTGCGAAGCGCGTTCCTCGTCCAGCTG
GCCGCATTGCACCCCTGGCTATAAGGTACCCGAGGTACTCATTTCAGGGCTTTGACGCCC
CF-28 Glomerella
TCGGGTCATTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCCCA
GGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACGG
GACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATAC
CGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGA
GGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGTG
AATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGG
GGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCT
TCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTCTG
AAACACGGACCAGTGTGCCAGCATCTTGCGAACGCGTACTCGCCGCCAAGGTATTGGCACAG
TATACATTCCCGAAGAGGCTACGTCCGAACTTTTGTCCCCAAGCCATGATGCTGCCG
CF-29 Fusarium
CAAGGGCCATTGCCCTAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCT
CTCGGGCCCGAGTTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGA
ACGGGACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTT
CGACGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAA
TACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAA
GAGAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGG
TTAATCATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGG
GGATAAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCT
GGCGGGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCT
RAMMMSCRSRRMMAMAAYTCTCCRSSWYYKTGCTRATSCSCGAACCTYAKTCCCCGCMGGGT
ATTACGCMACGGGCTATAACACTYYCCGAGAGAGCACAWTYCCGAAGCYTTTWTCCCSGSRA
AM
CF-30 Nigrospora
AGGGTATTCCCCTAGTACGGCGAGTGAAGCGGGAACAGCTCAAATTTGAAATCTGGCCCTCG
GGTCCGAGTTGTAATTTGTAGAGGATGCTTTTGGTGCGGTGCCTTCCGAGTTCCCTCGGAACG
GGACGCCTTAGAGGGTGAGAGCCCCGTACGGTTGGACGCCTAGCCTCTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATTTCTTCTAAAGCTAAATAC
TGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGCA
GGGTTAAATAGCACGTGAAATTGTTGAAAGGGAAGCGTTTATCACCAGACTTTTTCTGGGGGG
ATCATCCGGTGTTCTCACCGGTGCACTTCCCCCAGTTGAGGCCAGCATCGGTTTTCGGAGGGG
GATAAAAGCTTCGGGAATGTGACTCCCTCGGGAGTGTTATAGCCCGTTGCATAATACCCTTCT

78
GGGGACCGAGGTTCGCGCATCTGCAAGGATGCTGGCATAATGGTGATCAACGACCCGTCTTG
AAACACCGGACC
CF-31 Fusarium
ACGGAGGTATGGCCCTTGTAACGGCGTGGTGAACGGCAACAGCTCAAATTTGAAATCTGGCTC
TCGGGCCCGAGTCGTAATTTGTAGAGGATGCTTTCGACGCGGTGCCTTCCGAGTTCCCCGGAA
CGGGACGCCATAGAGGGTGAGAGCCCCGTCCGGTCGGATGCCAAATCTCTGTAAGGCTCTCTT
GACGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAAT
ACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAGAATGAAAAGCACTTTGAAAA
GAGAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGG
TTAATCATCTGGGTTTCTCCCCAGTGCACTTTTCCAGTCCGGGCCAGCATCAGTTTTCGCCGGG
GGTTAAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCT
GCCGGGGACTGAGGTTCGCGCATCTGCAAGGATGCTGSCGTAATGGTCATCAACGACCCGTCG
AAAAAGGCGCACCAACCAAATTTTTAAGGTCGGTTTTTTTAAGAGCTGGTCCCCGCGKTATCC
ACGGCATACATTTCCAGAGGGCATTCCAAGCTTTCCCGGGAAAAGGTGGG
CF-32 Fusarium
CASGGGGCCATTGCCCTAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTC
TCGGGCTGAAAGGGTTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGAACGG
GACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTTCGAC
GAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAATACC
GGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGAG
AGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGGTTAA
TCATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGGGGAT
AAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCTGGCG
GGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCTTGAA
AACACGGACCA
CF-33 Glomerella
CAATTGTTGCCACCGTCACTTCAGATAGAGTAGCCGCCTAGAATCACAGTTCAAATCTGGCCC
CAGGCCCGAGTTGTAATTTGCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAAC
GGGACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTC
GACGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAAT
ACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAA
GAGGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGG
TGAATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTC
GGGGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACC
CTTCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTC
TTGAAAACACGGACCAATGTTCTGATTTGCGGGCGGAGAGCGACCCCCCTCGAAAATATGAA
TCATGTCAATAGGGATTTAAGGTCACCGAAAGAGCCTCGTTCTG
CF-34 Penicillium.

79
CAAGGGGCCTTGCCTCAGTACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCT
CTTTGGGGGTCCGAGTTGTAATTTGTAGAGGGTGTGGCGGGTTCGGCTCCGGTCCAAATTCCT
TGGAACAGGGCGTCATAGAAGGTGAGAATCCCGTACGGGACCGGCGGCTATTCACATGTAAA
GCCCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGTGGTAAATTTCATCTAA
AGCTAAATATTGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACT
TTGGAAAGAGAGTTAAACAGTATGTGAAATTGTTGAAAGGGAAGCGCTTGCAACCAGACTTG
ATCGCGGCTGCTCCTCCCGGTTGGGGCTTCGGCGGTTCCCGTGGGCAGGACCTCACTGGTTGG
GGCTGAAGGTTAAAGGACTTTGGTATGTTCCGGGACTGGTGTAGGCTGATACCGGAAGACCAT
AGGCTACCTGAGGGGACCGATCTCCGCGCATCTGCTCGGATGGTGGCTCAATGACTGTCATCG
ACCCGTCTACCCACCACGGACCA
CF-35 Exserohilum
AGGCACGATTGGCCAAGTATCGGCGATGAACGGAACGCTCAAATTTGGAATCTGGCTCTTTCA
GAGTCCGCGTTGTAATTCGCAGAGGGCGCTTCGGTTTCGGCAGCGGTCCAAGTTCCTCGGAAC
AGGACGTCACACAGCGGGAAGAATCCGTACGTGGTCGCTAGCTATTGCCGTGTAAGGCCCCCT
CGACGAGTCGAGTTGTTCGGGAATGCAGCCCTAAATGGGAGGTAAAATTTCTCTAAAGCTAA
ATATTGGCCAGAGACCGATAGCGAACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGGAA
AGAGAGTCAAACAGCACGTGAAATCGTTGAAGGGGAAGCGCTTGCAGCCAGACTCGCTTGCA
GTTGCTCATCGGGGCTTTTGCCCGGTGCACTCTTCTGCAGGCAGGCCAGCATCAGTTTGGGCG
GTGAGATAAAGGTCTCTGTCACGTACCTCTCTTCGGGGAGGCCCTATAGGGGAGGCGACATAC
CACCAGCCTAGACTGAGGTCCGCGCATCTGTAGGAATGCTGGCGTAATGGGCTGTAAGCGGC
CCTTCTTAAAAAACGCCCCAAGGCCCCCATTGGCGTTACGCGGCATCTACCAATAAAGGGGAC
CTCCTTATAGGGGGGGACGTTAGTGGGCACCCCAATGAAACGCCCCCCCAAAAAAGGGGTCC
TGCAA
CF-36 Fusarium
TCCCGGGGTATTGCCCTAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCT
CTCGGGATGAGAGTGTAATTTGTAGAGGATGCTTTTGATGCGGTGCCTTCCGAGTTCCCTGGA
ACGGGACGCCATAGAGGGTGAGAGCCCCGTCTGGTTGGATGCCAAATCTCTGTAAAGCTCCTT
CGACGAGTCGAGTAGTTTGGGAATGCTGCTCTAAATGGGAGGTATATGTCTTCTAAAGCTAAA
TACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAA
GAGAGTTAAAAAGTACGTGAAATTGTTGAAAGGGAAGCGTTTATGACCAGACTTGGGCTTGG
TTAATCATCTGGGGTTCTCCCCAGTGCACTTTTCCAGTCCAGGCCAGCATCAGTTTTCGCCGGG
GGATAAAGGCTTCGGGAATGTGGCTCTCTCCGGGGAGTGTTATAGCCCGTTGCGTAATACCCT
GGCGGGGACTGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCATCAACGACCCGTCT
TGAAACACGGACC
CF-37 Pleurostoma
CCAAGGGGAATTGCCCCCAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCT-
GGCCTCGGCCCGAGTTGAAATTTGCAGAGGATGCTTCTGGCGCGGTGCCTTCCGAGTTCCCTG
GAACGGGACGCCACAGAGGGTGAGAGCCCCGTATGGTCGGACACCAAGCCAGTGTGAAGCTC
CTTCGACGAGTCGAGTAGTTTGGGAATGCTGCTCTAAGCGGGAGGTATACGTCTTCTAAAGCT
AAATACCGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACCTTGA
AAAGGGGGTTAAACAGTACGTGAAATTGTTGAAAGGGAAGCGCCTGTGACCAGACTTGCGCC
GGGCGGATCATCCAGCGTTCTCGCTGGTGCACTCCGCCCGGCTCAGGCCAGCATCGGTTCTGG
CAGGGGGACAAAGGCGGCGGGAACGTGGCTCCCCCGGGAGTGTTATAGCCCGCCGTGCAATG

80
CCCCTGCCGGGACCGAGGTTCGCGCATCTGCAAGGATGCTGGCGTAATGGTCACCAGCGACCC
GTCTTGAAACACGGAC
CF-38 Alternaria
CCCGGGTATTGCCCTAGTAACGGCGAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCTCT
TTTAGAGTCCGAGTTGRAATTTGCAGAGGGCGCTTTGGCTTTGGCAGCGGTCCAAGTTCCTTG
GAACAGGACGTCACAGAGGGTGAGAATCCCGTACGTGGTCGCTGGCTATTGCCGTGTAAAGC
CCCTTCGACGAGTCGAGTTGTTTGGGAATGCAGCTCTAAATGGGAGGTACATTTCTTCTAAAG
CTAAATATTGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTT
GGAAAGAGAGTCAAACAGCACGTGAAATTGTTGAAAGGGAAGCGCTTGCAGCCAGACTTGCT
TACAGTTGCTCATCCGGGTTTCTACCCGGTGCACTCTTCTGTAGGCAGGCCAGCATCAGTTTGG
GCGGTAGGATAAAGGTCTCTGTCACGTACCTCCTTTCGGGGAGGCCTTATAGGGGAGACGACA
TACTACCAGCCTGGACTGAGGTCCGCGCATCTGCTAGGATGCTGGCGTAATGGCTGTAAGCGG
CCCGTCTTGAAACACAAGGAC
CF-39 Glomerella
AAGAGGTATTGCGTCACAACCGAGCAGTGAAGCGGCAACAGCTCAAATTTGAAATCTGGCCC
CAGGCCCGAGTTGAGCCCCAGAGGATGCTTTTGGTGCGGTGCCTTCCAAGTTCCCTAGAACGG
GACGCCAGAGAGGGTGAGAGCCCCGTACAGTTGGACACCAAGCCTTTGTAAAGCTCCTTCGA
CGAGTCGAGTAGTTTGGGAATGCTGCTCAAAATGGGAGGTATATTTCTTCTAAAGCTAAATAC
CGGCCAGAGACCGATAGCGCACAAGTAGAGTGATCGAAAGATGAAAAGCACTTTGAAAAGA
GGGTTAAACAGCACGTGAAATTGTTAAAAGGGAAGCGCTTGTGACCAGACTTGCGTCCGGTG
AATCACCCAGCTCTCGCGGCTGGGGCACTTCGCCGGCTCAGGCCAGCATCAGCTCGCTGTCGG
GGACAAAAGCTTCAGGAACGTAGCTCTCTTCGGGGAGTGTTATAGCCTGTTGCACAATACCCT
TCGGCGGGCTGAGGTACGCGCTCCGCAAGGATGCTGGCATAATGGTCATCAGCGACCCGTCTT
GAAACACACGGACCAATGTTGACAGATTCCGTGCAGAGCGCGTACCTCAGCCCGCCAAAGGG
TATTGTGCAACAGGCTATAACACTCCCCGAAGAGAGCTACGTTCCTGAAGCT